生物医学研究长期面临着无法精准复刻人体器官微环境、难以突破动物模型种间生物学差异的核心痛点,这直接限制了病理生理机制的深度解析与创新治疗手段的研发。传统二维细胞培养体系无法还原人体组织的复杂三维结构与细胞间相互作用,动物模型则因物种差异难以准确预测人体对药物的真实响应,而微流控芯片技术、类器官培养与 3D 生物打印技术的兴起,为构建高仿生度的体外 3D 模型提供了全新解决方案,也推动了器官芯片、类器官芯片技术成为生物医学工程领域的核心发展方向。
1. 三大核心技术的特性与应用瓶颈
1) 微流控技术
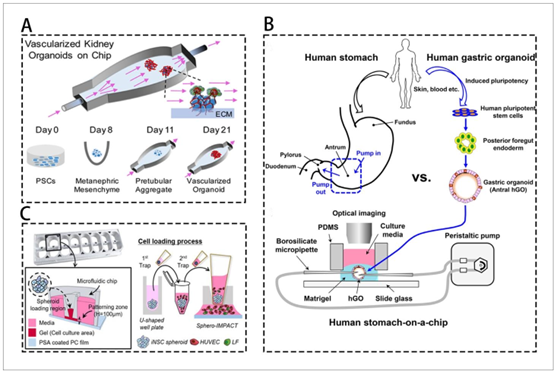
图1. 微流控技术与类器官——第一部分。(A) 在动态微流控芯片上培养的肾类器官展现出更成熟的足细胞和肾小管腔室,同时形成了庞大的可灌注管腔血管网络。经许可改编自参考文献95,版权©《自然》期刊2019年。(B) 置于微流控装置中的胃类器官受到规律性拉伸和收缩刺激,逼真模拟出类似蠕动的胃部运动。经许可改编自参考文献96,版权©英国皇家化学会2018年。(C) 通过将诱导神经干细胞来源的球体与可灌注血管在注塑成型的微流控芯片中共培养,成功构建了血管化脑类器官。经许可改编自参考文献101,版权©威利出版公司2022年。缩写说明:ECM为细胞外基质;hGO为人类胃类器官;HUVEC为人脐静脉内皮细胞;iNSC为诱导神经干细胞;LF为肺成纤维细胞;PC为聚碳酸酯;PDMS为聚二甲基硅氧烷;PSA为压敏胶;PSC为多能干细胞。
微流控技术是在亚毫米尺度下实现流体精准操控的多学科交叉技术,其核心载体为微流控芯片,首款器官芯片便依托该技术成功复刻了人体肺泡 – 毛细血管界面的核心结构与生理功能。该技术可对流体剪切力、营养梯度、机械力刺激等关键参数实现时空精准调控,同时支持模型的实时监测与高分辨率成像,是构建动态仿生微环境的核心工具。
在产业化应用中,PDMS 芯片是当前微流控领域最主流的载体,其制备工艺涵盖光刻、SU8 模具制备、PDMS 浇筑与键合等核心环节,配套的 PDMS 等离子键合机、PDMS 对准平台、PDMS 打孔器、PDMS 烘箱等设备,构成了 PDMS 芯片加工的完整硬件体系。同时,微流控芯片的定制化制备也可依托 MEMS 加工、微纳加工平台实现,通过深硅刻蚀、电子束光刻、薄膜镀膜等工艺,完成玻璃微流控芯片、COC 芯片、PMMA 芯片等不同材质芯片的规模化加工,解决了 PDMS 材料对小分子吸附的局限性。但单一微流控技术仍存在空间塑形能力不足、复杂结构制备精度受限、部分环节依赖人工操作的短板,无法完全还原原生组织的三维复杂结构。
2) 类器官技术
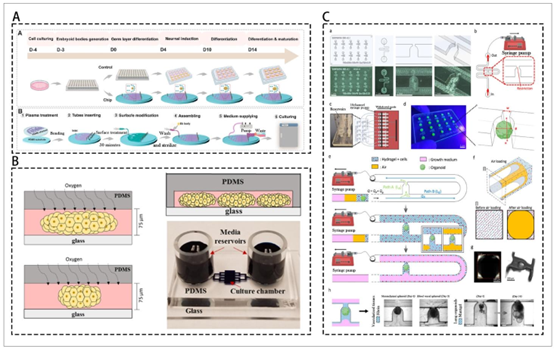
图2. 微流控技术与类器官——第二部分。(A) 具备动态流体扰动和氧合功能的脑类器官-微流控平台可实现超过50天的持续培养。经许可改编自参考文献20,版权归Elsevier所有,©2023。(B) 利用微流控装置或微腔实现膀胱癌类器官的长期培养。经许可改编自参考文献111,版权归Nature所有,©2017。(C) 借助微流控装置实现类器官血管生成的可视化。经许可改编自参考文献98,版权归Nature所有,©2024。缩写:PDMS,聚二甲基硅氧烷。
类器官是由多能干细胞或成体干细胞衍生而来的三维培养体系,可通过自组装形成与原生器官高度相似的结构,复刻组织特异性的细胞异质性、分泌功能与生理活性,是类器官芯片的核心生物组件。患者来源的类器官可完整保留供体的遗传背景,成为个性化药物筛选与精准医疗的核心载体,在肿瘤研究、罕见病建模等领域展现出巨大价值。
但传统静态培养模式下,类器官面临着成熟度不足、长期培养稳定性差、批次间异质性高的核心问题。随着类器官体积增大,单纯依靠扩散的营养与氧气递送效率大幅下降,易导致核心区细胞坏死,同时无法对其发育的物理与生化微环境实现精准调控,限制了模型的生理相关性与数据可重复性。
3) 3D 生物打印技术
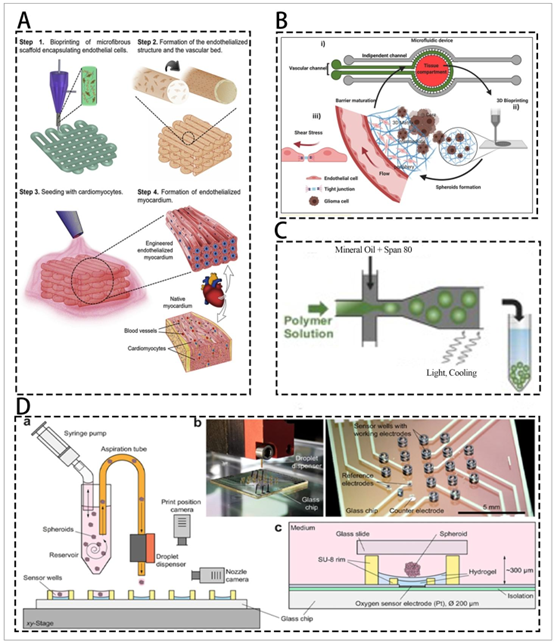
图3 微流控技术与3D生物打印。(A) 3D生物打印的内皮化心肌组织嵌入专为心血管毒性测试设计的微流控装置中。经许可改编自参考文献118,版权© Elsevier 2016。(B) 整合3D生物打印与微流控技术,模拟血脑屏障及邻近的3D血管周围肿瘤微环境。经许可改编自参考文献119,版权© Wiley 2021。(C) 用于实时调控打印细胞浓度的微流控打印头。经许可改编自参考文献123,版权© Wiley 2018。(D) 将肿瘤球状体自动化生物打印至芯片电化学氧传感器微通孔中。经许可改编自参考文献117,版权© 皇家化学会 2022。
3D 生物打印是依托计算机辅助设计,通过层层沉积的方式将生物材料与细胞组装成预设三维结构的创新技术,分为喷嘴基、光基两大主流技术路线,可实现复杂组织架构的高精度、自动化、高通量制备。该技术可通过对打印参数的精准调控,定制化构建仿生支架,为细胞生长与类器官自组装提供物理引导,同时支持多细胞类型的精准空间排布,最大程度还原原生组织的层级结构。
但单一 3D 生物打印技术仍存在明显局限:预成型的支架结构会一定程度上阻碍细胞间的相互作用与物质传递,难以实现营养与代谢废物的高效交换,同时打印过程可能对细胞活性造成损伤,打印结构与原生组织在生理功能上仍存在显著差距。
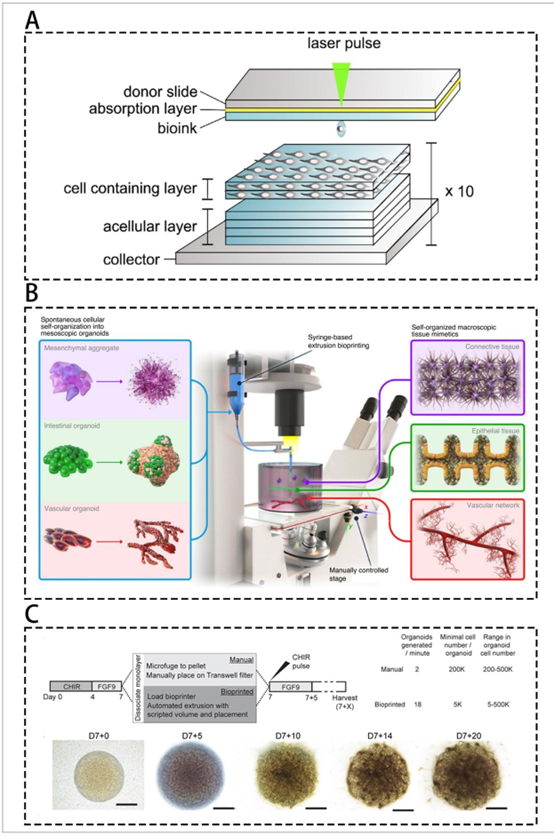
图4 3D生物打印与类器官。(A) 利用人干细胞激光辅助打印分层3D组织,以模拟天然角膜组织。经许可改编自参考文献130,版权© 爱思唯尔2018。(B) 结合3D生物打印和类器官技术,实现从毫米到厘米尺度的自组织调控。经许可改编自参考文献131,版权© 自然出版集团2021。(C) 自动化挤出式生物打印提升了肾脏类器官生产的通量、质量、可扩展性和结构。经许可改编自参考文献127,版权© 自然出版集团2021。缩写:CHIR,CHIR99201;FGF9,成纤维细胞生长因子9。
2. 技术融合的协同优势与实践应用
单一技术的固有局限,推动了技术融合成为体外仿生模型研发的主流趋势,两两融合的技术方案已在细胞培养芯片、多器官芯片研发中实现了广泛应用。
微流控与类器官的融合形成的微流控类器官培养芯片,实现了对类器官培养体系的全面升级。微流控的动态灌注体系,不仅能实现营养与氧气的高效递送,大幅延长类器官的培养周期,还能通过流体剪切力诱导血管内皮细胞的成管分化,显著提升类器官的血管化程度与成熟度。目前该方案已被应用于脑、肾、肝、肺、胃肠等多种类器官芯片的构建,同时依托微流控芯片的集成传感能力,实现了对类器官生长过程的实时成像与动态监测,解决了传统类器官培养数据可读性差的痛点。
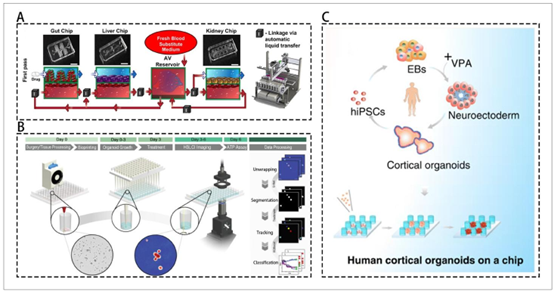
图5. 双技术组合的应用——第一部分。(A) 利用微流控技术和类器官构建药物吸收、代谢和排泄的生理相关药代动力学模型。经许可改编自文献159,版权©《自然》2020年。(B) 高通量肿瘤类器官 动静脉;三磷酸腺苷;拟胚体;人诱导多能干细胞;基于生物打印的高速活细胞药物筛选。经许可改编自文献161,版权©《自然》2023年。(C) 源自人诱导多能干细胞的皮质类器官微流控培养,用于构建早期脑发育和丙戊酸暴露模型。经许可改编自文献163,版权©《自然》2020年。缩写:
微流控与 3D 生物打印的融合,突破了传统微流控芯片空间结构制备的技术瓶颈。3D 生物打印可直接在微流控芯片内构建仿生血管网络与组织支架,比如研究人员通过该技术在微流控装置内构建了内皮化心肌组织,实现了心血管药物的高灵敏度毒性评估;也可打印出包含功能性血脑屏障的胶质瘤微环境模型,为脑肿瘤机制研究提供了高仿生平台。同时,基于微流控原理的打印喷头可实时调控打印细胞浓度,大幅提升 3D 生物打印的分辨率与结构稳定性,也实现了微流控芯片制备的全自动化,降低了人工操作带来的污染风险与批次差异。
类器官与 3D 生物打印的融合,则解决了传统类器官培养随机性强、重复性差的行业痛点。通过挤出式生物打印,可在 10 分钟内完成数百个肾脏类器官的标准化制备,大幅提升了类器官生产的通量与均一性;同时,3D 生物打印可通过仿生支架的设计,引导类器官的定向发育与自组装,构建出结构更复杂的角膜、骨软骨等组织模型,为大规模、标准化的药物筛选提供了可靠的模型载体。
3. 三项技术全整合的行业价值与未来展望
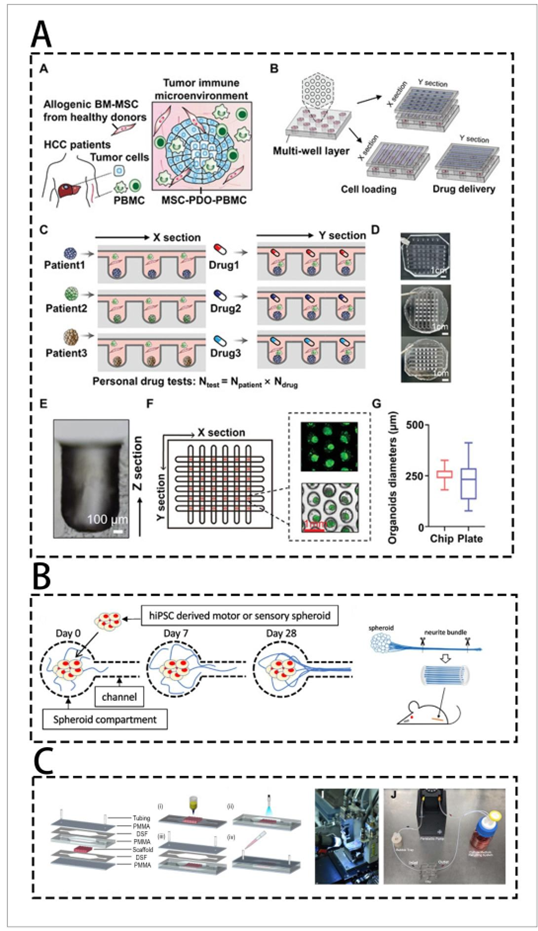
图6 双技术组合的应用——第二部分。(A) 间充质干细胞与外周血单个核细胞共培养构建模拟原始肿瘤微环境的肝细胞癌类器官。经许可改编自参考文献167,版权©威利出版公司2023年。(B) 从人诱导多能干细胞衍生的神经类器官在专用微流控装置中培养,以生成用于移植的人工突触束。经许可改编自参考文献171,版权©施普林格自然2024年。(C) 通过将肝细胞胞外囊泡生物打印到微流控芯片上构建肝芯片模型,以评估重编程的三阴性乳腺癌细胞在体外三维肝脏微环境中的转移行为。经许可改编自参考文献173,版权©IVYSPRING2023年。缩写:BM-MSC,骨髓间充质干细胞;DSF,双尺度流;HCC,肝细胞癌;hiPSC,人诱导多能干细胞;PBMC,外周血单个核细胞;PDO,患者来源类器官;PMMA,聚甲基丙烯酸甲酯。
微流控、类器官与 3D 生物打印三项技术的全整合,突破了双技术融合的局限,构建出生理相关性更高的体外仿生模型,目前已在心血管毒性评估、脑肿瘤机制研究、个性化药物筛选等领域实现了落地应用。整合后的模型,通过 3D 生物打印构建空间支架,依托类器官提供生物功能核心,再由微流控系统实现动态微环境调控与实时监测,形成了功能完整的仿生体系,不仅能更精准地预测药物在人体内的代谢与毒性,大幅降低新药研发的成本与周期,也为罕见病研究、个性化治疗方案制定提供了全新的平台。
当前,行业正探索引入时间维度的 4D 培养体系,该体系以三项技术的融合为基础,通过在组织发育的关键节点精准调控生化信号、物理微环境与空间结构,引导细胞的定向分化与组织的动态发育,进一步缩小体外模型与原生组织的发育差距。而该技术体系的产业化落地,仍依赖于微纳加工、MEMS 代工技术的持续升级,以及 PDMS 芯片加工平台、桌面式光刻机等核心设备的国产化与标准化,同时也需要建立统一的模型制备、性能评估与临床验证标准,推动技术从实验室研究走向临床转化。
总体而言,微流控芯片、类器官与 3D 生物打印技术的深度融合,正在推动体外生物模型从静态结构仿生向动态功能仿生的范式转变。该技术体系不仅为生物医学基础研究提供了强大的工具,也为新药研发、再生医学、个性化医疗带来了革命性的突破,未来随着材料科学、自动化技术与人工智能的深度融合,将在精准医疗领域展现出更广阔的应用前景。
参考文献:doi: 10.36922/IJB025130110
© 2026. All Rights Reserved. 苏ICP备2022036544号-1












