传染病始终是全球公共卫生安全的核心威胁,其高传染性的特征决定了及时、精准的诊断是切断传播链条、控制疫情扩散的关键。传统的传染病检测手段以 qPCR、DNA 测序、酶联免疫吸附试验为核心,虽具备较高的检测精度,却普遍依赖大型精密设备与专业操作人员,不仅检测周期长、试剂消耗量大,更难以在资源受限场景下完成大规模人群筛查。同时,呼吸道感染、热带传染病等多数病症存在症状高度相似的特点,单一靶标检测极易出现漏诊、误诊问题,临床诊断对多重靶标同步检测的需求日益迫切。在此背景下,微流控技术凭借自动化、微型化、集成化的核心优势,成为传染病床旁检测领域的核心研发方向,基于微流控平台搭建的多重检测体系,也为传染病的快速诊断与大规模筛查提供了全新的解决方案。
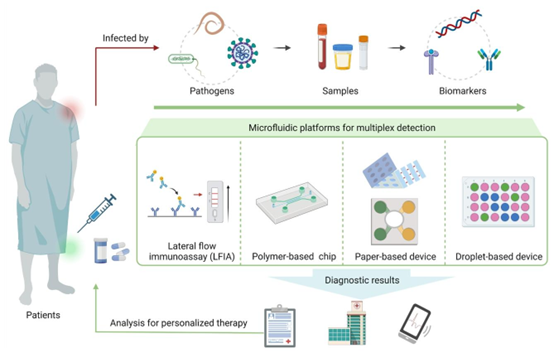
图1. 用于病原体多重检测的微流控平台概述。图1. 用于病原体多重检测的微流控平台概述。
1. 微流控多重检测的两大核心技术体系
微流控平台实现传染病多重检测的核心逻辑,是通过芯片内检测位点的空间分离,在独立的反应体系内完成多靶标同步识别,在避免不同反应体系相互干扰的同时,保障单靶标检测的灵敏度与特异性。目前行业内的主流技术体系分为微流控多重免疫传感与微流控多重核酸传感两大类,二者分别适配不同的检测场景与生物标志物类型。
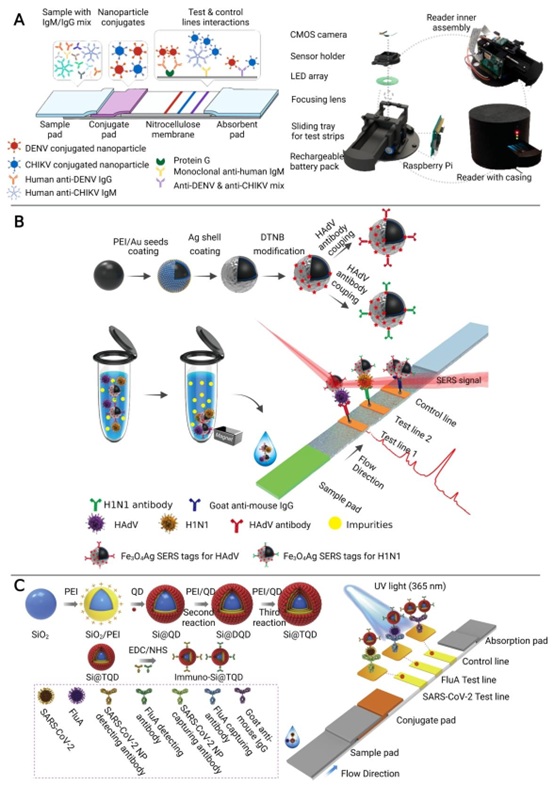
图2 利用微流控免疫传感器对传染病进行多重检测。(A) 登革热病毒(DENV)和基孔肯雅热病毒(CHIKV)IgM/IgG抗体的快速诊断平台,由多重颜色编码的侧向层析检测试纸和光学读数仪组成。经许可引自文献[27]。版权所有2019年,美国化学学会。(B) 基于磁性表面增强拉曼散射-侧向层析免疫分析(magnetic SERS-LFIA)对甲型H1N1流感病毒(H1N1)和人腺病毒(HAdV)的多重检测。经许可引自文献[29]。版权所有2019年,美国化学学会。(C) 基于双通道荧光免疫层析分析对甲型H1N1流感病毒(H1N1)和新型冠状病毒(SARS-CoV-2)的多重检测。经许可引自文献[32]。版权所有2021年,爱思唯尔。
1) 微流控多重免疫传感技术
微流控免疫传感以抗体作为生物识别元件,通过抗原 – 抗体的特异性结合反应,将生物识别事件转化为可量化的物理信号,是目前技术成熟度最高、商业化应用最广的微流控检测技术。该体系主要采用空间复用与条码复用两种多重检测策略,其中毛细管力驱动的侧向流免疫分析(LFIA)平台是最具代表性的产品形态,其完全符合 WHO 提出的 “经济、灵敏、特异、易用、快速、无设备依赖” 的检测标准,仅需在单条试纸条上排布多条检测线,即可通过空间分辨率实现多靶标的区分检测。
根据信号读取方式的不同,LFIA 平台可分为比色、表面增强拉曼散射(SERS)与荧光信号三大技术路线。传统金纳米颗粒比色法凭借操作简便、结果可视化的优势,成为基层检测的主流方案;而 SERS-LFIA 与荧光 LFIA 则通过新型纳米标签材料,将检测灵敏度提升了 2-3 个数量级,可实现新冠病毒、甲型流感病毒、人腺病毒等多种呼吸道病原体的同步定量检测,最低检出限可达到 pfu/mL 级别,大幅拓宽了免疫传感技术的临床应用边界。
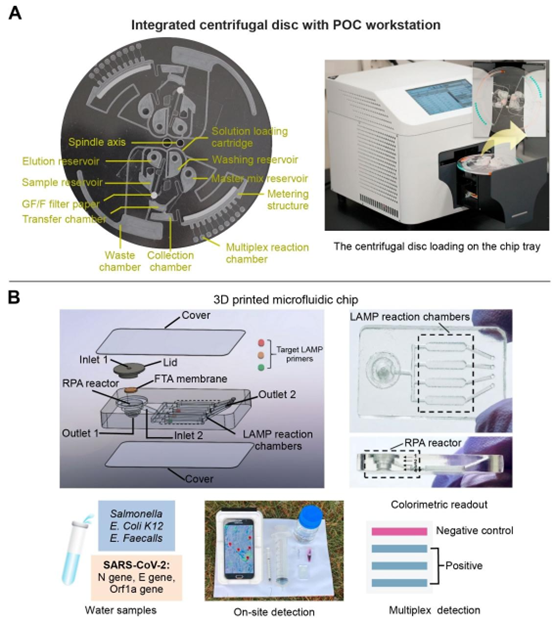
图3 聚合物基微流控芯片对传染病的多重检测。(A) 配备玻璃滤膜萃取柱用于纯化核酸、并设有多个反应室用于多重检测的离心式微流控芯片。经参考文献[63]许可转载。版权所有2021年,Elsevier。(B) 集成了片上核酸提取、两阶段等温扩增和比色检测的3D打印微流控芯片。经参考文献[70]许可转载。版权所有2021年,Elsevier。
2) 微流控多重核酸传感技术
核酸检测是传染病病原鉴定的金标准,微流控多重核酸传感技术突破了传统 PCR 技术对精密热循环设备的依赖,结合等温扩增、CRISPR/Cas 系统等新型核酸检测技术,实现了核酸提取、扩增、检测全流程的芯片内集成,是目前微流控领域的核心研发热点。根据芯片基材与结构的差异,该体系主要分为聚合物基微流控芯片、纸基微流控器件与液滴微流控器件三大类,各类平台均具备试剂消耗低、检测通量高、操作简便的核心优势。
其中聚合物基微流控芯片是自动化与集成度最高的技术路线,PDMS 是该类芯片最常用的基材,凭借良好的生物相容性、低成本与易加工的特性,成为微流控芯片制备的核心材料。PDMS 芯片的微流道结构加工高度依赖 MEMS 加工工艺,通过光刻、电子束光刻、激光刻蚀、注塑成型等微纳加工技术,可在芯片内完成复杂的微结构与流道网络设计,结合离心力驱动、毛细管力驱动等流体控制方式,实现多步连续生化反应的自动化运行。除 PDMS 外,COC、PMMA、玻璃等材料也被广泛用于微流控芯片制备,适配不同的检测场景与加工工艺,目前 3D 打印技术也逐步应用于芯片加工,进一步降低了微流控芯片定制的技术门槛与成本。
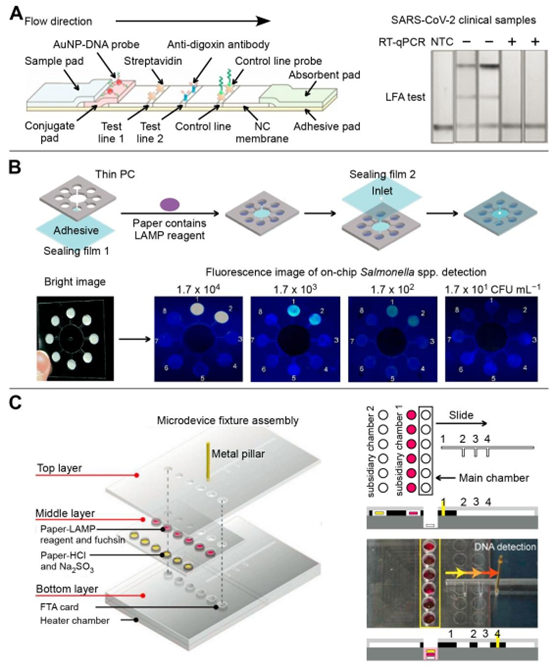
图4. 基于纸基微流控器件的传染病多重检测。(A) 基于CRISPR/Cas9介导的侧向层析分析(LFA)对新型冠状病毒(SARS-CoV-2)的E基因和ORF1ab基因进行多重检测。经许可改编自文献[58],版权所有2021年,WILEY。(B) 采用简易手工切割工艺制备了基于荧光微流控纸基分析器件(µPAD)的环介导等温扩增(LAMP)体系,可同时检测四种病原体。经许可改编自文献[86],版权所有2018年,英国皇家化学会。(C) 通过刻蚀法制备了比色滑动式微流控纸基分析器件(µPAD),可同时检测沙门氏菌属、金黄色葡萄球菌以及大肠杆菌O157:H7。经许可改编自文献[87],版权所有2019年,Elsevier。
2. 主流微流控检测平台的技术特性与产业化现状
目前应用于传染病多重检测的微流控平台,已形成四大主流技术路线,各类平台在检测性能、操作门槛、生产成本与应用场景上形成差异化互补,且均已实现不同程度的商业化落地。
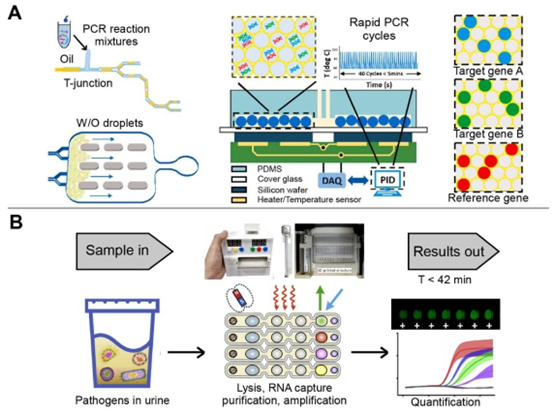
图5 基于液滴的微流控装置对传染病的多重检测。(A)通过T型结构法制备的液滴PCR检测系统。经许可改编自文献[100]。版权所有2021年,爱思唯尔。(B)磁力控制的自动化液滴微流控平台。经许可改编自文献[59]。版权所有2021年,爱思唯尔。
侧向流免疫分析平台是目前商业化最成熟的微流控产品,全球侧向流检测市场规模已突破百亿美元,已有多款呼吸道病毒、热带传染病多重检测产品获批上市,其核心优势在于检测速度快、无需配套设备、非专业人员即可操作,是基层医疗机构与现场快速检测的首选方案。但其仍存在灵敏度有限、定量能力不足的短板,未来需通过高响应信号标记材料与高分辨率检测设备的研发,进一步提升检测性能。
聚合物基微流控芯片是临床高端检测的核心方向,凭借高度集成的自动化流程,可在单芯片内完成 4 种以上病原体的同步检测,检测时间可控制在 90 分钟以内,目前已有 Revogene、GenPlex® 等多款商业化设备获批应用。同时,该类芯片的技术同源性也使其在类器官芯片、器官芯片、3D 细胞培养芯片等领域实现了技术延伸,成为生命科学研究与体外诊断领域的通用技术平台。
纸基微流控器件凭借基材成本极低、无需外部流体驱动的优势,成为资源匮乏地区传染病检测的核心方案,分为侧向流检测试纸与纸基分析设备两大类。该类平台可通过简单的工艺加工完成多通道设计,结合 LAMP 等温扩增与 CRISPR/Cas 技术,可实现多靶标核酸的高灵敏度检测,最低检出限可达到单拷贝级别,目前已有多款产品在传染病防控中实现落地应用。
液滴微流控器件是超高通量多重检测的核心技术路线,通过在芯片内生成皮升至纳升级的单分散液滴,将每个液滴转化为独立的生物反应器,可实现大规模并行生化反应。该平台结合数字 PCR、多重 LAMP 技术,可完成超低浓度病原核酸的定量检测,甚至可实现 169 种人类相关病毒的同步筛查,试剂成本较传统方法降低 300 倍以上,在大规模传染病监测与病原筛查中具备不可替代的优势。
3. 行业挑战与未来发展趋势
尽管微流控平台在传染病多重检测领域已取得显著的技术突破,但其产业化与大规模应用仍面临诸多挑战。在技术层面,多数微流控平台仍需在检测灵敏度、抗干扰能力上实现进一步提升,降低临床样本检测中的假阳性与假阴性问题;在材料与加工层面,PDMS 等聚合物材料的导热性、耐热性仍存在局限,芯片表面修饰技术、微纳加工量产工艺仍需持续优化,微流控芯片加工的成本控制与规模化生产仍是行业核心难题;在商业化层面,微流控检测产品仍需完成大规模临床试验验证,在设备小型化、操作全流程自动化上实现进一步突破,才能真正适配基层与现场检测的实际需求。
从行业发展趋势来看,微流控多重检测技术将朝着三大核心方向演进。其一为多技术深度融合,将 CRISPR/Cas 系统、SERS、荧光量子点等技术与微流控平台结合,在保障检测便捷性的同时,进一步提升灵敏度与多重检测能力;其二为加工技术的升级与成本优化,随着 MEMS 代工、3D 打印技术的成熟,微流控芯片定制与量产的技术门槛将持续降低,推动产品在基层医疗场景的普及;其三为全流程集成化与智能化,通过芯片结构设计实现 “样本进 – 结果出” 的全自动检测,结合智能手机等便携设备完成结果读取与数据分析,真正实现传染病的现场快速诊断与数字化监测。
总体而言,微流控平台凭借多重检测、集成化、便携化的核心优势,正在重塑传染病诊断的技术格局。随着微纳加工技术、材料科学与分子诊断技术的不断进步,微流控芯片将在公共卫生疫情防控、临床床旁诊断、基层传染病筛查中发挥愈发核心的作用,为全球传染病防控体系提供坚实的技术支撑。
参考文献:https://doi.org/10.3390/bios13030410
© 2026. All Rights Reserved. 苏ICP备2022036544号-1












