肝细胞癌(HCC)是全球范围内发病率与致死率居高不下的恶性肿瘤,早期精准诊断是提升患者 5 年生存率、改善临床预后的核心关键。甲胎蛋白(AFP)与 α-L – 岩藻糖苷酶(AFU)是临床公认的肝细胞癌核心生物标志物,传统临床检测方法普遍存在操作流程繁琐、检测周期长、单指标检测局限性强、低浓度样本灵敏度不足等痛点,难以满足临床即时检测与早期筛查的需求。表面增强拉曼散射(SERS)技术凭借超高检测灵敏度、分子指纹特异性识别、非破坏性检测的核心优势,成为生物标志物微量检测领域的研究热点,而传统 SERS 基底普遍存在活性位点分布不均、信号重复性差、难以与自动化检测流程兼容的问题,限制了其临床转化应用。
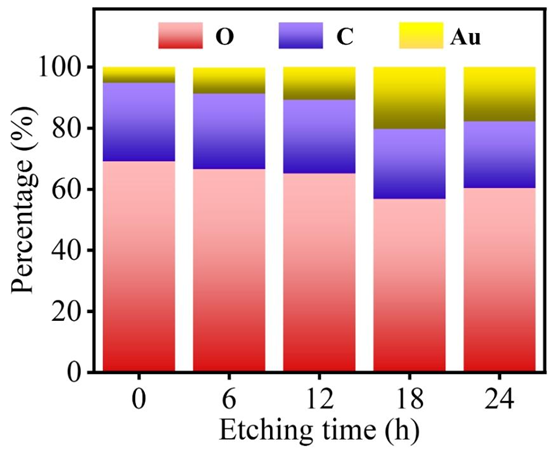
图S1。SAHMs上的金负载量随刻蚀时间的变化而变化。
微流控芯片技术凭借微纳尺度下流体的精准操控能力,可实现生物检测流程的微型化、集成化与全自动化,与 SERS 技术的联用成为突破上述技术瓶颈的核心方案。依托成熟的微纳加工、MEMS 加工工艺,可实现高精度 PDMS 芯片、玻璃芯片、COC 芯片的定制化制备,结合光刻、深硅刻蚀等微纳制造技术,能够构建功能化的微流道结构,为液滴生成、免疫反应、信号检测提供稳定的微尺度反应环境,同时该技术体系也可广泛适配细胞培养芯片、类器官芯片、器官芯片等生命科学研究场景,具备极强的技术扩展性。
1. 核心材料体系与微流控制备工艺
本研究以聚乙二醇二丙烯酸酯(PEGDA)水凝胶微球为载体,通过微流控辅助的微纳加工技术,构建了具备 3D 分级褶皱结构的 SERS 活性水凝胶微球(SAHMs),形成了高性能的 SERS 检测基底。实验核心材料体系涵盖 PEGDA、氯金酸(HAuCl₄・3H₂O)、柠檬酸钠等基础试剂,以孔雀绿异硫氰酸酯(MGITC)、3,3′- 二乙基噻二碳菁碘化物(DTDC)为拉曼报告分子,搭配 AFP、AFU 对应的单克隆抗体与牛血清白蛋白(BSA),构建了完整的免疫传感体系,所有反应均在磷酸盐缓冲液(PBS)体系中完成,保证了生物反应的活性与稳定性。

图S2。褶皱结构的俯视图(a)和侧视图(b)。
在基底制备环节,核心依托微流控液滴生成技术制备单分散性优异的 PEGDA 水凝胶微球,所使用的微流控芯片采用标准 PDMS 芯片制备工艺完成加工:通过光刻技术制备 SU8 模具,结合 PDMS 浇筑、固化、脱模工艺完成微流道结构的制备,再通过等离子键合机完成 PDMS 芯片与载玻片的不可逆键合,配合 PDMS 对准平台实现芯片的高精度封装,最终构建的微流控液滴芯片可稳定生成尺寸均一的水凝胶微球液滴,经光引发聚合后得到单分散水凝胶微球(HMPs)。后续通过刻蚀工艺在微球表面构建 3D 分级褶皱微纳结构,刻蚀时间的精准调控可实现微球表面金负载量的定量控制,BET 比表面积测试结果证实,分级微纳结构的引入大幅提升了微球的比表面积,为金纳米颗粒(AuNPs)的锚定与抗体的固定提供了充足的活性位点。
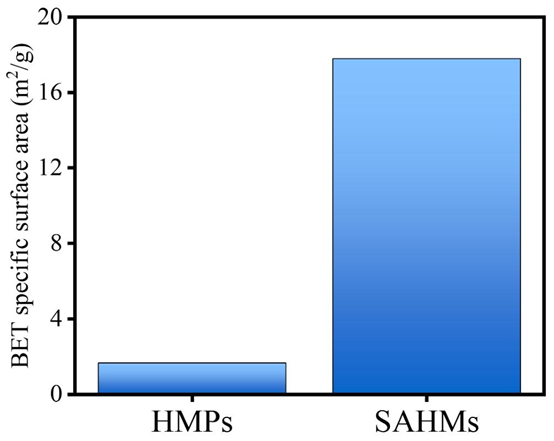
图S3。HMPs和SAHMs的BET比表面积。
为实现免疫传感的特异性识别,研究通过表面修饰工艺完成了捕获抗体在 SAHMs 表面的固定,结合紫外吸收光谱与朗伯 – 比尔定律完成了抗体固定量的定量表征,最终实现每个 SAHM 上约 0.91ng 功能化捕获抗体的稳定固定。同时通过优化工艺,完成了检测抗体与拉曼报告分子共修饰的 SERS 纳米标签制备,经 BSA 封闭非特异性结合位点后,纳米标签具备优异的胶体稳定性与生物活性,为后续的 “三明治” 免疫检测奠定了基础。

图S4。(a-b) 超疏水阵列微加热器的示意图与扫描电子显微镜图像。(c) 超疏水阵列微加热器上电-场分布的COMSOL仿真结果。
2. SERS 基底性能表征与检测体系验证
增强因子(EF)是评价 SERS 基底性能的核心指标,本研究以 10⁻⁶ M 的 MGITC 为探针分子,通过激光共聚焦拉曼显微镜系统完成性能测试,激发光源为 632.8nm 的 He-Ne 激光器,经 50 倍物镜聚焦后形成约 1.5μm 的激光光斑,最终通过公式计算得到该 3D 微纳分级 SERS 基底的增强因子可达 1.5×10⁸,证实了其具备极强的拉曼信号增强能力。同时通过 COMSOL 有限元仿真,模拟了分级微纳结构与 AuNPs 表面的电场分布,结果显示微纳褶皱结构与相邻 AuNPs 之间形成了大量高密度的电磁场 “热点” 区域,这是基底实现超高信号增强的核心物理机制。
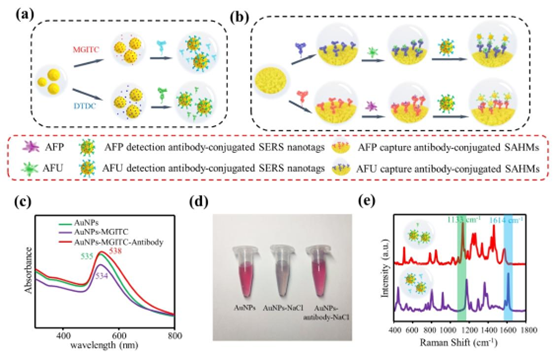
图S5。(a) 制备两种不同类型抗体偶联SERS纳米标签的连续流程。(b) 在SAHMs上构建“夹心”免疫复合物的步骤。(c) 金纳米颗粒与带检测抗体的SERS纳米标签的紫外-可见吸收光谱。(d) 盐老化实验的照片。(e) 两种单独纳米标签(DTDC和MGITC)的SERS光谱。
研究同时完成了基底信号均一性、稳定性的系统验证,通过拉曼 mapping 成像技术,对负载免疫复合物的 SAHMs 进行面扫描检测,结果显示 SERS 信号在整个微球表面分布均匀,无明显的信号波动,解决了传统平面 SERS 基底信号重复性差的行业痛点。此外,实验优化了 AuNPs 与两种拉曼报告分子的配比,通过盐老化实验验证了 SERS 纳米标签的长期稳定性,同时明确了 MGITC 在 1614cm⁻¹、DTDC 在 1133cm⁻¹ 的特征拉曼峰互不干扰,为双标志物的同步定量检测提供了基础。
3. 双标志物检测性能与行业应用前景
基于优化后的 SERS 基底与纳米标签,研究构建了 “三明治” 免疫传感结构,在微流控芯片中完成了 AFP 与 AFU 双标志物的自动化同步检测,整个检测流程总时长仅需 1 小时 40 分钟,远优于传统手动操作的免疫检测方法。在检测性能上,该体系对 AFP 的线性检测范围为 0.1-100 ng/mL,对 AFU 的线性检测范围为 0.01-10 ng/mL,线性范围完全覆盖临床血清样本中标志物的浓度区间,同时具备极低的检出限与优异的抗干扰能力,对 BSA、PSA、凝血酶等常见干扰蛋白无明显非特异性响应,可适配复杂临床样本的检测需求。
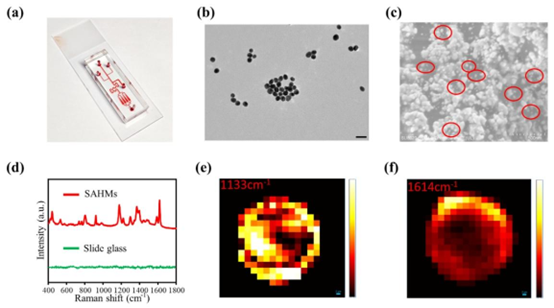
图S6。(a) 含红墨水的表面增强拉曼散射(SERS)检测微流控芯片照片。(b) 金纳米颗粒(AuNPs)的典型透射电子显微镜(TEM)图像,比例尺为100纳米。(c) 免疫复合物分布在超亲水自组装单层膜(SAHMs)上的表面增强拉曼散射纳米标签扫描电子显微镜(SEM)图像。(d) 超亲水自组装单层膜(SAHMs)上10⁻⁶摩尔浓度异硫氰酸玫瑰红(MGITC)的表面增强拉曼散射(SERS)光谱,以及其在载玻片上的常规拉曼光谱。(e-f) 从结合甲胎蛋白(AFP)和α-L-岩藻糖苷酶(AFU)的\(50 ng mL^{-1}\)的超亲水自组装单层膜(SAHMs)上获得的免疫复合物表面增强拉曼散射(SERS)成像图,比例尺为2微米。
与已报道的电化学、荧光、光电化学等检测方法相比,该微流控 – SERS 联用技术同时实现了双指标同步检测、全流程自动化操作、高灵敏度与高特异性,在临床即时检测(POCT)场景中具备显著的应用优势。从技术扩展性来看,该微流控辅助的 SERS 基底制备技术具备极强的通用性,仅需更换对应的抗体或适配体,即可拓展到其他肿瘤标志物、心血管疾病标志物、病原微生物等检测场景;同时其核心的微流控芯片制备、微纳加工与表面修饰工艺,可广泛适配 3D 细胞培养芯片、类器官芯片、器官芯片的开发与应用,为药物筛选、生命科学基础研究提供核心技术支撑。
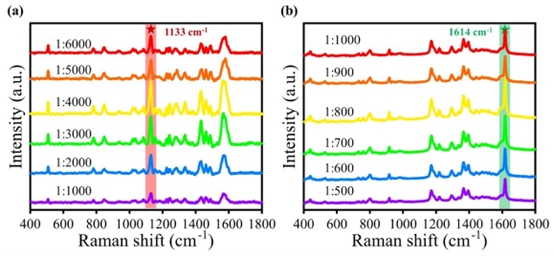
图S7。不同金纳米颗粒与报告分子DTDC(a)和MGITC(b)比例的纳米标签表面增强拉曼散射(SERS)光谱。
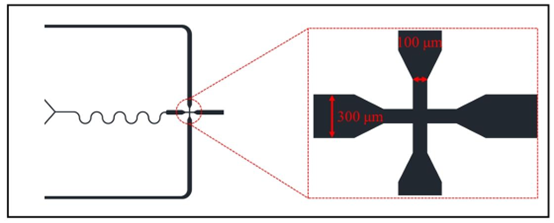
图S9。微液滴生成单元的计算机辅助设计(CAD)图
随着微流控芯片加工、微纳制造技术的不断成熟,PDMS 芯片、玻璃芯片、COC 芯片等不同材质微流控芯片的定制化加工与代工体系日趋完善,微流控技术与 SERS、光学检测、电化学检测等技术的联用,已成为体外诊断、生物医药领域的核心发展方向。本研究构建的微流控 – SERS 检测体系,不仅为肝细胞癌的早期快速检测提供了全新的技术方案,也为微纳生物传感技术的临床转化提供了可参考的技术路径,具备重要的科研价值与产业化应用潜力。
参考文献:College of Control Science and Engineering, China University of Petroleum (East China), Qingdao 266580, China.
© 2026. All Rights Reserved. 苏ICP备2022036544号-1




