微流控技术在过去 20 年间实现了跨越式发展,已从实验室基础研究逐步落地到生命科学分析、环境监测、临床分子诊断等多个核心场景。其中连续流微流控技术已实现广泛普及,而液滴微流控凭借独立微反应单元操控、超高通量分析、单分子级检测灵敏度的核心优势,成为当下微流控领域的研究热点,更是病毒检测、单细胞分析、数字核酸扩增等高端应用的核心技术载体。传统微流控系统多基于平面微通道网络构建微流控芯片,无论是 PDMS 芯片、玻璃微流控芯片,还是 COC/PMMA 材质的塑料微流控芯片,虽已实现成熟应用,但在光学耦合效率、系统集成度、现场原位检测适配性上仍存在难以突破的瓶颈。2019 年以来的全球公共卫生事件,更是凸显了可全球部署、快速响应、高灵敏度的床旁核酸检测技术的迫切需求,而本文献所提出的光纤内实验室(Lab-in-a-Fiber)光流控器件,正是针对这一行业痛点,完成了液滴微流控与激光诱导荧光(LIF)检测技术的全光纤集成,为微流控诊断技术的便携化发展提供了全新路径。
1. 器件核心设计与微纳加工工艺
该光纤内实验室器件采用模块化设计,核心分为液滴生成模块与光学检测模块两大单元,全程依托成熟的微纳加工与 MEMS 加工工艺完成制备,最大程度保障了器件的性能稳定性与批量化制备潜力。
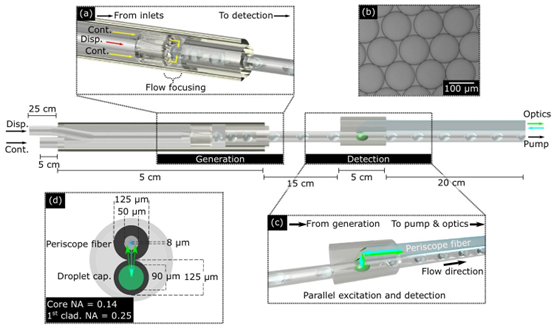
图1. 光纤实验室装置概述。该装置由两个模块组成。(a)通过流动聚焦产生的分散相液滴。五孔毛细管的中心孔通入分散相,外部四个孔通入连续相油。一根次级毛细管放置在靠近五孔毛细管出口的位置,迫使油进入分散相路径,通过流动聚焦促进液滴生成。(b)由1μM荧光素产生的液滴的宽场显微镜图像。经测量,它们的直径约为120μm。(c)液滴的荧光检测。激发光的传输和荧光发射的收集通过一个潜望镜光纤(一根以45°角切割并涂有铝的双包层光纤(DCF))在轴上实现。(d)给出了横截面。潜望镜光纤与液滴毛细管平行固定的截面图。潜望镜光纤的8μm纤芯用于将连续波(CW)激光耦合到下方的液滴,如蓝色箭头所示。诱导荧光通过50μm的第一包层区域收集,如绿色箭头所示。请注意,光纤实验室装置的长度未按比例显示,仅显示了每个部分的指示性长度。
液滴生成模块采用单轴同轴的毛细管流聚焦结构,区别于传统平面微流控芯片的正压驱动模式,创新性地采用负压驱动方案,更适配现场原位进样的使用需求。模块核心由五孔毛细管与单根 90μm/125μm 内径 / 外径毛细管熔融拼接而成,通过精密的微流道加工工艺,实现了 30μm 孔径流道的精准成型,配合后续的精密切割、毛细管对准与紫外胶封装,形成完整的流聚焦单元。通过流体阻力的精准计算与流路长度优化,器件可稳定生成直径约 120μm、体积约 0.9nL 的单分散液滴,液滴生成频率稳定在 41±0.5Hz,同时通过硅化试剂对通道内壁进行疏水修饰,避免了水相液滴与通道壁的非特异性吸附,这也是微流控芯片制备过程中保障液滴稳定性的核心工艺环节。
光学检测模块是该器件的核心创新点,研究团队开发了一款侧向耦合的潜望镜光纤,解决了传统微流控芯片中激光诱导荧光检测需要垂直光路、系统体积大、光学对准难度高的行业痛点。该潜望镜光纤以双包层光纤(DCF)为基底,通过精密划片切割在光纤端面制备 45° 斜角,再通过真空镀膜工艺完成 70nm 铝层的镜面沉积,最终形成可实现 90° 光路转向的光纤探针。该结构可同时完成激发光的侧向投射与荧光信号的同轴收集:8μm 纤芯用于 488nm 激发光的耦合输出,50μm 内包层用于荧光信号的高效收集,全程无需外置复杂的显微光路,实现了检测模块与微流控流路的同轴集成,器件最大外径仅 333μm,主体部分外径仅 125μm,具备优异的柔性与生物化学惰性,远超传统硬质微流控芯片的现场适配性。

如图2所示(插图中显示),其中五个孔的直径各为30微米。(b)对毛细管进行熔接,确保五孔毛细管的四个外孔保持开放,且90微米/125微米的毛细管未塌陷。图2. 液滴生成模块。我们光纤器件外壳毛细管的液滴生成模块的制造步骤,如图1(a)所示。(a)将一根90微米/125微米的毛细管对准五孔毛细管的中心孔(端面)。(c)将五孔毛细管切割至约200微米的长度。(d)将五孔毛细管段插入255微米/333微米外壳毛细管的左侧。(e)将一根125微米/250微米的毛细管插入外壳毛细管的右侧,并使其与五孔毛细管的出口孔保持约100微米的距离。(f)将第二根90微米/125微米的毛细管插入左侧。
2. 器件性能表征与关键技术突破
研究团队以荧光素为标记物,完成了器件的全性能表征,验证了其在生物检测场景下的实用性与可靠性。通过 10nM 至 100μM 宽范围的荧光素浓度梯度测试,器件建立了 10nM 的荧光素检测下限(LOD),这一指标与传统主流的实验室级微流控芯片平台相当,完全满足核酸扩增产物的荧光检测需求。同时,团队通过对连续 1000 个液滴的峰宽监测,验证了液滴流速与尺寸的长期稳定性,排除了流速波动对荧光检测结果的干扰,保障了定量检测的准确性。
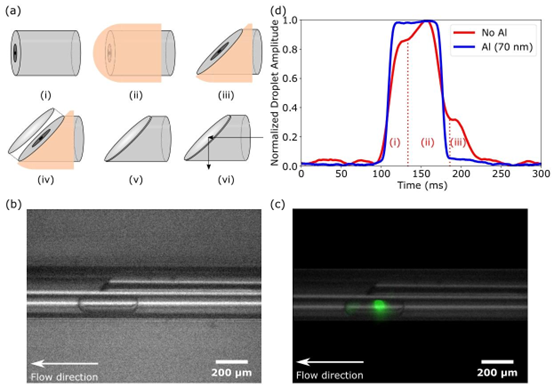
图3. 液滴检测模块。(a) 潜望镜光纤的分步制造过程。(i) 对双包层光纤(DCF)进行平切。(ii) 使用真空安全涂料遮蔽光纤尖端。(iii) 在切割机器上,沿与光纤轴法线成45°角的方向切割DCF。(iv) 对暴露的切割表面进行铝镀膜。(v) 通过丙酮和超声处理去除遮蔽物。(vi) 耦合到光纤近端的光在尖端垂直于传播轴射出。(b) 液滴检测模块的白光显微镜图像,其中潜望镜光纤固定在液滴毛细管上方(连续波激光器关闭),参见补充视频1。(c) 与(b)相同视野的荧光显微镜图像(连续波激光器开启),为清晰起见,叠加了器件的透明图层。可以看到绿色荧光集中在潜望镜光纤下方的液滴中,参见补充视频2。(d) 使用光纤实验室器件获得的1μM荧光素液滴的归一化分布图,该器件分别采用无铝层的潜望镜光纤(红线)和有铝层的潜望镜光纤(蓝线)制成。
该研究实现了三大核心技术突破,填补了行业内的技术空白:其一,首次实现了液滴微流控技术从平面芯片向全光纤结构的完整转化,既保留了液滴微流控的单分散性与数字检测潜力,又赋予了器件光纤级的光学耦合效率与集成度,解决了传统平面微流控芯片光学集成难度大的核心问题;其二,创新的单端负压驱动模式,区别于传统微流控芯片需要双端进样的复杂流路设计,仅通过近端负压即可实现远端进样,大幅简化了现场检测的操作流程,为原位采样检测奠定了技术基础;其三,同轴集成的激光诱导荧光检测模块,实现了激发与检测光路的一体化设计,无需复杂的外部光学对准,为微型化、便携化的床旁检测设备开发扫清了核心障碍。
3. 病毒检测应用验证与行业发展价值
为验证器件在实际临床诊断场景的适用性,研究团队以新冠病毒核酸为检测靶标,完成了 RT-LAMP 扩增产物的检测验证。实验结果显示,在室温条件下,器件即可实现阴性与阳性样本的有效区分,信噪比达 1.5;在 65℃的等温扩增标准温度下,引物二聚体引发的背景荧光被显著抑制,阴性样本信号大幅降低,检测信噪比提升至 3.6,充分证明了器件在核酸扩增诊断相关荧光区间内的稳定工作能力,也为数字液滴 RT-LAMP 床旁检测平台的开发提供了全新的技术路径。
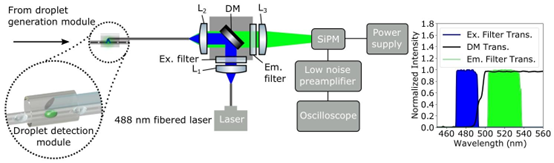
图4. 用于操作光纤实验室装置的光学器件和硬件。488 nm光纤耦合激光器的激发光通过光纤端口(\((L_{1})\))进行准直。光通过激发滤光片(Ex.滤光片)后,经二向色镜(DM)反射至第二个光纤端口\((L_{2})\),该端口用于将光耦合到光纤实验室装置中。收集到的荧光穿过二向色镜(DM)和发射滤光片(Em.滤光片)。右侧显示了该滤光片组的归一化透射光谱。消色差聚光透镜\((L_{3})\)将光松散地聚焦到硅光电倍增管(SiPM)上。硅光电倍增管的信号通过低噪声前置放大器耦合到示波器,该前置放大器用作1 kHz低通滤波器。
从行业发展角度来看,这项技术有着极高的应用与产业化价值。首先,光纤器件拥有成熟的规模化制备产业链,可实现公里级的标准化生产,相较于定制化微流控芯片的复杂加工流程,该器件具备更低的量产成本与更高的批间一致性,为低成本诊断设备的普及提供了可能。其次,该技术框架具备极强的拓展性,不仅可用于各类病毒、细菌的核酸检测,还可拓展至单细胞分析、类器官芯片培养在线监测、环境污染物原位检测等多个领域,适配多场景的微流控分析需求。此外,全光纤的结构设计可直接与内窥镜等医用介入设备结合,拓展至在体原位检测与分析场景,这是传统平面微流控芯片难以实现的应用边界突破。
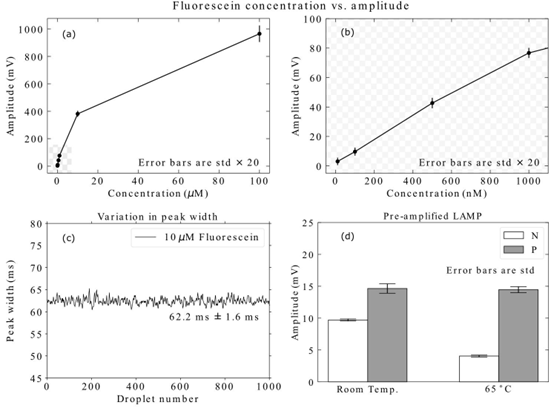
图5. 使用RT-LAMP检测法的表征及结果。(a)以荧光素作为替代荧光团对光纤实验室装置进行表征。每个点代表20,000个液滴,误差棒代表标准差×20以保证可见性。正如预期的那样,在高浓度下可以观察到荧光团的淬灭现象。(b)(a)中棋盘区域的放大图,显示了在观察到淬灭效应之前,较低浓度下的线性荧光区域。(c)1000个连续液滴的液滴峰宽代表性测量结果,表明液滴速度稳定。(d)预扩增SARS-CoV-2 RT-LAMP样本的结果。白色填充表示RNA阴性样本(N)。灰色填充表示RNA阳性样本(P)。实验在(左)室温及(右)65℃下进行。即使在室温下,阴性和阳性样本也可区分,但65℃下阴性样本背景荧光的抑制提高了分辨率。
4. 技术局限与未来发展方向
当前该器件仍存在一定的优化空间,研究团队也明确了后续的技术发展方向。在性能提升上,目前器件的荧光收集效率不足 5%,主要受限于双包层光纤的数值孔径,后续可通过大数值孔径光纤的结构优化,进一步提升检测灵敏度与信噪比;液滴生成频率目前为 41Hz,与 kHz 级的高通量液滴微流控芯片仍有差距,可通过缩短流路长度、优化流道内径实现分析通量的大幅提升。在功能集成上,当前仅完成了预扩增产物的检测,未来可集成模块化温控单元与孵育腔室,实现从样本进样、核酸扩增到荧光检测的全流程集成,打造 “样本进 – 结果出” 的一体化检测系统。
在产业化落地层面,后续可结合光刻、电子束光刻、深硅刻蚀等成熟的 MEMS 加工工艺,优化器件的自动化组装流程,进一步提升器件间的一致性,降低制备成本;也可拓展至多通道的多功能光纤器件,集成微流控操控、多通道光学传感、实时成像等多个功能模块,应对多靶标并行检测、器官芯片多参数长期监测等复杂应用场景,持续推动光纤内实验室技术在微流控与生物医学领域的深度应用。
总体而言,这项研究开发的光纤内实验室光流控器件,成功打破了传统平面微流控芯片的技术局限,将液滴微流控与激光诱导荧光检测技术完美集成于全光纤结构中,不仅为病毒核酸诊断提供了高灵敏度、便携化的全新技术方案,更开辟了光纤内实验室技术在微流控领域的全新发展方向,为低成本、高性能的床旁检测设备的普及奠定了坚实的技术基础。
参考文献:https://doi.org/10.1038/s41598-022-07306-0
© 2026. All Rights Reserved. 苏ICP备2022036544号-1












