1. 引言:纳米药物困境与微流控技术的崛起
纳米药物作为精准医疗的核心载体,凭借其高比表面积、靶向递送能力,在癌症治疗、基因疗法等领域展现出巨大潜力。然而,传统纳米颗粒(NPs)制备方法(如薄膜水合法、高压均质化)存在诸多局限:颗粒尺寸不均、批间差异大、有机溶剂残留、封装效率低等问题,严重制约了纳米药物的临床转化。在此背景下,微流控芯片技术以其精准的流体操控能力,成为突破传统制备瓶颈的关键技术,为纳米药物的规模化、标准化生产提供了全新解决方案。
微流控芯片基于微纳加工与 MEMS 加工技术,通过微米级通道实现流体的精准混合与反应控制,结合光刻胶模具、SU8 模具等精密成型工艺,可实现芯片结构的高精度复刻。目前,PDMS 芯片因光学透明性、易加工性及良好的生物相容性,成为微流控领域的核心载体,而 PMMA、COC 等材料则凭借优异的化学稳定性,在特殊药物制备场景中广泛应用。这些芯片的加工过程需依赖微纳加工平台、对准平台等专业设备,通过表面修饰技术(如 PEG 修饰、氨基修饰、环氧基修饰)进一步优化生物相容性与靶向性,为纳米药物制备提供了稳定可靠的反应环境。
2. 微流控技术的核心优势与材料体系支撑
1) 核心技术优势:突破传统制备瓶颈
微流控芯片技术的核心优势在于 “精准可控”,通过 hydrodynamic focusing(流体聚焦)等技术,实现有机相和水相的连续、均匀混合,从而制备出尺寸均一(PDI≤0.3)、单分散性好的纳米颗粒。与传统方法相比,微流控技术无需复杂的后处理步骤,可一次性完成纳米颗粒的合成与修饰,显著降低批间差异,同时减少有机溶剂用量,提升药物封装效率(部分体系可达 80% 以上)。
此外,微流控芯片的通道结构可通过光刻、MEMS 加工技术灵活设计,结合 PDMS 浇筑器、打孔器等配套设备,实现不同反应需求的定制化开发。例如,针对脂质体、固体脂质纳米颗粒(SLN)、聚合物纳米颗粒等不同类型的纳米药物,可通过调整芯片通道尺寸、流体流速比(FRR)、总流速(TFR)等参数,精准调控颗粒粒径(10-250nm),满足不同给药场景的需求。
2) 材料体系与加工工艺:筑牢技术应用基础
微流控芯片的性能发挥高度依赖材料选择与加工工艺。PDMS 作为最常用的芯片材料,具备低玻璃化转变温度(-125℃)、易塑形、光学透明等优势,可通过软光刻、等离子键合技术实现通道结构的精准制备,搭配 PDMS 对准平台、键合对准平台,确保芯片封装的密封性与稳定性。在特殊场景中,PMMA 芯片凭借低成本、机械强度高的特点,通过溶剂压印、热键合工艺批量生产;COC 芯片则以优异的耐溶剂性,成为有机相反应体系的优选。
芯片加工过程中,光刻胶模具、SU8 模具发挥着关键作用,通过 MEMS 加工工艺实现微米级通道的精准复刻,结合微纳加工平台的精密控制,确保芯片通道的尺寸一致性。同时,表面修饰技术(如 PEG 修饰、氨基修饰、醛基化修饰)可优化芯片表面亲疏水性,减少药物吸附损失,提升纳米颗粒的生物相容性与循环稳定性,为纳米药物的体内应用奠定基础。
3. 微流控在纳米药物制备中的具体应用场景
1) 脂质体纳米药物:精准调控与高效封装
脂质体作为临床应用最广泛的纳米载体之一,其传统制备方法存在粒径分布宽、封装效率低等问题。微流控芯片技术通过流体聚焦模式,将脂质有机相(如乙醇溶液)与水相在 PDMS 芯片的微通道中快速混合,利用磷脂分子的自组装特性,一次性制备出单分散性脂质体,粒径可精准控制在 90-230nm。
在实际应用中,微流控芯片可与表面修饰技术协同,通过 PEG 修饰、氨基修饰等方式提升脂质体的长循环能力与靶向性。例如,针对乳腺癌治疗的多药共载脂质体,可在 PDMS 芯片中实现阿霉素与紫杉醇的协同封装,结合 HER2 抗体修饰,显著提升肿瘤靶向递送效率。此外,SU8 模具与光刻胶模具的精准加工,确保了芯片通道的均匀性,为脂质体的规模化生产提供了可能。

图1. 空白脂质体制备的薄膜水合方法。通过该方法制备的脂质体通常具有多分散性;然而,旋转蒸发步骤的时间与所产生的薄膜质量之间存在相关性。水合后的混合速度和温度等因素也会影响脂质体的质量,因此必须对这些因素进行监控。

图2. 溶剂注入法制备空脂质体的流程示意图。溶剂注入法中需要考虑的主要因素是注入时的温度(这会因各个脂质的相变温度不同而有所变化)和注入速率。这些因素会影响所制备脂质体的大小、形状和多分散性。溶剂注入后,通常需要采用微挤出等后续方法来获得具有治疗可行性的制剂。
2) 固体脂质纳米颗粒(SLN):稳定性与控释性提升
SLN 作为脂质体的重要补充,具备稳定性高、药物控释效果好等优势,但传统高压均质化方法易导致颗粒团聚、批间差异大。微流控技术通过精准控制脂质熔融相与水相的混合速率,利用微纳加工形成的微米级通道实现剪切分散,制备出粒径均一(120-250nm)、PDI<0.2 的 SLN,封装效率较传统方法提升 30% 以上。
在芯片设计中,MEMS 加工技术确保了通道的精准尺寸,结合 PDMS 芯片的温度可控性,可实现脂质的快速冷却结晶,避免药物渗漏。例如,紫杉醇负载的 SLN 通过微流控芯片制备后,经 PEG 修饰可延长体内循环时间,在肺癌模型中展现出更强的肿瘤抑制效果。同时,微流控芯片可与芯片加工设备联动,实现 SLN 的连续化生产,满足工业化需求。

图3. 使用聚碳酸酯滤膜通过挤出法制备脂质体。增加通过膜的挤压次数会降低制剂的多分散性。该过程还应在与脂质相变温度相近的温度下进行,以防止挤出时脂质断裂(以及随后的脂质体破裂)。
3) 聚合物纳米颗粒与混合体系:多功能化定制
聚合物纳米颗粒(如 PLGA、PCL)凭借良好的生物降解性,在基因递送、药物控释中应用广泛。微流控芯片通过溶剂扩散法,在 PDMS 芯片中实现聚合物与药物的快速混合与沉淀,制备出粒径可控的纳米颗粒,结合表面修饰技术(如氨基修饰、羧基修饰)可提升细胞摄取效率。
脂质 – 聚合物混合纳米颗粒(LPHNPs)则融合了脂质的生物相容性与聚合物的稳定性,微流控芯片通过多通道流体混合,实现 PLGA 核心与脂质外壳的精准组装,经 DSPE-PEG 修饰后,显著提升靶向递送能力。例如,索拉非尼负载的 LPHNPs 通过微流控制备,在肝癌模型中展现出更低的毒性与更高的肿瘤富集效率。

图4. 利用微流控系统制备脂质体的示意图。图4. 利用微流控系统制备脂质体的示意图。图改编自Weaver等人[152]。改编自Weaver等人[152]。
4) 无机纳米颗粒:高纯度与均一性控制
微流控技术同样适用于金纳米颗粒、量子点、磁性纳米颗粒等无机纳米药物的制备。通过气体段塞微流控技术,可实现氧化铁纳米颗粒的快速合成,粒径变异系数小于 10%,纯度显著高于传统方法。这些无机纳米颗粒可与微流控芯片集成,用于肿瘤成像与协同治疗,结合 MEMS 加工的微电极阵列,实现药物释放的精准调控。
4. 微流控与器官芯片 / 细胞培养的协同创新
微流控芯片与细胞培养芯片、器官芯片的融合,为纳米药物的体外评价提供了全新平台。类器官芯片、3D 细胞培养芯片通过 PDMS 芯片加工设备构建仿生微环境,模拟体内组织的生理结构,可实时监测纳米药物的细胞摄取、毒性及疗效。
例如,肝器官芯片、肺器官芯片通过微流控技术实现营养物质与药物的精准递送,结合表面修饰的载玻片(如醛基玻片、羧基玻片)固定细胞,可模拟纳米药物在体内的代谢过程。3D 细胞培养芯片则通过微流道加工形成三维培养空间,更真实地反映纳米药物对肿瘤细胞的抑制效果,为临床前研究提供可靠数据。此外,微流控芯片与器官芯片的集成,可实现 “制备 – 检测” 一体化,显著缩短纳米药物的研发周期。
5. 行业应用与未来展望
1) 行业应用场景拓展
微流控芯片技术已在癌症治疗、基因递送、疫苗研发等领域实现突破。在癌症治疗中,靶向性纳米药物通过微流控制备并经表面修饰后,可精准识别肿瘤细胞,降低对正常组织的损伤;在基因递送中,siRNA 负载的纳米颗粒通过 PDMS 微流控芯片制备,结合 PEG 修饰提升稳定性,成功实现体内基因沉默。此外,MEMS 代工、芯片代工服务的成熟,为中小企业提供了低成本的微流控芯片定制方案,推动技术的普及应用。
2) 未来发展趋势
未来,微流控技术将朝着 “集成化、规模化、智能化” 方向发展。3D 打印微流控芯片将简化光刻胶模具、SU8 模具的加工流程,降低成本;与过程分析技术(PAT)的结合,可实时监测纳米颗粒的粒径、封装效率,实现制备过程的闭环控制。同时,微流控芯片与数字微流控、AI 技术的融合,将进一步提升流体操控的精准度,推动个性化纳米药物的研发。
在材料方面,新型生物相容性材料(如亲水修饰的 PDMS、可降解聚合物)将进一步提升芯片的生物安全性;表面修饰技术的创新(如长效亲水处理、靶向分子修饰)将增强纳米药物的靶向性与循环稳定性。此外,微流控技术与 MEMS 加工、微纳加工的深度融合,将实现芯片功能的多元化,为纳米药物的临床转化提供更强大的技术支撑。
微流控芯片技术凭借其精准的流体操控能力、与微纳加工 / MEMS 加工的高度兼容性,以及与表面修饰、器官芯片的协同创新,彻底改变了纳米药物的制备模式。从 PDMS 芯片的基础加工到类器官芯片的功能集成,从脂质体的规模化生产到个性化纳米药物的定制,微流控技术正成为纳米医药行业的核心驱动力。随着材料技术、加工工艺的持续进步,微流控芯片将在精准医疗领域实现更广泛的应用,为疾病治疗带来革命性突破。
参考文献: https://doi.org/10.3390/nano11123440
Dxfluidics product ( standard PDMS chip)
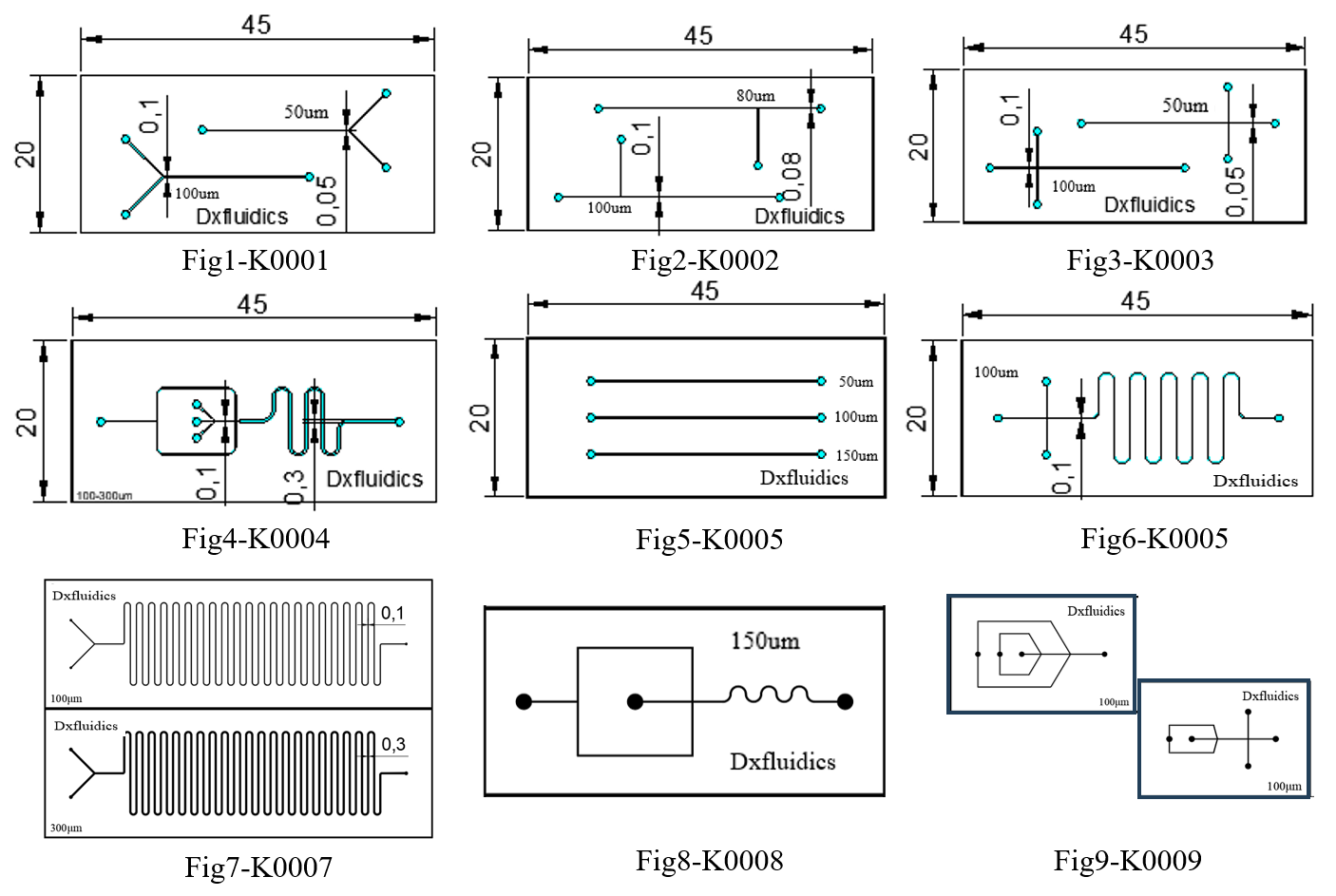
Our company also provides customized microfluidic PDMS chip processing services. For specific details, please feel free to contact us at +86-17751163890 (also available on WeChat) or email:sale@dxfluidics.com.
| Product Code | Outline (mm) | Height (um) | Width (um) | Thickness (mm) | Chip material | Price (CNY) |
| K0001 | 45*20 | 50 | 50&100 | 3+1 | PDMS+Glass | 300 |
| K0002 | 45*20 | 50 | 80&100 | 3+1 | PDMS+Glass | 300 |
| K0003 | 45*20 | 50 | 50&100 | 3+1 | PDMS+Glass | 300 |
| K0004 | 45*20 | 50 | 100&300 | 3+1 | PDMS+Glass | 300 |
| K0005 | 45*20 | 50 | 50&100&150 | 3+1 | PDMS+Glass | 300 |
| K0006 | 45*20 | 50 | 100 | 3+1 | PDMS+Glass | 300 |
| K0007 | 75*25 | 100 | 100&300 | 3+1 | PDMS+Glass | 300 |
| K0008 | 52*25 | 100 | 100&150&200 | 3+1 | PDMS+Glass | 300 |
| K0009 | 35*24 | 100 | 100&200 | 3+1 | PDMS+Glass | 300 |
Ordering Methods



© 2026. All Rights Reserved. 苏ICP备2022036544号-1











