在骨关节炎(OA)研究中,传统单培养模型因缺乏细胞间通讯、动物模型因物种差异难以精准模拟体内关节微环境,成为制约病理机制研究与药物研发的关键瓶颈。为此,近期研究团队开发了微流控芯片在骨关节炎关节炎症模型中的应用相关技术,通过整合多类人体细胞与精密微环境调控,构建出接近生理状态的健康与疾病体外模型,为 OA 研究突破传统局限提供了全新路径。本文将系统解析该微流控共培养系统的构建原理、核心优势、技术支撑及应用前景,深入阐述其在骨关节炎基础研究与临床转化中的价值。
参考文献:DOI 10.3389/fphar.2025.1579228
1. 微流控芯片在关节炎症模型中的构建与创新
模型构建中,通过向培养基添加 IFN-γ 和脂多糖(LPS)诱导巨噬细胞向 M1 表型分化,精准复现了 OA 的炎症微环境。这种设计不仅纳入了骨、软骨、滑膜组织来源的细胞,还通过微流控系统的流动控制实现了细胞间的旁分泌信号传递,较传统静态培养更接近在体关节的多组织交互特性。此外,该系统采用患者来源的原代细胞而非诱导多能干细胞(iPSCs),避免了干细胞分化不均导致的表型偏差,提升了疾病模拟的准确性。
2. 微流控技术的核心优势与实验验证
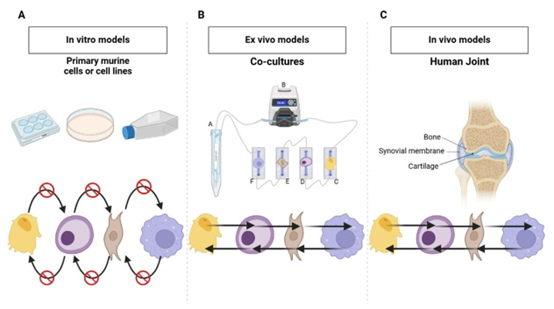
传统 OA 研究模型存在显著缺陷:单培养模型无法复现关节内骨、软骨、滑膜组织的细胞间交互,动物模型则因生理差异导致实验结果难以向人体转化。针对这一问题,研究团队以微流控芯片在骨关节炎关节炎症模型中的应用为核心目标,开发了多细胞共培养系统。
该系统采用 PDMS 芯片加工技术与 MEMS 工艺,基于 μ-Slide I Luer 微流控芯片,成功整合人类成骨细胞(接种密度 40,000 cells/cm²)、软骨细胞(80,000 cells/cm²)、成纤维细胞(替代滑膜成纤维细胞)及巨噬细胞(M0 静息态、M1 促炎态),实现了可控流动环境下的细胞共培养。为精准复现 OA 炎症微环境,研究通过向培养基添加 IFN-γ 与脂多糖(LPS),诱导 M0 巨噬细胞向 M1 表型分化,同时利用流体流动实现细胞间旁分泌信号传递 —— 这一设计较传统静态培养更贴近体内关节的多组织交互特性,且采用患者来源原代细胞(非 iPSCs),有效避免了干细胞分化不均导致的表型偏差,显著提升疾病模拟准确性。
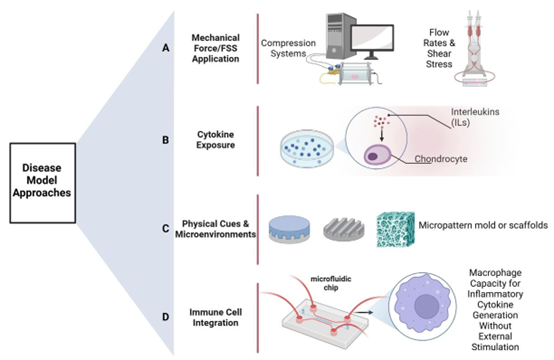
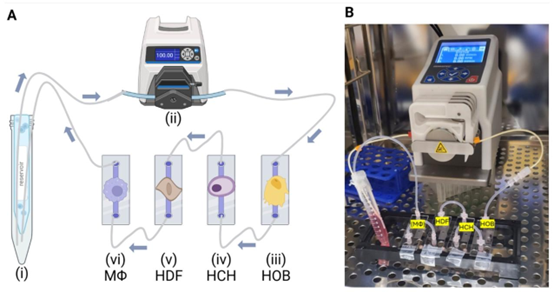
微流控芯片在骨关节炎关节炎症模型中的应用之所以具备创新性,核心源于三大技术优势:
- 精准空间分布:通过 PDMS 键合对准平台,使成骨细胞、软骨细胞等在各自微通道内有序接种,既保障细胞特异性生长环境,又为细胞间交互提供结构基础;
- 仿生机械刺激:采用 Masterflex® peristaltic pump调控 0.05 dyn/cm² 的流体剪切应力,模拟关节滑液流动对细胞的机械刺激,同时促进营养交换与代谢物排出,解决静态培养中 “营养匮乏、代谢堆积” 问题;
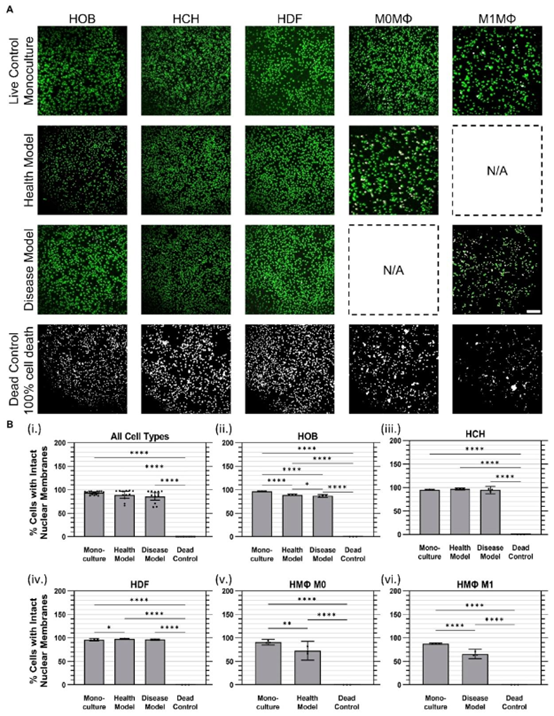
- 多维度评估体系:结合 NucBlue™/NucGreen™活死细胞染色、PrestoBlue™代谢活性检测及 LDH 细胞毒性 assay,全面验证模型稳定性。
实验数据进一步证实模型可靠性:共培养 24 小时后,健康模型与疾病模型的细胞存活率分别达 83.9%±14%、83.3%±12%,与单培养(93.3%±4%)无显著差异,且 LDH 释放量未升高,表明细胞膜完整性未受细胞毒性影响;更关键的是,共培养细胞代谢活性显著增强 —— 健康模型、疾病模型代谢水平分别是单培养的 5.9±3.2 倍、5.3±3.4 倍,直接证实细胞间通讯对维持生理功能的积极作用。
1. 引用 Ibidi 公司 μ-Slide I Luer 芯片技术说明页面,链接:https://ibidi.com/µ-slide-i-luer.html;
2. 引用 WHO 关于骨关节炎的疾病定义页面,链接:https://www.who.int/news-room/fact-sheets/detail/osteoarthritis;
3. 引用 Nature Reviews Rheumatology 关于 OA 体外模型的综述,链接:https://www.nature.com/nrrheum/articles?type=review-article
3. 关键技术支撑与加工工艺
微流控芯片在骨关节炎关节炎症模型中的应用依赖精密的芯片加工与细胞体系设计:
- 芯片加工:以 PDMS 为基材,通过光刻胶模具制备与 PDMS 浇筑工艺实现微通道精准成型,通道尺寸与细胞接种密度匹配(如软骨细胞 80,000 cells/cm²),确保细胞贴壁与生长空间;结合 MEMS 技术完成微通道密封与流体接口设计,配合蠕动泵形成闭环流动系统,满足 24 小时静态共培养与动态营养交换的双重需求。
- 细胞体系优化:采用人真皮成纤维细胞替代滑膜成纤维细胞,通过共培养旁分泌信号弥补功能差异;巨噬细胞由 THP-1 单核细胞经 PMA 诱导为 M0 表型后,再用 IFN-γ+LPS 处理获得 M1 表型,标准化流程确保炎症模型稳定性。
4. 应用前景与技术拓展
当前微流控芯片在骨关节炎关节炎症模型中的应用已展现两大核心价值:一是作为病理研究平台,可解析 M1 巨噬细胞分泌的炎症因子对软骨降解的调控机制,探索骨 – 软骨 – 滑膜的交互病理过程;二是作为药物筛选工具,通过模拟疾病状态下的细胞应答,评估抗炎药物、软骨保护剂的 efficacy 与安全性,降低动物实验成本与物种差异风险。
未来技术优化方向包括:细胞层面引入肥大细胞、浆细胞完善炎症网络;环境调控层面通过流动速率调节施加机械应力,模拟关节运动刺激;加工工艺上结合 3D Cell Culture Chip与细胞外基质(ECM),提升微环境仿生度;更可与器官芯片平台融合,构建 “关节 – 代谢器官” 联动模型,探索 OA 与全身代谢的关联。
© 2026. All Rights Reserved. 苏ICP备2022036544号-1













