血液分析是现代临床诊断的基石,从常规血常规检测到癌症、感染性疾病的早期筛查,都依赖于对血液中细胞和分子成分的精准分析。2026 年发表于《Lab on a Chip》的最新综述系统梳理了血液微流控领域的突破性进展,将血液样本处理分为全血、稀释血、裂解全血、裂解稀释血四大类,详细阐述了不同制备方式对应的微流控技术方案,同时深入探讨了芯片材料、制备工艺与临床转化面临的核心挑战,为下一代血液诊断设备的研发提供了全面的技术框架。
1. 血液样本制备体系与微流控技术适配
血液的复杂组成(红细胞占比约 45%,白细胞和血小板仅占 1%)是微流控处理的核心难点,不同的样本预处理方式直接决定了微流控芯片的设计逻辑和性能表现。
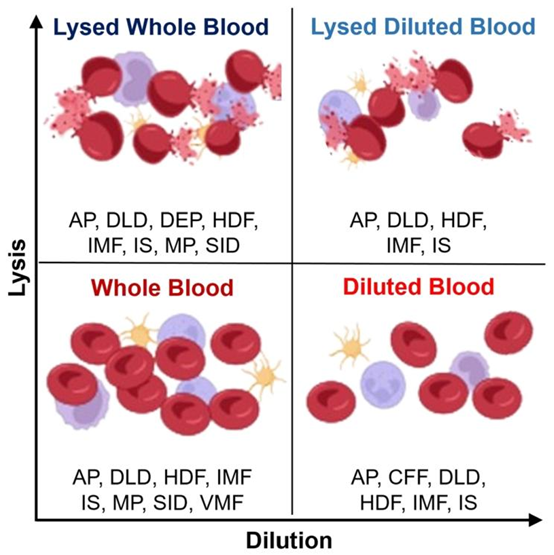
图1 血样制备技术及其对细胞完整性和浓度的影响。该图从裂解(纵轴)和稀释(横轴)两个维度对微流控系统中的制备方法进行了分类。四个象限分别代表全血、稀释血、裂解全血和裂解稀释血。每个象限列出了适用于对应血液类型的微流控技术,包括声泳(AP)、确定性侧向位移(DLD)、介电泳(DEP)、流体动力过滤(HDF)、惯性微流控(IMF)、免疫选择(IS)、磁泳(MP)、剪切诱导扩散(SID)、粘弹性微流控(VMF)以及错流过滤(CFF)。这些技术的选取基于已发表的文献,且已被证实可在指定血液类型上运行。不过,许多最初为全血开发的方法可借助样品稀释或红细胞裂解来提升分离分辨率并减少堵塞。
稀释血是目前应用最广泛的样本类型,通常采用 1:10 的 PBS 稀释比例降低细胞密度,减少微通道堵塞风险,同时稳定流体动力学特性。惯性微流控、确定性侧向位移、声泳等主流技术均能在稀释血样本中实现高效分离,例如螺旋惯性微流控芯片可从稀释血中分离出循环肿瘤细胞(CTC),回收率可达 69%-72%。
裂解全血技术通过选择性裂解红细胞保留白细胞和稀有细胞,大幅简化了样本处理流程,避免了稀释带来的分析物浓度降低问题。集成了红细胞裂解与惯性聚焦的微流控芯片,可实现 88% 的 CTC 回收率和 80% 的白细胞去除率,且分离后的细胞保持高活性,适合下游分子分析。
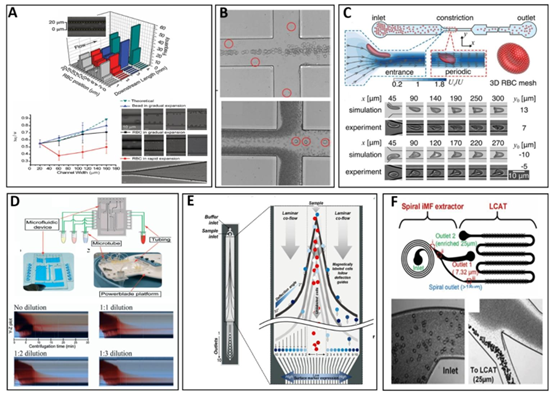
长度增加。经约翰威立父子公司许可转载自参考文献101,版权所有2010年。(B) 明场图像,展示了通道壁附近较小细胞的分离以及较大细胞通过中心通道排出的情况。根据知识共享署名-非商业性使用许可条款转载自参考文献102,图2 稀释血液的微流控处理。(A) 连续可扩展血液过滤装置。红细胞处于平衡状态的高速明场图像 版权所有2023年。(C) 红细胞剪切模量的测量。微流控芯片设计示意图,附带红细胞三维模型及效率对比。经皇家化学会许可转载自参考文献106。集成螺旋惯性微流控技术与横向腔声换能器(LCAT)装置示意图。在\(200 \mu L min^{-1}\)处20微米通道宽度内显示细胞分离位置的明场图像,以及展示通道宽度内红细胞位置频率的直方图,下游模拟和实验图像显示红细胞在微通道不同位置的变形情况。经皇家化学会许可转载自参考文献103。(D) 自动化离心微流控平台装置示意图。使用ATPS系统对不同稀释度血液进行分馏的时序图像,显示离心过程中出现明显分层。经皇家化学会许可转载自参考文献104。(E) Prism Chip中使用的钴基带状棱镜偏转芯片示意图,展示了磁标记细胞如何根据其磁性沿偏转路径导向,实现循环肿瘤细胞及细胞团簇的高分辨率分离。经美国化学会许可转载自参考文献105。(F) 细胞群的高通量表型选择性富集。
全血直接处理是血液微流控的终极目标,无需任何预处理的特性使其成为床旁诊断的理想选择。剪切诱导扩散、拐点聚焦等新型被动技术已实现从全血中富集白细胞和 CTC,其中拐点聚焦技术对 HeLa 细胞的分离效率可达 92.6%,但仍面临通道堵塞和细胞激活的挑战。
裂解稀释血则主要用于核酸和蛋白质提取,结合等速电泳(ITP)和重组酶聚合酶扩增(RPA)的集成芯片,可在 75 分钟内完成全血中李斯特菌的检测,为败血症的快速诊断提供了新方案。
2. 核心微流控分离技术与芯片设计创新
血液微流控分离技术可分为被动、主动、免疫选择和混合四大类,各类技术的优势互补推动了芯片性能的持续提升。
被动技术无需外部能量输入,依靠微通道几何结构产生的流体力学力实现细胞分离,具有高通量、低成本、易集成的特点。惯性微流控利用惯性升力和迪恩阻力的平衡使细胞聚焦到特定平衡位置,是目前最成熟的无标记分离技术;确定性侧向位移通过周期性微柱阵列实现尺寸依赖的细胞位移,可精确分离直径差异仅 1μm 的细胞。
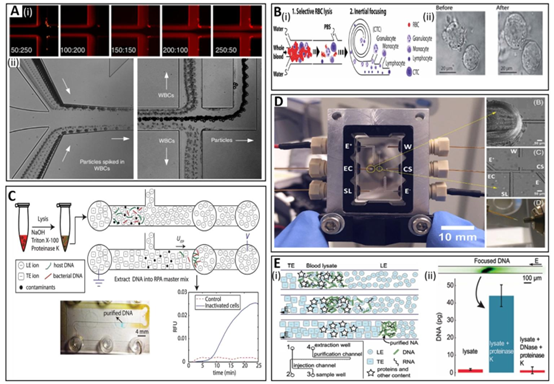
图3 裂解稀释血液的微流控处理。(A) (i) 不同流速比下样本和缓冲液流的荧光图像(\((Q)\) \(Q_{b})\)),显示出有效实现从裂解稀释血液中分离循环肿瘤细胞的流控效果。(ii) 明场图像展示了白细胞悬液中添加颗粒的分离情况,证明了该设备能够从裂解稀释血液中分离循环肿瘤细胞。转载自参考文献68,依据知识共享署名4.0许可协议发布,版权所有2019年。(B) (i) 用于红细胞选择性裂解和有核细胞惯性分离的设备示意图。(ii) 显示细胞在低渗溶液(超纯水)中发生溶胀的图像。经英国皇家化学会许可转载自参考文献75。(C) 等速电泳-重组酶聚合酶扩增检测流程示意图。该流程概述了利用氢氧化钠、曲拉通X-100和蛋白酶K裂解添加了单核细胞增生李斯特菌的全血,随后进行等速电泳纯化和重组酶聚合酶扩增检测的过程。整个流程总时长在50分钟以内,重组酶聚合酶扩增检测还需额外25分钟。经英国皇家化学会许可转载自参考文献109。(D) 连接了流体和电气装置的组装式微流控设备,展示了用于高效处理和加工血液样本的设计。经约翰威立出版公司许可转载自参考文献110,版权所有2022年。(E) (i) 基于等速电泳的核酸纯化流程示意图。(ii) 柱状图显示了从经蛋白酶K处理的裂解物中纯化得到的核酸质量,同时展示了等速电泳通道内聚焦的DNA区域图像。经美国化学会许可转载自参考文献111,版权所有2009年。
主动技术通过电场、磁场、声场等外部能量场操控细胞,具有更高的分离精度和灵活性。声泳技术利用声波产生的辐射力分离细胞,对细胞损伤极小,已实现全血中血小板和单核细胞的高效富集;磁泳技术结合免疫磁珠标记,可实现目标细胞的特异性捕获,是 CTC 分离的主流技术之一。
免疫选择技术基于抗原 – 抗体的特异性结合,通过抗体功能化的微通道表面或磁珠捕获目标细胞,具有极高的特异性。Prism Chip 利用棱柱形偏转结构分离磁标记的 CTC,实现了 5.7 log 的白细胞去除率,且能保留细胞的增殖能力。
混合技术结合了被动和主动技术的优势,成为高性能微流控芯片的发展方向。CTC-iChip 集成了确定性侧向位移、惯性聚焦和磁泳三种技术,可在 1 小时内处理 8mL 全血,CTC 回收率高达 97%,是目前临床转化最成功的血液微流控平台之一。
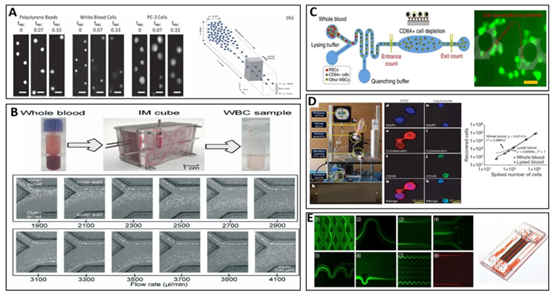
图4 全血裂解液在微流控技术中的应用。(A) 在长宽比为2:1的直微通道中,流速为450 μL \(min-1\)时的颗粒聚焦情况。在红细胞体积分数(fRBC)更高的初始样本中,可识别出单个聚焦的颗粒,且荧光信号质量无明显下降。经英国皇家化学会许可,转载自参考文献66。(B) 经IMF立方体制备的白细胞样本。图像展示了10 μm和4 μm颗粒在不同流速下的分布。经英国皇家化学会许可,转载自参考文献69。(C) 基于差异表达的细胞计数技术示意图。将10 μL全血与裂解缓冲液和淬灭缓冲液一同注入生物芯片,以优先裂解红细胞(比例尺:40 μm)。依据知识共享署名4.0协议转载自参考文献63,版权所有2017年。(D) 循环肿瘤细胞(CTC)分离的工作站搭建。硅基上刻有微柱的CTC芯片。针对不同靶细胞浓度的捕获效率进行回归分析,对比全血与裂解血样本。该图为添加的细胞数与回收的细胞数关系图。合并图像可识别循环肿瘤细胞和造血细胞。经Springer Nature许可,转载自参考文献116,版权所有2007年。(E) 白细胞在磁分选仪中从入口到出口不同位置的荧光条纹图像(插图1-7)。插图8为产物端口分离出的循环肿瘤细胞的荧光条纹图像。同时展示了微加工磁分选仪装置的图像。经作者许可转载,原文发表于《美国国家科学院院刊》,版权所有2020年美国国家科学院。
3. 芯片材料与制备工艺的关键突破
微流控芯片的材料选择和制备工艺直接影响其性能、成本和量产能力,是血液微流控技术临床转化的关键环节。
PDMS 芯片凭借光学透明、弹性好、生物相容性优异的特点,成为实验室研发阶段的首选材料。PDMS 芯片制备流程包括 SU8 模具制作、PDMS 浇筑、脱模、PDMS 键合和打孔等步骤,PDMS 键合机、PDMS 对准平台和 PDMS 工作站等专用设备的普及,大幅提升了芯片的制备精度和重复性。然而,PDMS 存在小分子吸附、批次间差异大、耐溶剂性差等缺陷,限制了其在临床和量产场景的应用。
热塑性材料如 COC 芯片、PMMA 芯片和 PC 芯片,具有优异的化学稳定性、低吸附性和可注塑量产的优势,正逐渐成为商业化微流控芯片的主流材料。这些材料兼容注塑、热压印等大规模制备工艺,且能耐受高压灭菌,更符合临床诊断的要求。
微纳加工技术的进步为微流控芯片的发展提供了坚实基础。光刻、深硅刻蚀、阳极键合等 MEMS 加工工艺可制备出高精度的微通道、微柱阵列和微电极结构;微纳加工平台的开放共享,降低了微流控芯片的研发门槛,推动了技术的快速迭代。此外,芯片表面修饰技术如 PEG 修饰、氨基修饰、醛基修饰等,可有效减少非特异性吸附,提升细胞捕获的特异性和灵敏度。
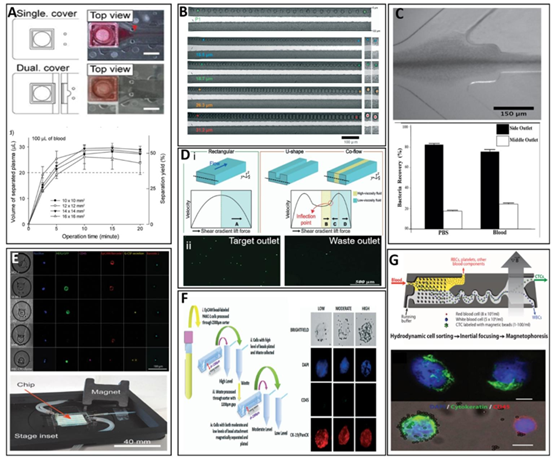
《科学进展》。利用高速成像对全血中四种粒径(直径分别为15.5微米、18.7微米、26.3微米和31.2微米)的颗粒进行成像。经英国皇家化学会许可,转载自参考文献42。(C)非牛顿流体(聚环氧乙烷)中血细胞的弹性惯性聚焦。转载自图5 微流控技术中全血的应用。(A)全血应用于单盖板和双盖板装置。红色箭头指示参考文献121,基于知识共享署名4.0国际许可协议转载,版权所有2017年。(D)(i)不同通道设计的流速剖面示意图;(ii)[此处原文缺失对应机构名称,按原文保留]学会的荧光显微镜图像。(G)CTC-iChip系统可在阳性分离模式(如图所示)或阴性耗竭模式下运行。这些图像展示了posCTC-iChip详细的细胞分析和成像能力。转载自参考文献125,版权所有2013年,美国[此处原文缺失对应机构名称,按原文保留]协会。(图中)比例尺为4毫米。基于知识共享署名4.0国际许可协议转载自参考文献120,版权所有2021年。(B)展示了出口区域的尺寸依赖性迁移,显示了荧光标记的HeLa细胞的空间分离。经英国皇家化学会许可,转载自参考文献122。(E)用于循环肿瘤细胞捕获和分析的微流控芯片设计与操作。基于知识共享署名4.0国际许可协议转载自参考文献123,版权所有2020年。(F)根据三种不同上皮细胞黏附分子(EpCAM)水平分离细胞的流程示意图。展示了基于EpCAM表达水平分离的循环肿瘤细胞(CTC)的明场和免疫荧光图像,比例尺为20微米。经英国皇家化学会许可,转载自参考文献124。
4. 现存挑战与未来发展方向
尽管血液微流控技术取得了显著进展,但仍面临诸多挑战制约其广泛临床应用。全血处理中的通道堵塞问题仍是最大瓶颈,即使是最先进的芯片也难以长时间稳定处理大体积全血;血液细胞的激活和损伤会影响检测结果的准确性;不同患者血液样本的个体差异也增加了芯片标准化的难度。
未来,血液微流控技术将朝着集成化、自动化、智能化的方向发展。集成了样本处理、分离、检测和分析的全流程芯片,将大幅简化临床操作流程;AI 技术与微流控的融合,可通过机器学习优化微通道设计和流体控制参数,提升芯片的鲁棒性和适应性;3D 打印微流控芯片技术的成熟,将实现芯片的快速定制和低成本生产。
同时,血液微流控技术与器官芯片的结合将开辟新的应用领域。血管器官芯片、肿瘤类器官芯片等都依赖精准的血液流动模拟和细胞相互作用研究,血液微流控技术将为药物筛选、疾病机制研究提供更接近生理环境的实验平台。
综上所述,血液微流控技术已从实验室研究逐步走向临床应用,材料科学、微纳加工技术和人工智能的交叉融合,将推动下一代血液诊断设备的革新,为精准医疗和床旁诊断提供更加强有力的技术支撑。
参考文献:DOI: 10.1039/d5lc00059a
© 2026. All Rights Reserved. 苏ICP备2022036544号-1












