1. 研究背景:微生物分选需求与微流控技术的行业价值
枯草芽孢杆菌作为革兰氏阳性杆状模式菌,被美国 FDA 认证为普遍安全级(GRAS)微生物,是工业蛋白表达、生物医药合成、功能生物材料制备的核心细胞工厂,也是微生物生理学、代谢调控与基因编辑研究的核心模式生物。在自然培养与工业发酵体系中,枯草芽孢杆菌菌群存在显著的形态异质性,单杆菌、不同长度的链状菌体、团聚体等形态,直接对应菌株的生长周期、基因特性与环境胁迫响应状态,获取长度均一的菌体样本,是基础生物学研究与工业高效发酵的核心前提。
传统的菌体富集与分离技术,如离心淘析、膜过滤等,仅能基于尺寸实现粗分离,依赖昂贵的专用设备,且对微量珍贵样本兼容性差;显微操作法虽能实现精准分选,却存在通量极低、操作繁琐的痛点。而微流控芯片技术凭借低成本、高通量、高精度的核心优势,成为微生物精准分选的突破性技术方向,尤其是细胞分选芯片的技术迭代,为单一菌种的形态学依赖型分选提供了全新解决方案,也推动了 MEMS 加工、微纳加工技术在生命科学领域的深度应用。
2. 技术核心:粘弹性微流控的分选机理与芯片设计制备
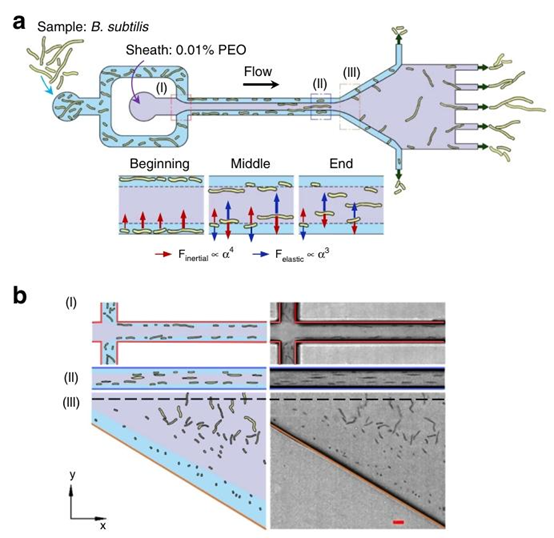
图1 利用粘弹性微流控技术实现枯草芽孢杆菌的无标记连续长度分离。a 粘弹性微流控通道的示意图以及枯草芽孢杆菌细胞按长度分离的原理(未按比例绘制)。该微通道包括两个入口(用于注入细胞悬液和含有聚环氧乙烷的鞘液)、一个直矩形微通道、一个扩张区域和七个出口。b 不同形态的枯草芽孢杆菌细胞在入口、矩形微通道末端和扩张区域的横向位置分布示意图(左)和实验图像(右)的俯视图。比例尺代表10微米。
本研究的核心创新,是基于粘弹性微流控技术,在直矩形微流控通道中实现了枯草芽孢杆菌的无标记、连续式长度依赖型分选,其核心机理是弹惯性效应下的差异化细胞迁移。
在粘弹性流体与牛顿流体的共流体系中,菌体的运动特性由雷诺数 Re、魏森伯格数 Wi、弹性数 El 三个无量纲数主导,菌体同时受到弹性升力与惯性升力的协同作用。其中弹性升力源于流体法向应力差的非均匀分布,与菌体等效粒径的三次方成正比;惯性升力由壁面效应与剪切梯度效应共同产生,与菌体等效粒径的四次方成正比。两种力的尺度效应差异,让不同长度的枯草芽孢杆菌在微流控通道中产生差异化的横向迁移,最终形成长度依赖的平衡位置,实现无标记分选。
本研究中的微流控芯片采用双入口、直矩形分离通道、扩张区与七出口的核心结构,通道截面宽 20μm、高 50μm,设置 10mm、15mm、20mm 三种通道长度进行参数优化。芯片制备依托成熟的 MEMS 加工工艺完成:通过激光直写光刻机在硅基底上制备 SU-8 负性光刻胶模具,再经 PDMS 浇筑工艺完成微流控芯片主体制备 —— 将 PDMS 预聚体与固化剂按 10:1 重量比混合脱泡后,浇筑于 SU-8 模具上,60℃烘箱固化 2 小时以上,脱模后完成进出样口打孔,最终通过 PDMS 等离子键合机与玻璃基底完成不可逆键合,经 95℃热板加固后完成 PDMS 芯片的全流程制备,整个工艺适配标准化的 PDMS 芯片加工设备与微纳加工平台的量产需求。
3. 关键参数调控:微流控芯片分选性能的核心影响因素
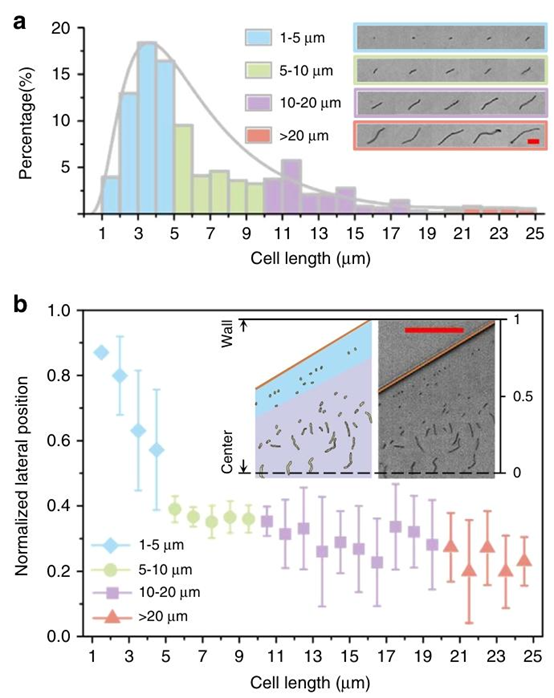
图2 枯草芽孢杆菌细胞的横向位置取决于细胞长度。a 四组枯草芽孢杆菌细胞链长分布的直方图:1–5 μm(蓝色)、5–10 μm(绿色)、10–20 μm(紫色)和\(>20 \mu m\)(粉色)。插图为显示四组不同长度的枯草芽孢杆菌细胞的图像。比例尺代表10 µm。b 四组不同长度的枯草芽孢杆菌细胞的标准化横向位置图。误差线表示至少20次测量获得的标准偏差。插图为扩张区域不同长度的枯草芽孢杆菌细胞标准化横向位置分布的示意图(左)和实验图像(右)。比例尺代表50 µm。
研究系统探究了流速比、PEO 浓度、通道长度三大核心参数对分选效果的影响,明确了粘弹性微流控菌体分选的最优工艺窗口,为微流控芯片设计与应用优化提供了核心依据。
在流速比优化中,研究固定含 100ppm PEO 的鞘流流速为 40μL/min,设置 2-10μL/min 的样品流梯度,对应 20-4 的流速比范围。结果显示,当流速比为 8(样品流 5μL/min)时,不同长度菌体的横向位置差异达到峰值:1-5μm 的短菌体更贴近通道侧壁,而 5μm 以上的长菌体更靠近通道中心,实现了最优的分选区分度。流速比过高或过低,都会因惯性力与弹性力的平衡被打破,导致不同长度菌体的迁移差异缩小,分选效果下降。
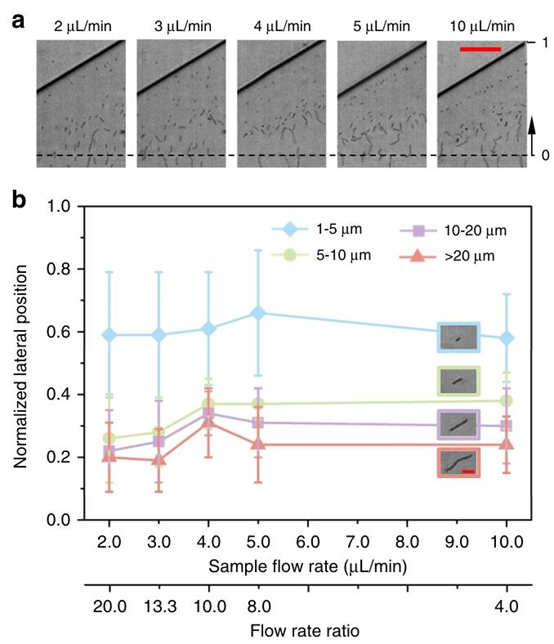
图3 流速比对在15毫米长矩形微通道中使用100 ppm PEO溶液分离枯草芽孢杆菌细胞的影响。鞘流流速固定为40 µL/min,而样品液流速则分别为2、3、4、5和10 µL/min。相应的雷诺数(Re)分别为23.25、23.8、24.35、24.91、27.67,威森伯格数(Wi)分别为8.61、8.82、9.02、9.23、10.25。a 五种不同样品流速下,不同长度的枯草芽孢杆菌细胞在扩张区域的实验图像。黑色虚线代表通道中心线。比例尺为50 µm。b 四组不同长度的枯草芽孢杆菌细胞的平均归一化横向位置图:1–5 μm(蓝色)、5–10 μm(绿色)、10–20 μm(紫色)和\(>20 \mu m\)(粉色)。误差棒表示至少100次测量获得的标准偏差。
PEO 浓度是调控流体粘弹性的核心参数,研究对比了 100ppm、500ppm、1000ppm 三种 PEO 浓度的分选效果。100ppm 浓度下,流体弹性效应与惯性效应达到最优平衡,短菌体被截留于两相界面处,长菌体可穿透界面向通道中心迁移,形成清晰的长度依赖型分布;当浓度升高至 500ppm 以上,界面弹性力成为主导,长菌体向侧壁迁移,不同长度菌体的横向位置重叠度显著提升,分选效果大幅下降。
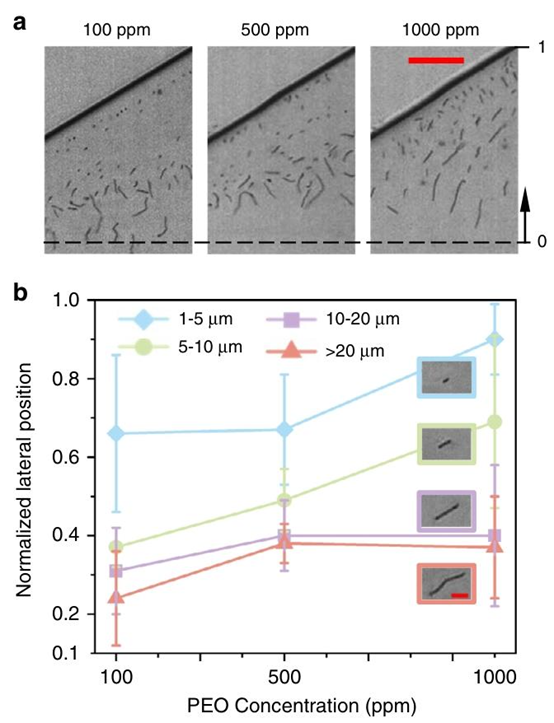
图4 PEO浓度对15 mm长矩形微通道中枯草芽孢杆菌细胞分离的影响,实验采用三种不同浓度的PEO溶液:100、500和1000 ppm。样品和鞘液的流速分别为5 µL/min和40 µL/min。雷诺数(Re)分别为24.91、21.52、18.39,威森伯格数(Wi)分别为9.23、26.25、41.25。a 三种不同PEO浓度下,不同长度的枯草芽孢杆菌细胞在扩张区域的实验图像。黑色虚线代表通道中心线。比例尺为50 µm。b 四组不同长度枯草芽孢杆菌细胞的平均归一化横向位置图:1–5 μm(蓝色)、5–10 μm(绿色)、10–20 μm(紫色)和>20 μm(粉色)。误差线表示至少100次测量得到的标准偏差。
通道长度的优化结果显示,弹惯性效应对菌体的迁移调控具有累积效应,随着通道长度从 10mm 增加至 20mm,所有菌体均向通道中心发生渐进式迁移,不同长度菌体的迁移差异也随之放大。这一结果为微流控芯片长度设计提供了核心依据,可根据分选目标的菌体尺寸差异,灵活调整通道长度,平衡分选效率与芯片加工的工艺难度。
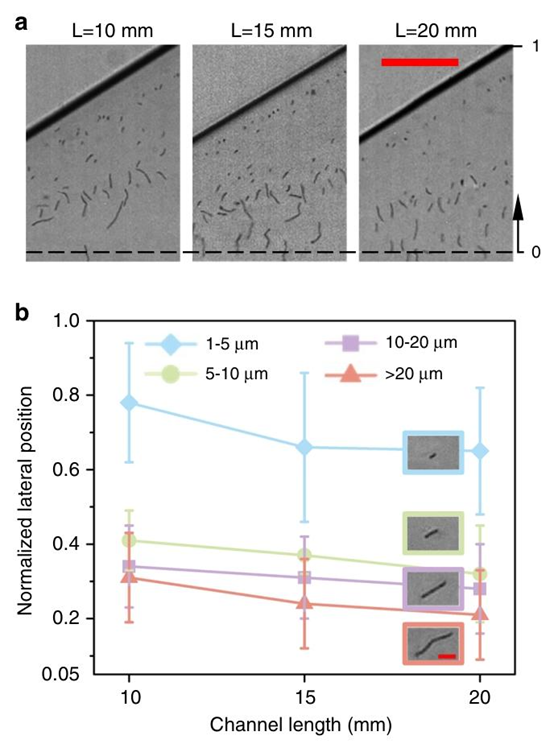
图5 在长度分别为10、15和20 mm的三种矩形微通道中,使用100 ppm的PEO溶液时,通道长度对枯草芽孢杆菌细胞分离的影响。样品和鞘液的流速分别为5 µL/min和40 µL/min。雷诺数(Re)和威森伯格数(Wi)分别为24.91和9.23。a 不同长度的枯草芽孢杆菌细胞在三种不同长度通道的扩张区域的实验图像。黑色虚线代表通道中心线。比例尺代表50 µm。b 四组不同长度枯草芽孢杆菌细胞的平均归一化横向位置图:1–5 μm(蓝色)、5–10 μm(绿色)、10–20 μm(紫色)和>20 μm(粉色)。误差线表示至少100次测量获得的标准偏差。
4. 性能验证与技术的产业化应用前景
基于最优参数组合,研究实现了枯草芽孢杆菌 1-5μm 与 > 5μm 两个菌群的高效分离,核心性能指标达到行业领先水平:1-5μm 的短菌体在侧壁 1 号出口实现了 97.5% 的提取纯度、61.3% 的提取得率;>5μm 的长菌体在中心 4 号出口实现了 100% 的提取纯度、65.2% 的提取得率,富集因子最高可达 6.88,成功实现了菌株稳定期与指数期菌体的精准区分,这也是国际上首次通过粘弹性微流控技术,实现革兰氏阳性菌单一菌种的长度依赖型无标记分选。
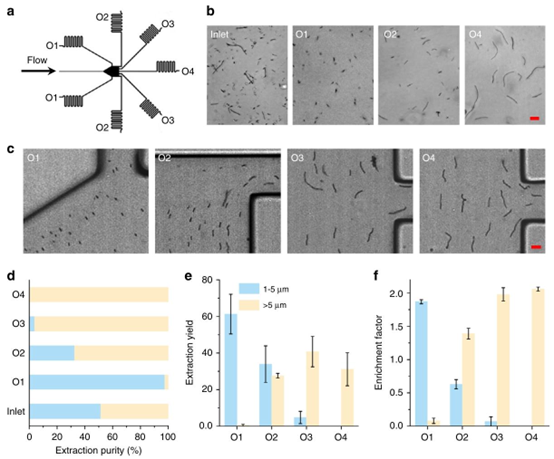
两组枯草芽孢杆菌细胞:入口和每个出口处1–5 μm(蓝色)和>5 μm(黄色)的细胞。e、f为两组细胞的(e)EY和(f)EF柱状图,它们分别更可能从靠近侧壁的出口(O1)和中心线的出口(O4)流出。比例尺代表10 µm。d为不同长度枯草芽孢杆菌的EP对比图c叠加的实验图像显示,不同长度的枯草芽孢杆菌更可能从不同的出口流出:短细胞和长细胞分别从用于收集不同长度枯草芽孢杆菌细胞的出口流出。b对比入口和出口处枯草芽孢杆菌细胞比例的快照图像。矩形微通道。样品液和鞘液的流速分别为5 µL/min和40 µL/min。a图6的示意图:在15 mm长的微通道中使用100 ppm PEO溶液在出口处分离和富集不同长度的枯草芽孢杆菌细胞,显示每个出口处不同长度枯草芽孢杆菌细胞的情况。误差线代表三次测量的标准差。
该技术的应用场景具备极强的拓展性:基础研究层面,分选后的均一性菌体可用于基因组、转录组与蛋白质组学分析,解析微生物形态异质性的分子调控机制;工业应用层面,可用于发酵体系中优势菌体的在线富集,大幅提升工业菌株的发酵效率与产物得率。同时,该分选原理可快速拓展至更多微生物与真核细胞分选场景,为 3D 细胞培养芯片、类器官芯片、器官芯片的样本制备提供核心技术支撑,也为微流控芯片定制、微流控芯片代工行业提供了全新的技术方案,可基于该原理开发定制化的微生物分选芯片、细胞共培养芯片,适配生物医药、环境监测、食品安全检测等多领域的产业化需求。
5. 技术优化方向与微流控行业发展趋势
本研究填补了单一菌种形态学分选的技术空白,也为粘弹性微流控技术的行业应用奠定了实验基础。未来该技术的优化可从多维度推进:芯片结构层面,可通过非对称出口设计、流体电阻优化、级联微通道架构,进一步提升分选通量与纯度;材料层面,除 PDMS 芯片外,可采用 COC 芯片、PMMA 芯片、玻璃芯片等材料,适配芯片规模化注塑量产的需求;加工工艺层面,依托成熟的微纳加工、深硅刻蚀、光刻代工技术,可实现芯片的低成本规模化制备,而桌面式光刻机、紫外光刻机的技术普及,也大幅降低了微流控芯片的研发与定制门槛。
与此同时,该技术可与显微成像、基因测序、在线检测等功能模块集成,开发一体化的微流控检测芯片,推动微流控技术在生命科学基础研究、生物医药产业化中的深度落地,也为微流控芯片加工、MEMS 代工行业带来了全新的市场增量,成为微纳制造技术与生命科学交叉融合的核心发展方向。
参考文献:doi.org/10.1038/s41378-021-00333-3
© 2026. All Rights Reserved. 苏ICP备2022036544号-1












