2025 年 5 月发表于 ChemRxiv 的最新教程综述,系统阐述了超高通量液滴微流控技术在环境微生物菌株及菌群培养、功能筛选中的核心应用,为破解 “未培养微生物组” 难题提供了标准化技术路径。随着微流控芯片加工工艺的成熟,尤其是 PDMS 芯片低成本制备技术的普及,该技术正从实验室走向产业化应用,成为环境生物技术、生物修复与微生物生态学研究的核心工具。
1. 传统微生物筛选的瓶颈与液滴微流控的崛起
微生物多样性是新型生物催化剂、天然产物与环境修复菌株的核心来源,但传统平板培养技术存在显著局限性:仅能分离约 1% 的环境微生物,大量稀有、慢生长或对培养条件敏感的菌株被遗漏,且筛选通量低、试剂消耗大、成本高昂。例如,1 克土壤中可包含 10¹⁰个细菌细胞与 4×10³-5×10⁴个物种,传统方法无法实现对其完整多样性的覆盖。
液滴微流控技术的出现彻底改变了这一格局。该技术将微生物封装于皮升级微液滴中,使每个液滴成为独立的微型生物反应器,支持单克隆或小型菌群的平行培养与分析。依托软光刻技术,科研人员可通过 PDMS 浇筑器、PDMS 热板与 PDMS 烘箱快速制备定制化 PDMS 芯片,大幅降低了微流控设备的研发与使用成本。相较于传统毫升级培养体系,液滴微流控实现了百万倍的体积缩减,单样本筛选通量可达每秒数千个液滴,为环境微生物的大规模筛选提供了可能。
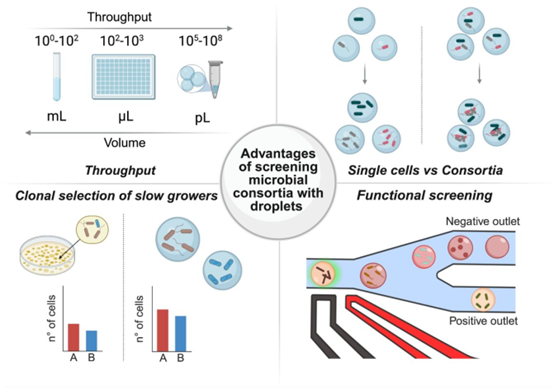
图1. 微生物学中基于微滴筛选的优势。该示意图展示了液滴微流控技术的关键优势,包括慢生长微生物的克隆筛选、功能活性检测、仅需微量样品即可实现的高通量检测,以及对单细胞或整个微生物群落的精准包封。
2. 液滴微流控在微生物筛选中的核心技术优势
1) 极致迷你化与全流程成本控制
PDMS 芯片加工平台的成熟推动了液滴微流控的普及,单块 PDMS 芯片的制备成本仅需数十元,且可实现一次性使用,避免交叉污染。液滴体系将培养基、试剂与样品的消耗降至皮升级别,单轮筛选的试剂成本较传统方法降低 99% 以上。针对高端设备成本较高的问题,被动液滴分选技术应运而生,无需荧光或吸光度检测系统,仅通过液滴的表面张力、变形性或尺寸差异即可实现目标菌株的富集,进一步降低了技术门槛。
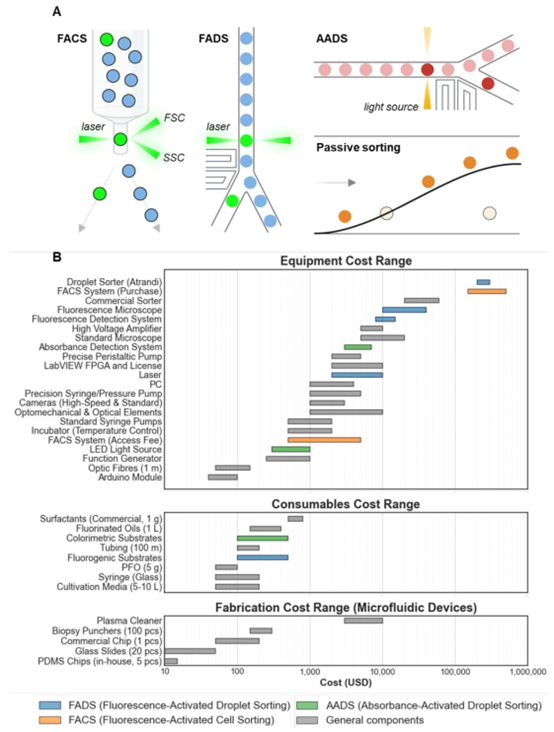
图2. 基于液滴的高通量筛选(HTS)方法概述及相关成本。(A) 常见液滴分选技术的示意图,包括荧光激活细胞分选(FACS)、荧光激活液滴分选(FADS)、吸光度激活液滴分选(AADS)以及被动分选方法。(B) FACS、FADS、AADS和通用型液滴微流控操作在设备、试剂和微流控器件制备方面的成本构成对比,重点标注了关键组件和成本影响因素。
2) 稀有与慢生长微生物的精准分离
传统稀释涂布法易受快速生长菌株的竞争抑制,无法有效分离慢生长菌。液滴微流控通过单细胞封装,彻底消除了种间竞争,使每个菌株在独立空间内生长。研究表明,该技术可从海水、肠道与土壤样本中分离出大量传统方法无法培养的微生物,例如通过图像辅助液滴分选,可将肠道稀有菌群的回收率提升 10 倍以上。同时,该技术支持多物种共培养,可通过 kChip 等可编程平台精准控制菌群组成,研究种间互作与协同代谢。
3) 高通量功能筛选与表型关联
功能筛选是微生物生物技术的核心环节,液滴微流控可实现基于酶活性、抗菌活性、代谢产物合成等表型的高通量筛选。例如,通过荧光激活液滴分选(FADS)与吸光度激活液滴分选(AADS),可每秒筛选数千个液滴,快速定位高活性菌株。该技术已成功应用于纤维素酶、淀粉酶、生物表面活性剂等工业酶的高产菌株筛选,经过多轮诱变与筛选,可使目标酶活提升 2 倍以上。
3. 微生物筛选微流控系统的模块化组成
完整的液滴微流控筛选系统由多个标准化模块组成,各模块可通过 PDMS 芯片键合机与 PDMS 对准平台实现灵活集成,适配不同的实验需求。
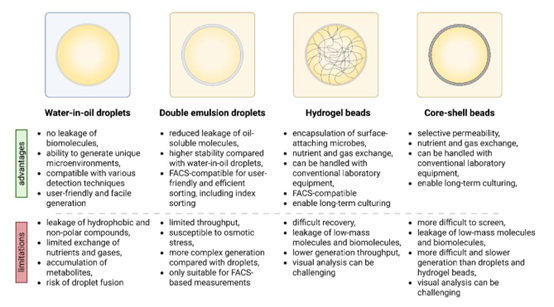
图3. 微滴和胶囊基平台中微生物筛选的分区策略概述。水包油微滴、双乳液微滴、水凝胶微球和核-壳微球的示意图。每种形式在适用性、操作便捷性以及与分选方法(如荧光激活细胞分选/荧光激活液滴分选)的兼容性方面均具有独特的优势和局限性。
液滴生成模块是系统的核心,常用流聚焦、T 型结与共流结构,可生成单分散性良好的微液滴。近年来,粒子模板乳化技术的出现进一步简化了操作,无需复杂的微流控设备,仅通过涡旋即可完成细胞封装。孵育模块支持片上与片外两种模式:片外动态孵育通过循环含氧油相解决了好氧菌的供氧问题,片上微阵列孵育则可实现单个液滴的长时间实时监测。
成像与检测模块依托 PDMS 芯片的高透明性,可结合明场显微镜、荧光显微镜与共聚焦激光扫描显微镜,实时观察微生物的生长状态与形态变化。液滴分选模块分为主动与被动两类:主动分选包括 FADS、AADS 与拉曼光谱分选,适用于高精度功能筛选;被动分选则基于液滴的物理性质,无需标记,操作简便,适合大规模初筛。此外,皮升注射与液滴融合模块可实现多步反应的精准控制,为复杂功能分析提供支持。
4. 标准化实验工作流与应用拓展
开展环境微生物液滴微流控筛选需遵循标准化流程:首先是样品前处理,通过机械分散、酶解与过滤制备单细胞悬液,避免微流道堵塞;其次选择合适的液滴格式,单乳液液滴适用于短期培养与快速筛选,双乳液液滴兼容流式细胞仪分选,水凝胶微球则支持长期培养与营养交换;随后优化培养条件,可采用低营养培养基或模拟原生环境的培养基,提高未培养菌的回收率。
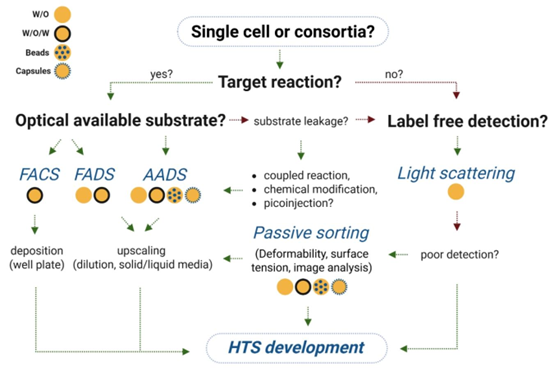
图4. 筛选策略选择。该示意图概述了利用液滴微流控系统开发高通量筛选(HTS)策略的决策流程。从输入的生物形式(单细胞或菌群)和目标反应出发,该决策树会根据底物可用性、泄漏可能性以及检测方法,指导选择合适的液滴形式(如油包水、水包油包水、水凝胶微球或微胶囊)和分析方法。光学检测途径包括荧光激活细胞分选、荧光激活液滴分选和声学激活液滴分选,每种途径对分选及下游处理均有影响。对于非光学底物或信号较弱的情况,可考虑光散射、被动分选等无标记替代方案。
筛选方法的选择需根据目标表型确定:若目标反应有光学底物,可采用 FADS 或 AADS;若无合适标记,则可通过图像分析或被动分选基于生长表型或液滴物理性质进行筛选。筛选获得的阳性液滴可通过微孔板沉积或琼脂平板接种进行放大培养,结合基因组学与代谢组学分析,实现基因型与表型的关联。目前,该技术已拓展至类器官芯片、3D 细胞培养芯片与器官芯片加工领域,为复杂生物体系的研究提供了统一的技术平台。
5. 现存挑战与未来发展方向
尽管液滴微流控技术取得了显著进展,仍面临诸多挑战:复杂环境样品的单细胞悬液制备难度大,易形成细胞团块;检测方法的 multiplexing 能力有限,难以同时分析多个代谢产物;筛选后菌株的放大培养与活性保持仍需优化;高端微流控设备的成本与技术门槛限制了其在中小实验室的普及。
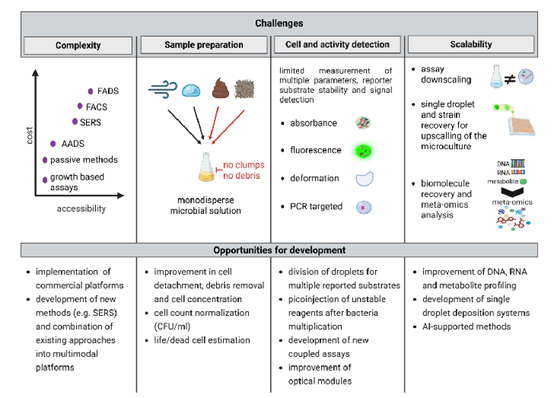
图5. 微生物学研究中微流控系统应用的挑战与机遇。该方案概述了阻碍微流控技术在微生物学领域广泛应用的关键挑战,分为四大类:复杂性、样品制备、细胞与活性检测以及规模化应用。关键挑战包括成本与可及性之间的权衡、样品制备的难点、多重活性检测的局限性,以及生物分子回收、组学整合等规模化应用问题。下方部分则阐述了发展机遇,包括样品处理能力提升、多重检测技术发展、试剂递送优化、联用检测方案,以及分子谱分析和人工智能辅助分析的技术进步。
未来,该技术将朝着三个方向发展:一是与单细胞基因组学、转录组学深度融合,实现功能筛选与组学分析的一体化;二是结合人工智能与深度学习,开发自动化图像分析与实验控制系统,提升筛选效率与准确性;三是推动微流控芯片的标准化与产业化,通过微纳加工平台与 MEMS 加工技术实现芯片的批量生产,降低使用成本。随着技术的不断成熟,液滴微流控将成为下一代微生物生物技术的核心驱动力,为环境治理、生物医药与工业生物制造提供源源不断的创新资源。
参考文献:https://doi.org/10.26434/chemrxiv-2025-mhh5j
© 2026. All Rights Reserved. 苏ICP备2022036544号-1












