1. 微流控芯片领域的发展瓶颈与技术革新背景
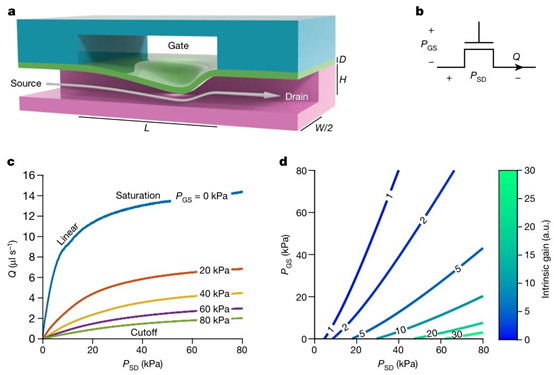
图1 | 类似于电子晶体管,弹性体通道的栅极和源极之间的差异为\(P_{GS}\),压力差表现出压力控制的流量限制。a,源极和漏极之间的纵向截面为\(P_{SC}\)。通过漏极的体积流量为Q。c,实验测量的微流控晶体管特性曲线,其固有增益大于1。a.u.,任意单位。限制。b,微流控晶体管的示意图符号。压力微流控晶体管作为\(P_{G S}\)和\(P_{sD }\)的函数,描绘了一个大区域的微流控晶体管,由两层厚弹性体制成,具有从源极到漏极的非线性流动(箭头),称为流动(线性、截止和饱和)。d,施加在栅极和源极之间的固有增益等高线图使膜偏转,限制通道(品红色、蓝绿色)和薄弹性体膜(绿色)。展示了电子晶体管中常见的所有三种工作状态
微流控技术已成为分子生物学、合成化学、体外诊断、组织工程与器官芯片研发的核心底层技术,基于微流控芯片的 3D 细胞培养芯片、细胞分选芯片、类器官芯片等产品,正在推动生命科学与精准医疗领域的跨越式发展。但长期以来,微流控领域始终面临一个核心痛点:无法以电子电路的精度、模块化与可扩展性实现流体及悬浮颗粒物的自动化操控。尽管气动微阀、MEMS 加工技术的进步推动了微流控芯片的集成化发展,但现有方案大多依赖外部电子控制系统实现流体调控,不仅限制了芯片的规模化集成,还会造成反馈延迟,无法实现真正意义上的芯片级全自主流体控制。
此前学界虽已开展微流控晶体管的相关研究,但均未能复现电子晶体管的饱和特性,也无法实现比例放大这一现代电路设计的核心功能。而发表于《Nature》的这项研究,首次利用流体流动限制现象,开发出具备流体信号比例放大能力的微流控晶体管,实现了电子电路基础拓扑向流体域的完整复刻,为全自主微流控芯片、实验室芯片(Lab-on-a-Chip)的发展奠定了核心技术基础。
2. 微流控晶体管的核心设计原理与标准化制备工艺
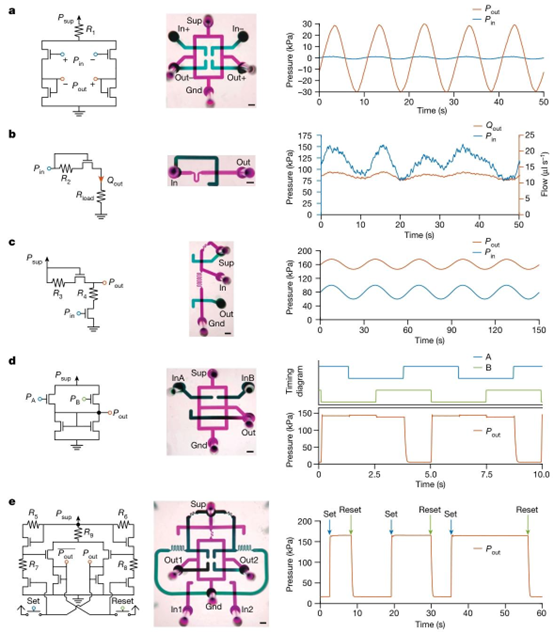
图2 | 基于微流控晶体管的电路可复制关键电子电路的行为。每个电路都提供了原理图(左)、带有标记端口的微流控实现照片(中;伪彩色;比例尺,1毫米)以及电路功能的代表性演示(右)。微流控端口标签的定义和详细说明见方法部分以及扩展数据图7和8。电源端口和接地端口分别标记为“Sup”和“Gnd”。a,流体差分放大器。输入压差信号(蓝色,施加于“In+”和“In–”)经放大倍数22放大后,生成输出差分信号(橙色,在“Out+”和“Out–”处测量)。b,流量调节器。输入压力(蓝色,施加于“In”)在75至150千帕之间变化,经调节后向负载提供目标流量(橙色,在“Out”处测量)\(12 \pm 1.5 \mu s^{-1}\)。c,电平转换器。变化的输入压力信号(蓝色,施加于“In”)的基线向上偏移80千帕,从而产生具有相同形态的输出压力信号(橙色,在“Out”处测量)。d,与非门。只有当两个输入信号(蓝色和绿色,分别施加于“InA”和“InB”)均为高电平时,输出信号(橙色,在“Out”处测量)才为低电平。e,SR锁存器。锁存器的持久状态(橙色,在“Out2”处测量,互补状态在“Out1”处测量)可根据施加到输入端口“In1”或“In2”的瞬时脉冲(用于“置位”(蓝色)或“复位”(绿色))设置为高压或低压。
微流控晶体管的核心创新,在于对可变形边界受限流动中流动限制现象的精准利用。当流体在带可变形边界的微通道中流动时,若压力差超过阈值,流速不会随压力差提升而显著增加,即进入流动限制状态,这一特性与电子场效应晶体管的饱和特性高度契合。
该微流控晶体管采用十字交叉的双层微通道结构,两层通道之间由可变形弹性薄膜分隔,整体采用标准软光刻技术制备,核心材料为 PDMS(聚二甲基硅氧烷),适配主流的 PDMS 芯片制备工艺。器件制备过程中,通过 SU-8 负性光刻胶在硅片上旋涂、曝光、显影完成通道模具制备,再经 PDMS 浇筑、固化形成上下层通道结构,中间层采用 20μm 厚的硅酮薄膜,最终通过氧等离子体键合完成三层结构的组装。整个流程可依托常规的 PDMS 芯片加工设备、光刻机、PDMS 键合机、PDMS 键合对准平台实现标准化量产,也可兼容 MEMS 微纳加工、深硅刻蚀等主流微流控加工工艺,适配玻璃芯片、COC 芯片、PMMA 芯片等多材质微流控芯片的加工需求。
通过对通道几何尺寸、薄膜杨氏模量的精准调控,研究团队使器件的 Shapiro 数大于 1,稳定进入流动限制状态,复现了电子晶体管的截止区、线性区与饱和区三大工作区间。测试结果显示,该微流控晶体管存在大范围的工作区间,其固有增益远大于 1,具备稳定的流体信号比例放大能力,核心性能完全对标电子 p 沟道结型场效应晶体管。
3. 模块化电路拓扑复刻,实现全流体域信号处理
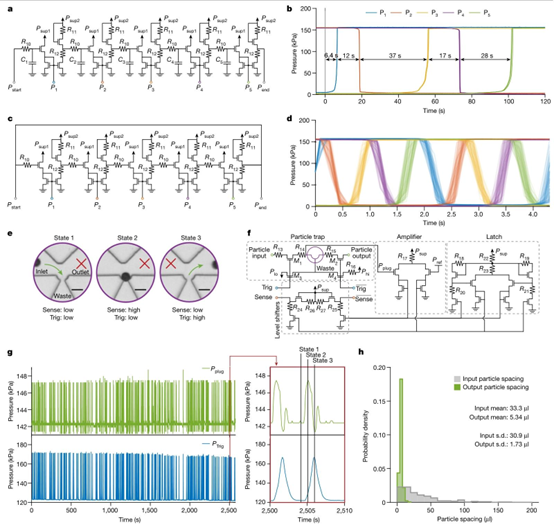
图3 | 微流控晶体管实现了时序操作和智能分配器电路,用于自主单粒子操控。a,时序延迟计时器的电路示意图,包含多个级联的低通滤波器、放大器和电平转换器。b,在时间\(t=0\)施加到\(P_{start }\)的阶跃信号通过电路模块传播,产生可控的时间间隔以触发连续的流体事件。选择电容值是为了按不同间隔依次触发五个流体事件。该电路三次试验的触发压力信号叠加,并标注了平均间隔持续时间。c,包含五个放大器和五个电平转换器的环形振荡器的电路示意图。d,环形振荡器在每个反相器的输出端自发产生方波,相位相差五分之一周期。对振荡器信号进行了数分钟的测量,每个信号的63个单位间隔叠加后绘制在眼图中。e,智能分配器操作概述,描绘了核心微流控陷阱在感应和分配单个粒子时的不同状态(比例尺,50μm)。f,智能分配器的电路示意图,包含多个电路模块和微流控陷阱(紫色)。g,使用智能分配器实现确定性单粒子排序和浓缩。该分配器配置中,触发线(Trig)和感应线(Sense)直接连接,因此单个粒子被感应后立即分配到输出通道。显示了陷阱本身(\((P_{plug })\))和触发器(\((P_{Trig })\))在\(n=230\)个粒子运行过程中的压力信号,以及一个代表性的分配事件以观察个体动态(红色插图)。h,在此配置下使用智能分配器时输入和输出粒子间距的直方图,显示间距平均值下降了6倍(表明粒子浓缩),间距标准偏差下降了17倍(表明粒子排序)。
基于微流控晶体管的核心特性,研究团队完成了电子电路三大基础拓扑(共源、共栅、共漏)向微流控领域的 1:1 转化,构建了覆盖模拟与数字信号处理的全系列基础电路模块,无需任何外部电子、光学或气动控制器,即可在芯片内完成流体信号的全流程处理。
在模拟电路领域,团队基于共源拓扑构建了流体差分放大器,实现了 22 倍的信号增益,可对单细胞、微颗粒产生的微弱压力信号进行高灵敏度放大;基于共栅拓扑开发了流量调节器,可在 75~150kPa 的输入压力波动下,为下游负载提供 12±1.5μL/s 的稳定流量,适配资源受限场景下的微流控设备运行;基于共漏拓扑设计了电平转换器,可在不改变信号形态的前提下完成 80kPa 的信号基线平移,实现了多电路模块的级联与模块化设计,大幅提升了微流控芯片设计的灵活性。
在数字电路领域,团队实现了通用 NAND 逻辑门与 SR 锁存器的流体域构建。NAND 门作为通用逻辑门,可组合实现所有布尔逻辑运算,为微流控芯片的数字信号处理、流体事件同步提供了基础;SR 锁存器则实现了双稳态输出与流体信号记忆功能,可用于流体事件计数、时序逻辑运算,为微流控芯片的存储功能提供了核心单元。基于这些基础模块,研究团队进一步完成了时序延迟定时器、环形振荡器(流体时钟)等复杂时序电路的级联构建,可精准控制多步化学合成、细胞培养等时序流体操作,为多器官芯片、分步药物筛选芯片的全自主运行提供了时序控制核心。
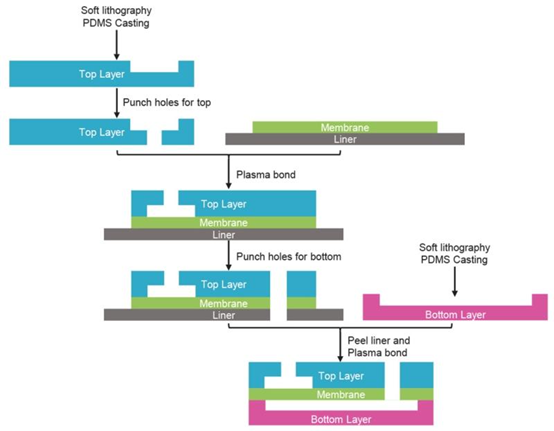
然后,该层在氧等离子体下与一层薄硅树脂膜结合。扩展数据图6 | 多层微流控晶体管的组装——然后将底层的端口冲压到顶层-基于膜的电路中。软光刻技术用于制造顶层和组件。该组件通过手工对齐,最终在氧等离子体下与底部的聚二甲基硅氧烷层结合。顶层端口被冲压到顶层聚二甲基硅氧烷层中。
4. 单细胞 / 单颗粒自主操控,生命科学与诊断场景落地
这项研究的突破性应用价值,在于实现了微流控芯片对悬浮颗粒、单细胞的全自主检测与操控,完成了电子晶体管无法实现的 “信号感知 – 处理 – 物理操控” 全流程流体域闭环。
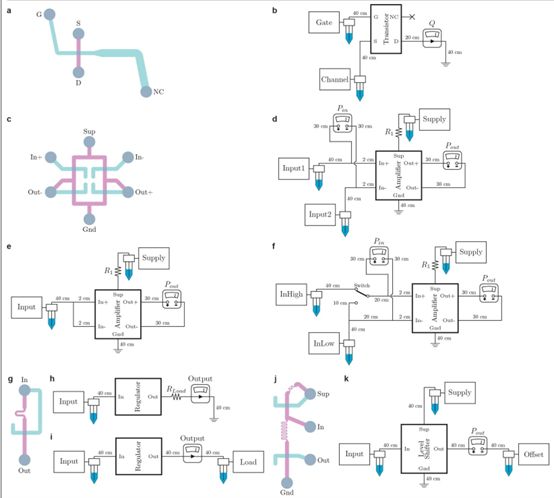
放大器频率响应(波特图)测量的设置。g,引脚分布 扩展数据图7 | 单晶体管、放大器、流量调节器和电平转换器测量的设置。相关组件详情(如几何形状和电阻值)见扩展数据表1。a,单晶体管芯片的引脚分布图(NC:无连接),其中冲孔端口为灰色,通道层为品红色和蓝绿色。b,用于单晶体管特性曲线和跨导曲线测量的流体设置。e,用于放大器共模抑制测量的流体设置。f,流量调节器芯片的流体图,其中冲孔端口为灰色,通道层为品红色和蓝绿色。h,用于调节器演示和线路调节测量的流体设置。i,用于负载调节测量的流体设置。j,电平转换器芯片的引脚分布图,其中冲孔端口为灰色,通道层为品红色和蓝绿色。交叉端接链路表示无连接。c,放大器的引脚分布图,其中冲孔端口为灰色,通道层为品红色和蓝绿色。k,用于电平转换器演示、偏移量和增益测量的流体设置。d,用于放大器演示和失真测量的流体设置。
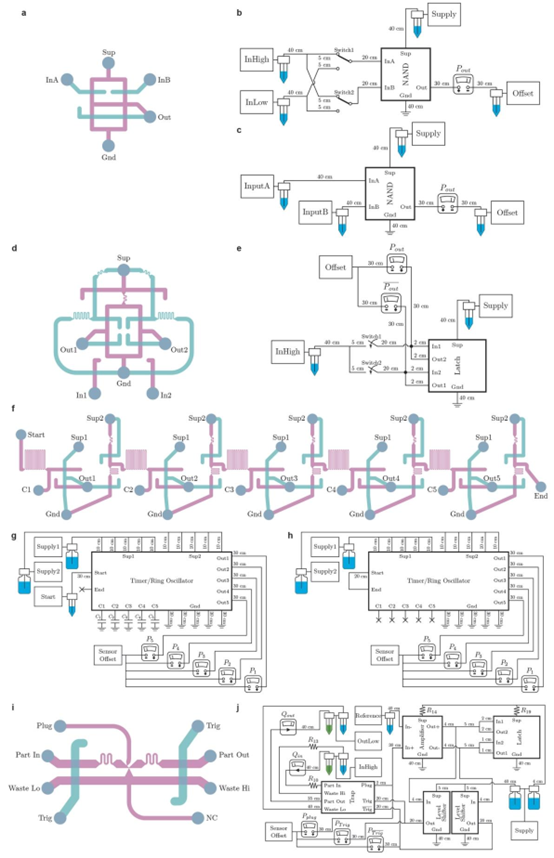
研究团队基于微流控晶体管电路,构建了智能颗粒分配器,核心由微流控颗粒捕获阱、信号放大电路、锁存器与电平转换器组成。当微颗粒进入捕获阱时,上游微弱的压力变化被放大电路识别,生成高电平传感信号,再经触发信号控制完成颗粒的定向释放,整个过程无需任何外部电子设备干预。通过将传感与触发信号形成反馈环路,该分配器实现了颗粒的确定性排序与富集,使颗粒间距均值下降 6 倍,间距标准差下降 17 倍,可直接应用于单细胞分选、单细胞测序、单颗粒药物包裹等场景。
该技术为类器官芯片、3D 细胞培养芯片、血脑屏障芯片等产品提供了全新的控制方案,可在芯片内完成细胞捕获、培养、给药、检测的全流程自动化操作,无需依赖复杂的外部控制系统,大幅降低了器官芯片的使用门槛,推动了器官芯片在药物筛选、个性化医疗领域的产业化落地。同时,该技术也可适配微流控 PCR 芯片、免疫诊断芯片、POCT 微流控芯片等体外诊断产品,实现检测流程的全芯片自动化,推动即时检测设备的微型化与便携化发展。
5. 行业价值与未来发展前景
这款微流控晶体管的问世,填补了微流控领域长期以来缺乏核心放大元件的空白,将电子电路领域百年积累的设计体系完整引入微流控领域,彻底改变了微流控芯片依赖外部控制的传统架构。
从产业化角度来看,该技术完全兼容现有的 PDMS 芯片加工、MEMS 微纳加工、软光刻等主流工艺,可依托现有的微纳加工平台、微流控芯片代工体系实现快速产业化转化,无需全新的产线投入。同时,模块化的设计逻辑大幅降低了微流控芯片定制的开发难度,可根据应用需求快速组合基础电路模块,开发出适配不同场景的全自主微流控芯片,无论是实验室级别的微流控芯片研发,还是工业化的微流控产品量产,都具备极强的适配性。
未来,随着微流控晶体管在响应速度、集成度上的持续优化,该技术将推动全自主实验室芯片的快速发展,在单细胞分析、合成生物学、精准医疗、环境检测等领域实现更广泛的应用,为微流控技术的真正规模化、普及化应用奠定核心技术基础。
参考文献:https://doi.org/10.1038/s41586-023-06517-3
© 2026. All Rights Reserved. 苏ICP备2022036544号-1












