参考文献:DOI 10.3389/fbioe.2022.968342
细胞作为生命活动的基本单元,其内在动态过程具有极强的随机性与异质性,即便是基因序列完全一致的细胞,在相同环境下也会表现出差异化的基因表达与行为表型。传统的群体水平检测手段会掩盖单细胞的动态特征,而琼脂糖垫延时成像仅能支持数代细胞的观察,单细胞测序技术也只能获取静态的分子快照,无法追踪细胞谱系的长时程动态变化。微流控芯片技术的出现,为长时程单细胞活体成像提供了突破性解决方案,其中被称作 “Mother Machine(母机)” 的微流控装置,更是成为原核单细胞动态研究的核心平台,推动了微生物学、合成生物学、细胞衰老等多个领域的重大发现。
1. Mother Machine 微流控芯片的核心设计与标准化制备工艺
Mother Machine 的核心设计逻辑,是通过微米级的功能结构实现单细胞的长时程捕获与谱系追踪。其经典结构由主进料通道与数十组垂直分布的单细胞宽度死端沟槽组成,沟槽尺寸与目标微生物的菌体大小精准匹配,以大肠杆菌为例,沟槽通常设计为 1.2μm 高度、1.3μm 宽度与 20μm 长度,既能保证菌体以单细胞队列排布,又能通过扩散实现营养物质的稳定供给。主进料通道内的恒定培养基流动,会持续将分裂产生的子代细胞冲出沟槽,仅保留位于沟槽末端的 “母细胞”,从而实现对单一细胞谱系数百代的连续追踪。
PDMS 芯片制备是该装置落地应用的核心环节,完整的制备流程覆盖了从模具制作到芯片封装的全链条工艺。首先通过 CAD 软件完成芯片结构设计与掩膜版制作,在洁净室环境中通过光刻技术在硅晶圆上构建模具,常规的 SU8 模具可通过紫外光刻机、桌面式光刻机完成加工,而亚微米级的精细结构则需借助电子束光刻技术实现。模具制备完成后,通过 PDMS 浇筑与固化完成芯片主体的复刻,这一过程可通过 PDMS 热板、PDMS 烘箱实现精准的温控固化,配套 PDMS 浇筑器可大幅提升芯片制备的均一性。固化后的 PDMS 芯片经 PDMS 打孔器完成进出料孔的加工后,通过 PDMS 等离子键合机实现与盖玻片的不可逆封接,完成微流控芯片的核心制备;针对不同应用场景,也可采用阳极键合工艺完成硅 – 玻璃芯片的封装,或适配 COC 芯片、PMMA 芯片等其他基材的微流控芯片加工。
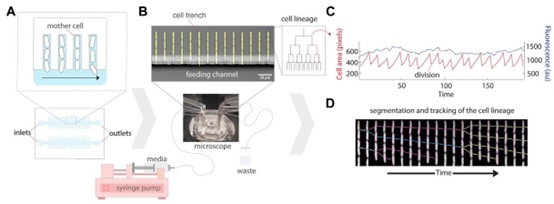
图1 母机微流控装置实验设置及数据分析示意图。(A)该平台的示意图,其将单个细菌细胞捕获在与较大进料通道垂直的沟槽中。子细胞随流动培养基冲出沟槽,而母细胞则留在细胞沟槽末端。(B)母机的显微照片,在精确控制的环境条件下,使用延时显微镜对YFP进行追踪。(D)生长中细胞的荧光成像示例时序图,显示细胞叠加在装置的明场图像上。培养基通过注射泵从入口泵入主进料通道,然后从出口流入废液烧杯。(C)沟槽中生长细胞的谱系可发出荧光,展示了谱系的分割和追踪。
2. Mother Machine 平台的技术升级与多场景功能拓展
自经典设计问世以来,Mother Machine 平台围绕实验痛点完成了多维度的技术革新,大幅拓展了其应用边界,也推动了微流控芯片加工技术的持续迭代。
在图像分析层面,针对传统分析方法依赖荧光标记、通量低的问题,多款开源软件实现了基于相衬图像的自动化细胞分割与谱系追踪,其中基于深度学习的 DeLTA、DistNET 等算法,可将分割与追踪的综合误差率控制在 1% 以内,彻底摆脱了对外源荧光蛋白的依赖,大幅提升了实验的设计灵活性。
在流体与环境调控层面,经典的单进料结构升级为双输入母机(DIMM),通过蛇形混合通道实现了低雷诺数环境下的培养基快速切换与精准混合,可模拟复杂的环境波动;配套的批次培养模拟系统,通过蠕动泵与气泡陷阱实现了摇瓶培养环境的芯片内复刻,填补了静态恒流培养与自然生长环境之间的空白。
在单细胞筛选层面,平台升级实现了动态表型与基因型的关联分析:DuMPLING 技术通过沟槽末端的微纳间隙与后端通道,实现了固定细胞的原位 FISH 基因分型;SIFT 技术则通过集成微阀与光镊系统,完成了活细胞的表型筛选、分离与下游测序,突破了传统微流控芯片无法实现动态表型筛选的瓶颈。
在物种适配层面,通过沟槽尺寸与结构的优化,该平台从大肠杆菌拓展至枯草芽孢杆菌、谷氨酸棒杆菌等多种微生物,通过尺寸放大与结构改良,更是实现了古菌、裂殖酵母、出芽酵母的长时程培养,相关设计逻辑也被广泛应用于 3D 细胞培养芯片、细胞共培养芯片、类器官芯片与器官芯片的开发中,成为微流控细胞培养芯片的核心设计范式之一。
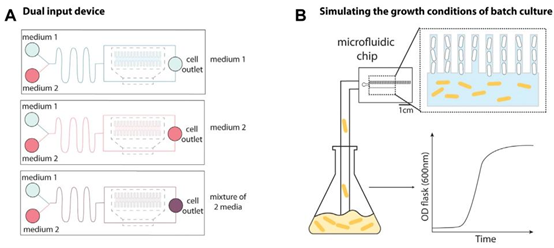
要将培养物注入装置中,以重现分批培养条件。这使得观察细胞在不同环境条件之间进入和退出静止期成为可能。示意图灵感来源于Kaiser等人(2018年)。(B)生长曲线平台支持分批培养,设有两个培养基入口,之后是一条蛇形通道,流体在到达细胞槽之前会流经该通道,以促进混合和/或快速切换。为改善流体和环境控制而对母机结构进行的改造。(A)双输入母机(DIMM)通过在营养耗尽的培养物和新鲜培养基之间切换,实现了静止期的转换。示意图灵感来源于Bakshi等人(2021年)。
3. Mother Machine 平台在生命科学领域的突破性应用
Mother Machine 平台的技术特性,使其成为破解单细胞异质性相关科学问题的核心工具,在多个生命科学领域实现了颠覆性发现。
在细胞尺寸调控研究中,该平台通过数百代细胞的连续追踪,证实了大肠杆菌、枯草芽孢杆菌主要通过 “加法器” 机制实现尺寸稳态,即细胞在分裂前会增加恒定的长度,而非达到固定尺寸或生长固定时间,进一步揭示了 DNA 复制与细胞分裂的双加法器调控模型,颠覆了传统的细胞周期调控认知。
在基因突变与进化研究中,平台无生长竞争的特性,实现了对基因突变这一稀有事件的精准捕捉,直接观测到了 DNA 复制错误的发生过程,修正了基因突变平均适应度代价的传统认知,同时揭示了 DNA 损伤响应的随机脉冲特性是导致细胞间突变率差异的核心原因。
在细胞衰老研究中,该平台首次实现了对称分裂细菌的老极谱系连续追踪,证实了即便是二等分裂的大肠杆菌,也会因损伤分子的不对称分配出现衰老表型,明确了老极细胞的生长速率变化与死亡规律,为单细胞衰老的普适性机制研究提供了核心数据支撑。
此外,该平台还在细菌抗生素持留态机制、基因表达随机脉冲调控、芽孢杆菌细胞命运决定、合成生物学基因回路优化等领域实现了重大突破,例如基于该平台完成了经典合成振荡器 “阻遏振荡器” 的重构,使其振荡精度达到了天然生物振荡器的水平。
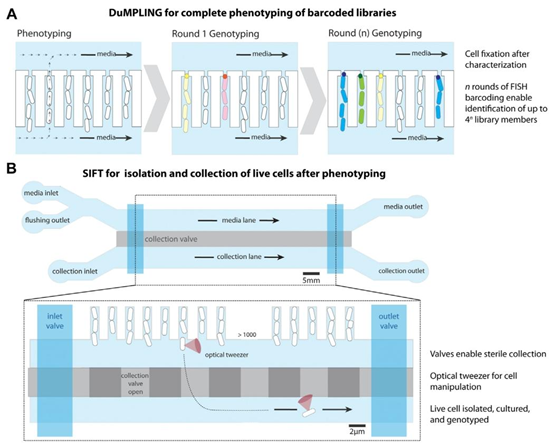
图3 为实现细胞筛选而对母机进行的改造。(A)基于动态微流控显微镜的库原位基因分型前表型分析(DuMPLING)在细胞槽末端有一个300纳米的间隙,允许培养基流过细胞通道。通过荧光原位杂交(FISH)进行的多轮条形码标记可实现混合库的基因分型。示意图改编自Lawson等人(2017年)。(B)延时显微镜后的单细胞分离(SIFT)使用改良的微流控芯片,该芯片在细胞槽下方包含一个额外的细胞分离通道,由加压阀系统(收集阀)分隔。第二组阀门(入口阀和出口阀)可密封该通道,用于入口清洁,并在细胞加载后限制培养基流动。光镊将目标细胞从其槽中移至收集阱,在那里细胞被分离并从装置中取出,进行培养和测序。示意图改编自Luro等人(2020年)。
4. 行业发展总结与未来展望
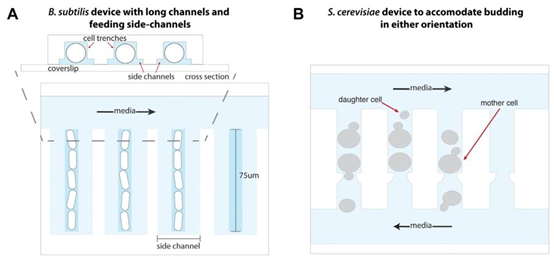
垂直介质通道。示意图灵感来源于Li等人(2017年)。改进型MM装置中每个细胞沟槽能够将出芽产生的酿酒酵母子细胞从任一方向移除,使其进入沟槽各处的营养可利用区域。示意图灵感来源于Norman等人(2013年)。(B)在两端保持开口,生长环境包括长度为75微米的细长沟槽,以适应其多细胞链状状态,以及能够实现均匀性的侧通道。对母机结构的改造是为了优化其他生物体的生长。(A)为枯草芽孢杆菌改造的母机设计 图4
Mother Machine 微流控平台的发展,是微流控技术与单细胞生物学深度融合的缩影,其从单一结构的装置,逐步发展为集环境精准调控、自动化成像分析、单细胞筛选分离于一体的综合性平台,背后离不开 MEMS 加工、微纳加工技术的持续进步,也离不开微流控芯片定制、MEMS 代工产业的成熟支撑。
未来,该平台的发展将呈现两大核心方向:一是应用场景的持续拓展,从原核微生物向哺乳动物细胞延伸,在肿瘤细胞耐药性、造血干细胞分化、类器官培养等领域发挥价值,推动器官芯片技术从结构模拟向功能复刻升级;二是技术体系的持续完善,通过与 AI 深度学习、微纳传感、光遗传学技术的结合,实现单细胞动态过程的实时监测与精准干预,同时微流控芯片量产技术的发展,也将推动该平台从实验室走向更广泛的临床与工业应用场景,为生命科学的底层机制研究与生物技术的产业化落地持续赋能。
© 2026. All Rights Reserved. 苏ICP备2022036544号-1













