1. 多孔生物医用微粒的研发背景与技术痛点
多孔微粒凭借大比表面积、高负载能力与层级化微观结构,已在诊疗诊断、可控药物递送、无创诊断、组织工程等生物医学领域实现了广泛应用,同时也是 3D 细胞培养、类器官芯片构建的核心载体材料。当前行业内多孔微粒的主流制备方案以模板引导法与乳液基技术为主,但两种工艺均存在难以突破的技术瓶颈。
模板引导法需通过煅烧或化学蚀刻去除模板,不仅流程繁琐耗时,残留的有毒蚀刻剂还会破坏材料结构与包埋的活性物质,限制了其在生物医用场景的应用;乳液基技术虽无需模板去除步骤,却依赖设计精密的制备设备,操作门槛高,且制备过程中有机溶剂的扩散会影响最终微粒的生物相容性,难以适配器官芯片、细胞培养微流控芯片等对材料生物安全性要求极高的场景。
在此背景下,开发高效、易操作、高生物安全性的多孔微粒制备技术,成为生物医用材料与微流控领域的核心研发方向。而微流控技术作为微纳加工领域的核心技术,凭借其对微尺度流体的精准操控能力,在单分散性微粒制备中展现出独特优势,基于液滴微流控技术的功能化微粒制备方案,也成为行业内的研究热点。
2. 基于微流控电喷雾技术的多孔微粒制备体系构建
本研究创新性地将气泡驱动纳米马达引入液滴微流控体系,通过微流控电喷雾技术实现了多孔生物医用微粒的连续化、一步法制备,整个制备过程具备高度可控性,最终产物也展现出优异的孔隙率与单分散性。
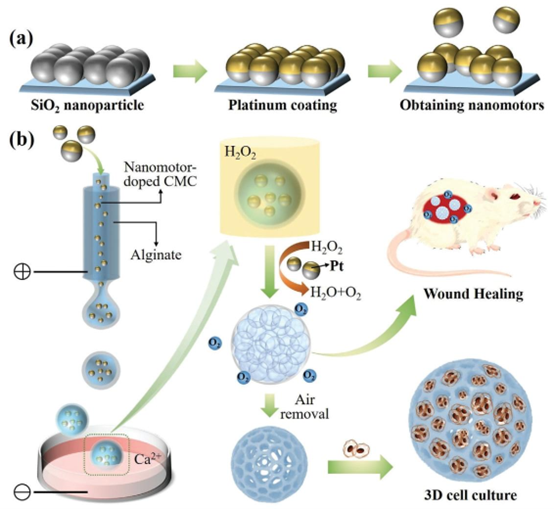
图1. 示意图:a) PSNs的生成过程;b) 多孔微颗粒的生成过程及其应用。
研究首先完成了气泡驱动纳米马达的制备,以二氧化硅纳米颗粒为基底,通过气液界面自组装在玻片表面形成有序六方堆积的单层结构,再通过磁控溅射镀膜工艺在纳米颗粒表面沉积铂层,最终经超声处理得到离散的铂包被二氧化硅纳米颗粒(PSNs)。该纳米马达可在过氧化氢溶液中持续催化产生氧气气泡,为多孔结构的构建提供了核心动力,其制备过程涉及的镀膜、微纳加工工艺,均可通过成熟的 MEMS 加工体系与微纳加工平台实现标准化落地。
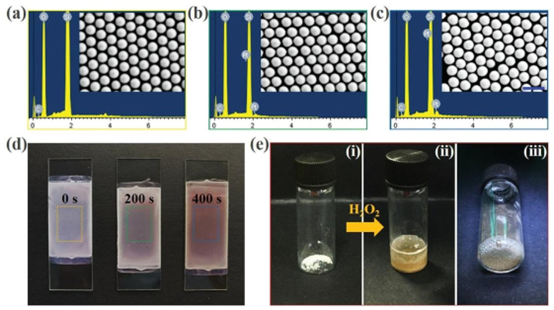
图2. 气泡驱动纳米马达的制备:a) 未修饰SN单层的SEM图像(插图)及相应的元素分析,b) 铂溅射200秒后的SN单层,c) 铂溅射400秒后的SN单层;d) 从左到右分别为铂溅射0秒、200秒和400秒后SN单层的结构色;e) PSN与\(H_{2} O_{2}\)溶液接触后的性能。比例尺为500纳米。
在微流控芯片系统的设计上,研究采用同轴组装的双圆柱毛细管构建微流控电喷雾装置,内相为分散了 PSNs 的羧甲基纤维素钠溶液,外相为海藻酸钠溶液,通过流体动力学聚焦效应与外加电场作用,连续生成核壳结构的双乳液液滴。液滴外壳的海藻酸钠可与收集液中的氯化钙快速凝胶固化,维持微囊形态,而液滴粒径可通过电场电压、收集距离、内外相流速精准调控,最终制备的微囊尺寸变异系数低于 5%,具备极佳的单分散性。该微流控芯片系统的设计逻辑,可直接适配 PDMS 芯片加工、微流控芯片定制的标准化流程,也可与 PDMS 芯片加工设备、器官芯片加工平台实现工艺兼容。

图3. 核壳结构微胶囊和多孔微颗粒的生成:a) 微流控电喷雾装置在微胶囊生成过程中喷口的实时图像;b) 具有固化壳层和未固化内核的微胶囊;c) 含有大量氧气气泡的多孔微颗粒;d) 不含气泡或含少量气泡的多孔微颗粒;e、f) 分别为微胶囊直径与电场电压和收集距离的关系。比例尺为500 μm。
多孔结构的成型则依赖纳米马达的催化反应:过氧化氢扩散进入未固化的内核后,PSNs 持续催化产生氧气气泡并填充整个微囊,经氯化铝溶液固化内核后,通过真空处理或静置排出气泡,最终形成内外连通的多孔结构。扫描电镜表征显示,制备的微粒表面带有连通外界的窗口,内部大孔之间存在大量互连的小孔,这种层级化多孔结构为物质交换与营养运输提供了通道,完美适配生物医用场景的核心需求。
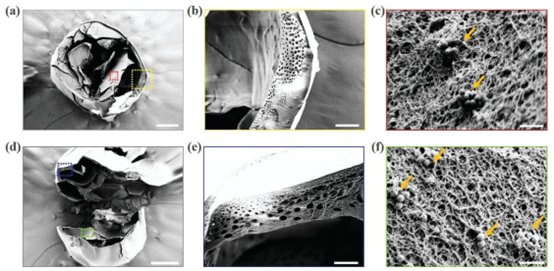
图4. 多孔微颗粒的微观结构:a) 扫描电镜观察下多孔微颗粒的整体视图;b) (d)中蓝色框的放大视图;f) (d)中绿色框的放大视图,多孔微颗粒中残留的PSN(由橙色箭头标记);(a)中的黄色框;c) (a)中红色框的放大视图以及多孔微颗粒中残留的PSN(由橙色箭头标记);比例尺:(a, d)为200 μm,(b)为100 μm,(c, f)为1 μm,(e)为50 μm;d) 所得多孔微颗粒的内部微观结构;e) 孔结构骨架的微观结构(的放大视图)
3. 多孔微粒的核心生物医学应用验证
1) 3D 细胞培养微载体应用
研究验证了该多孔微粒作为 3D 细胞培养微载体的可行性,以 3T3 成纤维细胞为模型,证实细胞可通过表面孔隙进入微粒内部,在培养 7 天后形成稳定的细胞聚集体。与实心海藻酸钠微粒相比,多孔微粒中的细胞展现出更优异的活性与增殖能力,这一特性使其成为 3D 细胞培养芯片、细胞共培养芯片的理想载体,也为类器官培养、组织工程支架构建提供了新的材料方案,可广泛应用于细胞治疗、器官芯片模型构建等领域。
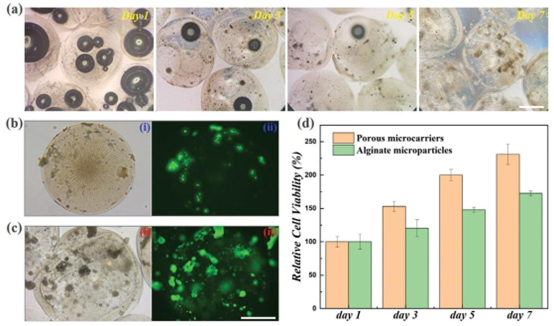
图5. 用于3D细胞培养的多孔微颗粒:a) 多孔微颗粒中细胞在培养1、3、5和7天后的状态;b) 固体海藻酸盐-羧甲基纤维素(CMC)微颗粒和c) 多孔微颗粒与3T3细胞共培养7天后的透射光学显微镜图像(i)和荧光图像(ii);d) 固体海藻酸盐-羧甲基纤维素微颗粒和多孔微颗粒与3T3细胞共培养后的MTT测定结果。比例尺为500 μm。
2) 糖尿病创面修复应用
针对 I 型糖尿病创面难愈合的核心痛点 —— 创面局部缺氧,研究进一步验证了载氧多孔微粒的促创面愈合效果。在 I 型糖尿病大鼠全层皮肤缺损模型中,载氧多孔微粒处理组的创面在 15 天内几乎完全愈合,愈合效果显著优于空白对照组与无载氧实心微粒组。组织学分析证实,载氧微粒组的再生上皮厚度更优,胶原沉积更有序,创面床血管密度更高,炎症因子 IL-6 表达水平更低,证实该材料可通过持续供氧、维持创面湿润、抑制炎症反应,高效促进糖尿病创面愈合,在创伤修复生物医用材料领域具备极高的转化价值。
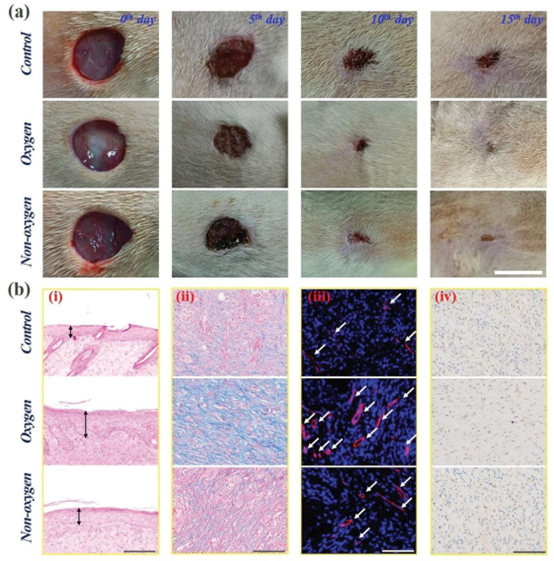
图6. 含氧化合物多孔微粒促进伤口愈合能力的研究:a) 对照组、氧气组和非氧气组在伤口愈合过程中伤口面积的变化。比例尺为1厘米;b) 组织学分析:(i) 苏木精-伊红(H&E)染色分析结果;(ii) 马松(Masson)染色分析结果;(iii) CD31与α-平滑肌肌动蛋白的双重免疫荧光染色结果(\(( \alpha-SMA)\));(iv) 白细胞介素-6(IL-6)的免疫组织化学染色结果。(i)中的比例尺为200微米,(ii, iii, iv)中的比例尺为100微米。
4. 研究的技术突破与行业应用前景
本研究的核心突破,在于首次将气泡驱动纳米马达与液滴微流控技术结合,建立了一种无有毒试剂、流程简单、可控性强的多孔生物医用微粒制备方法,解决了传统工艺的核心痛点。该技术体系与现有的微流控芯片加工、PDMS 芯片制备、MEMS 微纳加工工艺完全兼容,可快速实现从实验室研发到产业化的落地,适配微流控芯片工厂的规模化生产需求。
从行业应用来看,该研究制备的多孔微粒不仅可作为 3D 细胞培养、类器官芯片的核心载体,还可拓展至药物递送、生物检测、组织工程、器官芯片加工等多个领域,为微流控生物芯片的功能化升级提供了全新的技术路径。同时,其在糖尿病创面修复中的优异表现,也为慢性创面治疗提供了新的材料方案,在临床转化领域具备广阔的想象空间,将持续推动微流控技术与生物医用材料行业的深度融合与创新发展。
参考文献:DOI: 10.1002/advs.202104272
站内搜索
© 2026. All Rights Reserved. 苏ICP备2022036544号-1













