1. 引言:血小板生成研究的临床需求与技术革新
血小板作为止血、血栓形成及免疫调节的核心血细胞,其体外高效制备一直是临床输血与基础医学研究的关键瓶颈。传统观点认为骨髓是血小板生成的主要场所,但近年来研究证实,肺血管系统同样是血小板生物合成的重要阵地。随着微流控芯片、PDMS 芯片制备、MEMS 加工等技术的快速发展,体外复刻生理微环境、解析血小板生成机制成为可能。本文基于《Nature Communications》发表的肺血管血小板生成研究,结合微流控技术、器官芯片、细胞培养芯片等前沿工具,系统解读血小板生成的核心机制与体外制备的技术突破,为临床血小板替代疗法提供新思路。
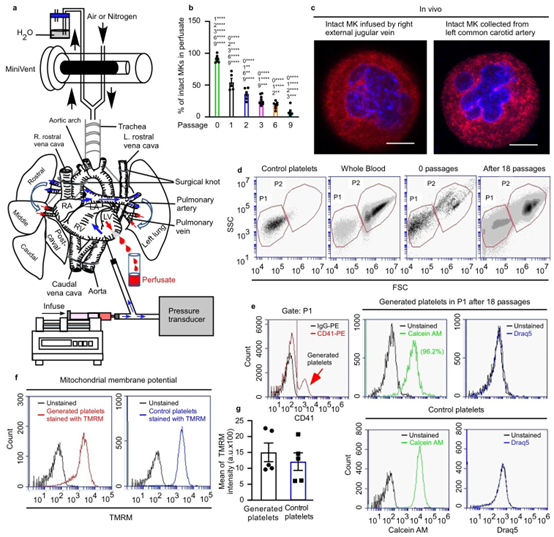
图1 | 小鼠血小板是由巨核细胞在体外多次通过小鼠肺血管系统产生的。用CD41-PE或CD41-FITC抗体标记的小鼠巨核细胞(MKs)在体外反复通过肺血管系统。整个过程中肺都用空气通气(b、d-g)。a 说明小鼠血小板生成方法的示意图。应用呼气末正压以防止肺塌陷。b 巨核细胞通过肺血管系统指定次数后,灌流液中的完整巨核细胞。定量分析来自≥250个视野,总共计数≥230个细胞,并以细胞总数的百分比显示。每列上方的数字表示与其他传代次数的显著差异。对于传代次数0、1、2、3、6和9,分别进行了8次和6次独立实验。误差线为平均值±标准误。采用双向方差分析和Tukey多重比较检验,\(^{*} p<0.05\)、\(^{*} p<0.01\)、\(^{* *} p<0.001\)和\(^{*+++} p<0.0001\)。c 体内实验证明完整的小鼠巨核细胞通过肺血管系统。将小鼠巨核细胞用CellTracker™Red CMTPX染料(红色)和Hoechst 33342(蓝色)染色后,注射到麻醉的C57BL/6受体小鼠的右侧颈外静脉。从左侧颈总动脉收集血液,并通过共聚焦荧光显微镜对细胞进行成像。所示图像代表\(n=4\)次独立实验。比例尺:10μm。d 生成的血小板定量的门控策略。第18次传代后收集的灌流液中生成的血小板数量由P1门中的CD41(+)事件数量确定。e P1门中的事件(来自图1d所示的实验)被定义为生成的血小板(由红色箭头指示),与来自对照IgG-PE处理的巨核细胞的血小板相比,具有更高的平均荧光。P1门还捕获CD41阴性细胞,包括干细胞和宿主来源的血小板。分别通过Calcein-AM和DRAQ5染料检查生成的血小板的活力以及它们是否含有DNA。f 通过活性线粒体中四甲基罗丹明甲酯(TMRM)的积累来确定生成的血小板和对照血小板的线粒体膜电位,并通过流式细胞术进行测量。g 对(f)中的TMRM信号进行定量,并以平均值±标准误显示。\(N=5\)次独立实验;采用双尾非配对t检验。源数据在源数据文件中提供。
2. 肺血管系统:血小板生成的生理微环境与核心机制
1) 肺血管的独特结构与血小板生成优势
肺血管系统凭借其复杂的微血管网络、健康的肺内皮细胞及高效的气体交换功能,为血小板生成提供了得天独厚的生理条件。研究通过离体小鼠心肺模型证实,巨核细胞(血小板前体细胞)尽管直径达 50-100μm,仍能多次穿过平均内径仅 5-8μm 的肺毛细血管,通过核极化、去核等过程,最终每个巨核细胞可生成约 3000 个功能完整的血小板,这一效率与体内生理水平高度一致。
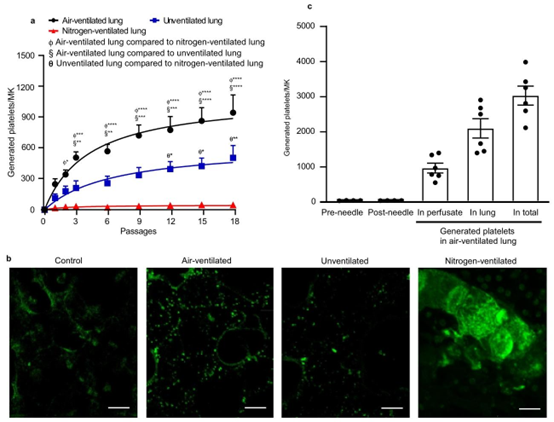
图2 | 巨核细胞通过小鼠肺血管体外生成血小板的定量分析。用CD41-PE或CD41-FITC抗体标记的小鼠巨核细胞(MKs)被反复通过体外肺血管。肺用空气、纯氮气通气或不通气。a 通过流式细胞术(FACS)测量在不同传代次数下,经空气通气(黑色圆圈)、纯氮气通气(红色三角形)或不通气(蓝色方块)的肺灌流液中每个巨核细胞生成的血小板数量。\(N=5\)(空气通气肺或不通气肺)和4次(氮气通气肺)独立实验。数据以平均值±标准误表示。采用双向方差分析(Two-way ANOVA)及Tukey多重比较检验,*\(^{*} p<0.05\)、\(^{*} p<0.01\)、\(\cdots p<0.001\)和\(^{* * *} p<0.0001\)。b 经染色的巨核细胞(CD41-FITC,绿色)被通过
2) 血小板生成的关键调控因素
研究明确了四大核心因素对肺血管血小板生成的调控作用:一是氧合作用,纯氮气通气导致的缺氧会几乎完全抑制血小板生成,而正常空气通气能维持内皮细胞线粒体膜电位稳定,为巨核细胞活化提供支持;二是通气功能,即使无通气条件下血小板仍可生成,但数量显著降低,证实通气通过直接作用于巨核细胞或间接改善内皮细胞功能调控血小板生成;三是肺内皮细胞健康状态,受损内皮细胞会导致血小板生成效率下降;四是微血管结构,肺毛细血管的分支特性与尺寸限制为巨核细胞的变形、去核提供了必要的机械刺激。此外,肌动蛋白调节因子原肌球蛋白 4(TPM4)在血小板生成的最终步骤中发挥关键作用,TPM4 缺陷小鼠的巨核细胞无法完成血小板释放,进一步揭示了细胞骨架重组在该过程中的核心价值。
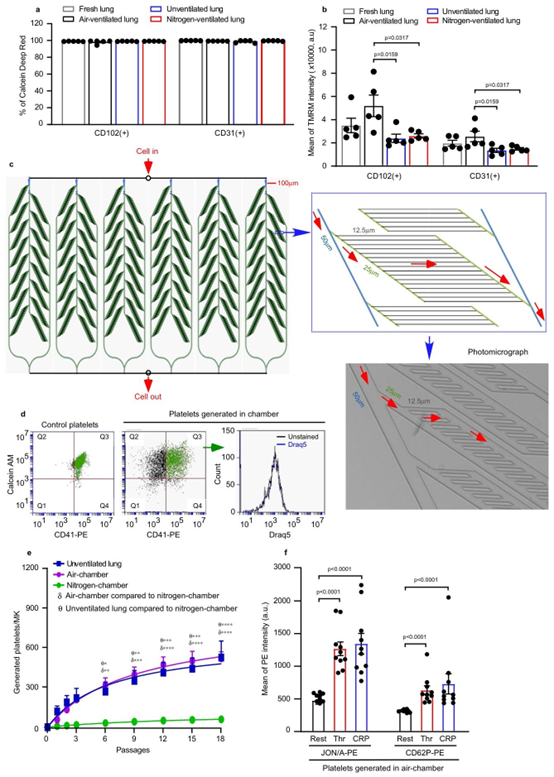
图3 | 肺内皮细胞健康和微血管结构在血小板生成中的作用。a、b 从通气约2小时的灌注肺中分离肺内皮细胞(ECs),通气气体为空气(黑色)或纯氮气(红色),或不通气(蓝色)。来自新鲜肺组织的内皮细胞作为对照(灰色)。用FITC偶联的抗CD31/PECAM-1或抗CD102/ICAM-2抗体对内皮细胞进行染色。每组进行\(N=5\)次独立实验。双尾
3. 微流控技术:体外复刻血小板生成的创新工具
1) 微流控芯片的设计与制备工艺
为体外复刻肺血管微环境,研究团队采用 PDMS 材料(聚二甲基硅氧烷),通过 MEMS 加工技术、光刻工艺制备了模拟肺微血管结构的微流控芯片。该芯片采用分支通道设计,通道深度统一为 10μm,宽度从 100μm 逐步递减至 12.5μm,完美还原了肺毛细血管的尺寸梯度与分支特性。芯片制备过程中,通过 PDMS 键合对准平台实现精准封装,结合等离子键合技术确保通道密封性,为细胞流动与相互作用提供稳定微环境。这种基于 PDMS 芯片的微流控系统,不仅具备气体通透性,还能通过流体力学调控模拟体内血流剪切力,为体外血小板生成提供了可控、可重复的研究工具。
2) 微流控芯片在血小板生成研究中的应用
实验证实,将巨核细胞注入微流控芯片后,经过 18 次循环灌注,每个巨核细胞可生成约 492 个血小板,虽低于离体肺模型的生成效率,但显著高于传统体外培养方法。生成的血小板具备典型的圆盘状形态,富含 α 颗粒、致密颗粒及微管线圈,且在凝血酶、胶原相关肽刺激下能正常激活并表达 P – 选择素,展现出与天然血小板相当的功能特性。此外,微流控芯片还能模拟缺氧、内皮细胞损伤等病理条件,为解析血小板生成障碍的分子机制提供了精准模型。该技术突破了传统 2D 培养无法还原生理微环境的局限,通过 MEMS 微纳加工技术实现了血管结构、流体力学与细胞相互作用的多维度复刻。
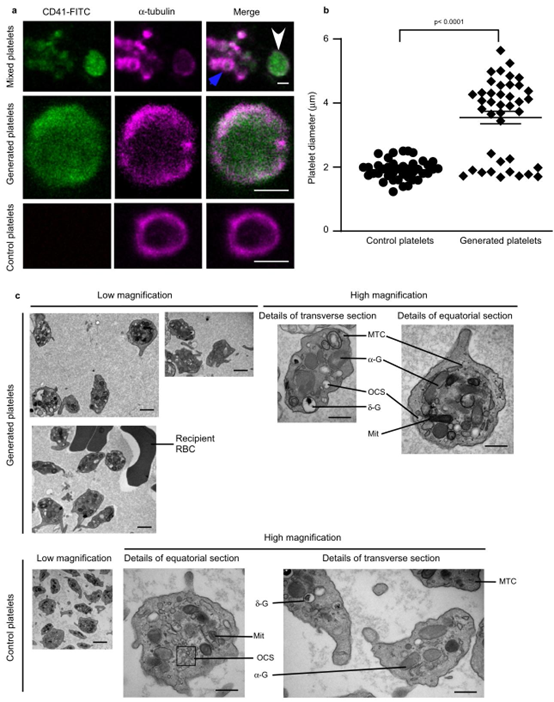
图4 | 生成的血小板表现出与对照血小板相当的典型物理特征。a、b 预先用CD41FITC(绿色)标记的小鼠巨核细胞(MKs)在体外反复通过肺血管。整个过程中肺都用空气通气。a 体外心肺制备的灌流液中含有生成的血小板(白色箭头)和宿主血小板(蓝色箭头),对其进行α-微管蛋白(品红色)染色,共聚焦图像在上部面板中显示为混合群体。中间面板(生成的血小板)和底部面板(对照血小板)的放大图像中显示了更详细的α-微管蛋白环图像。这些图像代表了\(n=3\)次独立实验。比例尺:2 µm。b 使用Fiji ImageJ-Win64测量a中血小板的直径(来自\(n=3\)次独立实验的40个血小板),生成的血小板直径为3.6±0.2 µm,对照血小板为1.9±0.05 µm。与对照血小板相比,根据直径范围,生成的血小板有两个亚群:约33%的生成血小板(直径范围:1.7-2.4 µm)与对照血小板(直径范围:1.2-2.4 µm)大小相似,67%的生成血小板(直径范围:3.7-5.6 µm)明显大于对照血小板。数据为平均值±标准误。双尾Mann-Whitney检验,\(P<0.0001\) c 通过透射电子显微镜观察生成的血小板和对照血小板的超微结构。在空气通气条件下将巨核细胞通过心肺制备物灌注之前,通过腹腔注射抗GPIbα抗体R300清除宿主血小板。高倍放大图像中显示并标注了亚细胞结构的缩写:α-G,α颗粒;σ-G,σ颗粒或致密体;Mit,线粒体;OCS,开放管道系统;MTC,微管线圈;RBC,红细胞。比例尺:低倍放大图像中为2 µm,高倍放大图像中为500 nm。所示图像代表了\(n=5\)次独立实验。源数据在源数据文件中提供。
4. 生成血小板的功能特性与临床应用潜力
1) 生成血小板的形态与功能优势
通过透射电镜与流式细胞术分析,微流控芯片及离体肺模型生成的血小板存在两个功能亚群:约 33% 的血小板尺寸与天然血小板一致(1.7-2.4μm),67% 为大尺寸血小板(3.7-5.6μm)。大尺寸血小板表面胶原受体(GPVI、CD49b、CD42d)表达水平更高,对凝血酶的反应性更强,展现出更优的黏附与聚集功能。在体外血栓形成实验中,生成的血小板能快速黏附于胶原表面,形成稳定血栓结构,其早期黏附能力甚至优于天然血小板,提示其在急性出血治疗中的潜在优势。
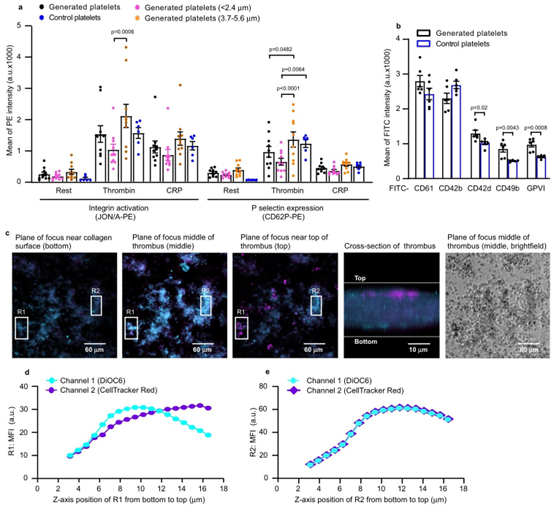
图5 | 生成的血小板在功能上与对照血小板相当。用CD41-FITC或CD41-PE抗体或DiOC6染料标记的小鼠巨核细胞(MKs),在体外通过肺血管系统传代18次。全程用空气给肺通气。a 通过流式细胞术(FACS)测量的,在2 U/mL凝血酶或5 µg/mL CRP-XL诱导下,洗涤后的生成血小板(CD41-FITC)与洗涤后的对照血小板中整合素αIIbβ3活化和P-选择素表达的平均荧光强度(MFI)。生成血小板的数据合并为总生成血小板(黑点),并按血小板大小分类(\(diameter <2.4 \mu m\)为粉点,直径3.7-5.6 µm为浅棕点),与对照血小板(蓝点)进行比较。使用颗粒大小标准试剂盒(货号PPS-6)估算生成血小板的大小。\(N=10\)(生成血小板)和6(对照血小板)次独立实验,数据为平均值±标准误。采用双因素方差分析(ANOVA)及Tukey多重比较检验,p值如图所示。b 通过流式细胞术测量表面糖蛋白。生成的血小板通过抗CD41-PE抗体染色来界定。表面糖蛋白用不同的FITC偶联抗体染色,如图所示。\(N=6\)次独立实验,数据为FITC强度的平均值±标准误。采用双尾非配对t检验,CD42d的p值为\(p=0.02\),CD49b的p值为\(p=0.0043\),GPVL的p值为\(p=0.0008\)。c 代表性富血小板血栓的图像。生成的血小板(呈蓝色,同时用DiOC6(青色)和CellTracker™Red CMTPX染料(品红色)染色)分布在血栓的各个层面,而宿主血小板(仅用CellTracker™Red CMTPX染料染色,品红色)主要位于血栓顶部。图像代表\(n=5\)次独立实验的结果。比例尺如图所示。d、e R1和R2(图5c中的区域1和区域2)沿z轴的MFI分布图。d R1沿z轴的MFI分布。在R1中,生成的血小板占据血栓的下部,直至约12 µm处(青色和品红色信号同时增强),而超过该点后,宿主血小板占主导(因为超过12 µm后,品红色信号强于绿色信号)。e R2沿z轴的MFI分布。在R2中,这部分血栓仅由生成的血小板组成,因为青色和品红色信号沿z轴同时变化。原始数据见原始数据文件。
2) 临床应用场景与技术转化方向
生成血小板的高效功能为临床输血提供了新的替代方案,尤其适用于稀有血型、血小板功能障碍患者及大规模灾害救援中的血液供应。结合器官芯片技术,未来可构建集成肺血管微环境、细胞培养与实时监测功能的一体化平台,实现血小板的规模化体外制备。此外,通过微流控芯片的定制化设计,可精准调控血小板生成的数量与功能亚群比例,满足不同临床场景需求。PDMS 芯片的可重复性与低成本优势,以及 MEMS 加工技术的规模化生产潜力,为该技术的临床转化奠定了基础。
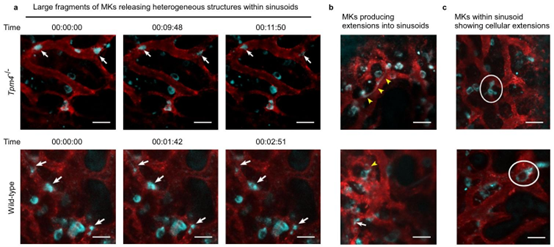
图8 | 活鼠颅骨骨髓巨核细胞的活体双光子显微镜图像。通过静脉注射抗CD105-AlexaFluor 546抗体和AlexaFluor 546标记的牛血清白蛋白(红色)使骨髓血管系统可视化。通过静脉注射抗GPIX-AlexaFluor 488抗体(青色)对巨核细胞(MKs)及其衍生物进行染色。野生型(WT)和原肌球蛋白\(4’\) \((T p m 4^{-1})\))巨核细胞通常被观察到与骨髓血窦壁紧密接触。每组(WT和Tpm4−/−)的图像均来自\(n=6\)只生物学独立的小鼠。比例尺,50微米。a 所示时间点,血窦血管内野生型和\(Tpm4\)巨核细胞的大碎片(白色箭头)沿血流方向释放异质结构的代表性图像。b 野生型和\(Tpm4\)巨核细胞的代表性图像,细胞体位于骨髓腔内,向血窦内延伸(黄色箭头)。c 血窦内野生型和\(Tpm4\)巨核细胞的代表性图像,显示细胞延伸(白色圆圈)。
5. 技术突破与未来展望
1) 核心技术突破的科学价值
本研究的核心突破在于首次明确了肺血管系统血小板生成的分子机制与关键调控因素,同时通过微流控技术实现了该过程的体外复刻。PDMS 芯片与 MEMS 加工技术的融合应用,解决了体外微环境复刻的关键难题,为造血功能研究提供了全新工具。而 TPM4 在血小板生成最终步骤中的关键作用,不仅揭示了细胞骨架调控的特异性机制,也为血小板生成障碍疾病提供了潜在治疗靶点。
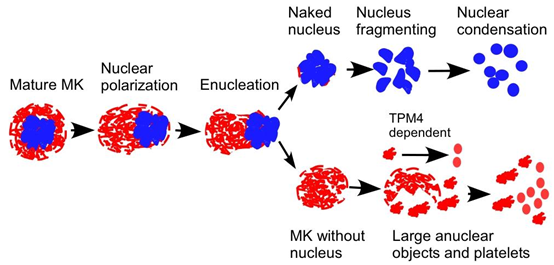
图9 | 成熟巨核细胞生成血小板的步骤示意图。该图显示了完整的成熟巨核细胞(MKs)通过反复穿过肺血管系统,最终形成血小板的生成途径。此过程涉及细胞核极化、去核、细胞质逐渐碎裂形成血小板(最后步骤依赖于原肌球蛋白4(TPM4))以及核碎裂和浓缩。
2) 未来发展方向与技术升级路径
未来,随着器官芯片技术的迭代,可构建多器官集成的微流控平台,结合 3D 细胞培养芯片技术,进一步提升血小板生成效率与功能稳定性。在芯片制备方面,可通过优化光刻胶模具设计、PDMS 浇筑工艺及键合技术,实现芯片通道尺寸的精准调控与规模化生产。同时,结合数字微流控技术与实时检测模块,可实现血小板生成过程的动态监测与质量控制。此外,将微流控芯片与干细胞技术结合,有望从多能干细胞诱导生成巨核细胞,进而实现血小板的全流程体外制备,彻底解决临床血小板供应短缺问题。
肺血管系统血小板生成机制的解析与微流控技术的创新应用,为体外血小板制备带来了革命性突破。PDMS 芯片、MEMS 加工、器官芯片等技术的融合,不仅实现了生理微环境的体外复刻,更构建了高效、可控的血小板生产体系。生成的血小板在形态与功能上与天然血小板高度一致,具备广阔的临床应用前景。随着微流控技术的不断升级与临床转化的推进,体外制备的血小板有望成为临床输血的重要补充,为血液疾病治疗与公共卫生应急提供关键支撑。同时,该研究也为其他血细胞的体外制备提供了可借鉴的技术范式,推动微流控生物芯片在再生医学领域的广泛应用。
参考文献:https://doi.org/10.1038/s41467-023-39598-9
© 2026. All Rights Reserved. 苏ICP备2022036544号-1













