1. 行业背景与技术瓶颈
CAR-T(嵌合抗原受体 T 细胞)疗法作为血液系统恶性肿瘤治疗的革命性手段,已在淋巴瘤、白血病等疾病的临床治疗中展现出显著疗效。目前全球已有十余款 CAR-T 产品获批上市,且大量临床研究正拓展其在实体瘤、自身免疫性疾病等领域的应用边界。然而,传统 CAR-T 生产流程存在难以突破的瓶颈:标准制备周期长达 9-14 天,导致具有 naive-like 表型(Tnlp)的 T 细胞(包括初始 T 细胞和干细胞样记忆 T 细胞)大量耗竭。这类细胞具备高增殖活性和自我更新能力,是维持 CAR-T 疗法长期疗效的关键,其缺失直接影响临床治愈率,约 50%-60% 的患者无法通过传统 CAR-T 疗法获得长期缓解。
此外,传统生产工艺依赖 48 孔板、6 孔板等常规培养载体,存在病毒载体与 T 细胞相互作用不足、转导效率低(通常仅 8%-17%)等问题,需使用高病毒滴度增加成本,同时延长的体外培养过程加剧了 T 细胞分化耗竭。在此背景下,基于微流控技术的创新平台应运而生,以 PDMS(聚二甲基硅氧烷)为核心材料的微流控芯片凭借其精准的流体操控能力、优异的生物相容性和可规模化加工特性,成为突破 CAR-T 生产瓶颈的核心解决方案。
2. PDMS 微流控平台的设计与制备工艺
1) 核心材料与加工技术
本研究采用 PDMS 作为微流控芯片的核心制备材料,通过软光刻技术结合 3D 打印模具实现平台加工。PDMS 材料因良好的生物相容性、透光性和弹性,成为微流控细胞培养芯片的首选材质,其加工过程兼容 MEMS(微机电系统)加工工艺,可实现高精度通道结构的批量制备。芯片模具采用 3D 打印技术定制,通过优化模具结构实现蛇形通道与扩大 incubation 区域两种拓扑设计,通道高度可在 50μm-200μm 范围内调节,适配不同体积的细胞 – 病毒混合体系。
在加工流程中,PDMS 微流控芯片的制备融合了光刻胶模具成型、PDMS 浇筑、键合对准等关键步骤。通过 MEMS 加工中的软光刻技术,将设计好的通道图案转移至光刻胶模具表面,随后浇筑 PDMS 预聚体并固化成型,最终通过等离子键合技术实现芯片密封。这种加工方式不仅保证了微流控芯片通道尺寸的一致性(误差小于 5%),还支持 PDMS 模具的定制化生产,可根据临床需求调整通道几何参数,为细胞与病毒的高效相互作用提供结构基础。
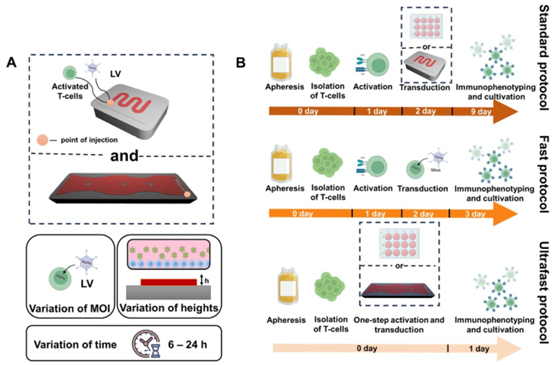
图1(A)所使用的MFD和所执行的优化步骤的示意图,其中包括转动惯量(MOI)、通道高度和孵育时间的变化。(B)超快、快速和标准方案的示意图。
2) 平台性能优化
研究团队通过系统优化微流控芯片的关键参数,包括通道高度、感染复数(MOI)和孵育时间,实现了转导效率与细胞活力的平衡。最终确定 150μm 通道高度为最优设计,对应工作体积 25μL,既缩短了病毒与 T 细胞的 “自由路径”,又保证了营养物质交换效率,细胞存活率维持在 85% 以上。在 MOI=3 的条件下,24 小时孵育周期成为最佳工艺参数,避免了高 MOI 导致的细胞毒性,同时通过微流控芯片的结构优势提升病毒颗粒的局部浓度,解决了传统培养中病毒扩散受限的问题。
此外,微流控芯片的表面修饰技术进一步优化了细胞 – 病毒相互作用。通过在 PDMS 通道内壁进行亲水修饰,降低了细胞吸附阻力,同时提升了病毒载体的附着效率,为后续的激活与转导同步进行奠定了基础。这种表面修饰与通道结构设计的协同优化,体现了微流控芯片在精细调控细胞微环境方面的独特优势。
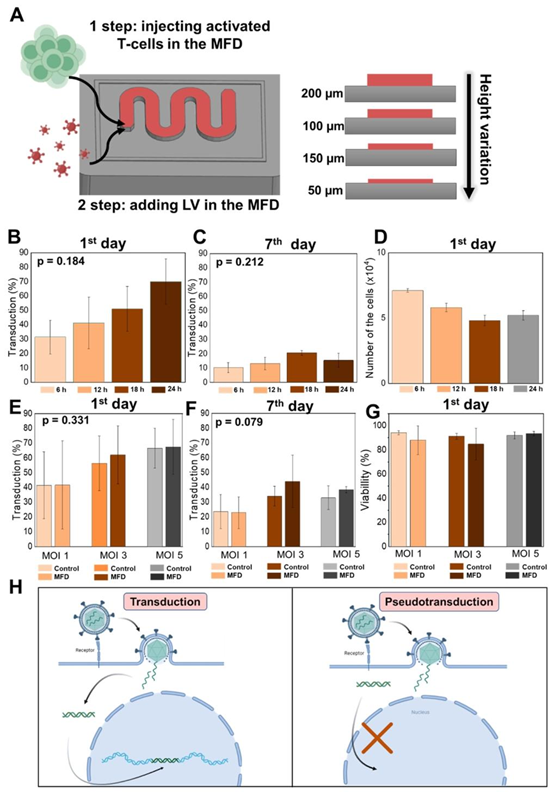
图2 利用MFD优化CAR-T细胞生产。(A)我们的MFD中CAR-T细胞生产的示意图。(B)在MFD中,第1天(6、12、18、24小时时间点)固定MOI为3时T细胞的转导效率。(C)在MFD中,第7天(6、12、18、24小时时间点)固定MOI为3时T细胞的转导效率。(D)在MFD中,第1天(6、12、18、24小时时间点)的T细胞产量。(E)在MFD中,第1天(6、12、18、24小时时间点)不同MOI(1、3、5)下T细胞的转导效率。(F)在MFD中,第7天(6、12、18、24小时时间点)不同MOI(1、3、5)下T细胞的转导效率。(G)在MFD中,第1天(6、12、18、24小时时间点)不同MOI(1、3、5)下的T细胞存活率。(H)转导和假转导过程的示意图。
3. 微流控细胞培养芯片驱动的 CAR-T 生产革新
1) 超快生产工艺的建立
基于 PDMS 微流控芯片的 CAR-T 生产工艺实现了 “激活 – 转导” 一体化,将总制备周期从传统的 9 天缩短至 24 小时,成为真正意义上的 “超快生产方案”。该工艺无需提前激活 T 细胞,而是将磁珠分选后的外周血单个核细胞(PBMCs)与抗 CD3/CD28 抗体修饰的生物可降解纳米颗粒、慢病毒载体(LV)在微流控芯片中直接混合孵育。
微流控芯片的通道设计加速了质量传递效率,病毒颗粒与 T 细胞的碰撞频率较传统培养板提升 3-5 倍,转导效率达到 27%(MOI=3),显著高于 48 孔板(17%)和 6 孔板(8%)的传统方法。这种同步激活与转导的模式,不仅简化了操作流程,更减少了体外培养对 Tnlp 细胞的耗竭,为提升 CAR-T 疗法的长期疗效提供了技术保障。
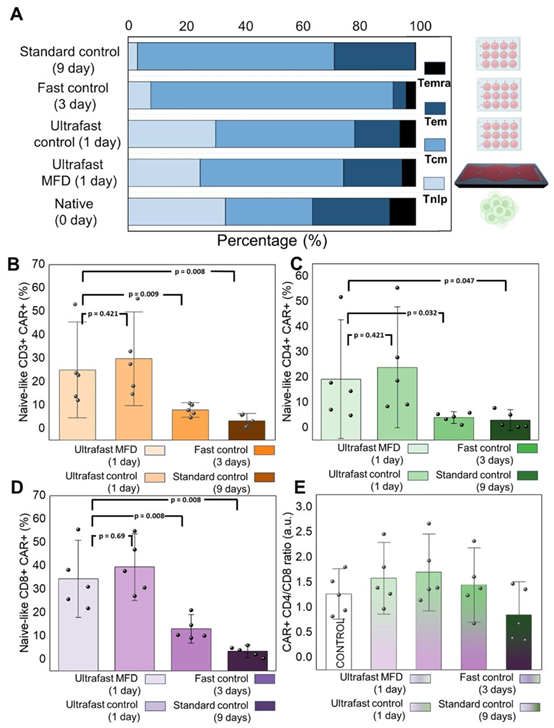
图5 使用标准、快速和超快速方案生产CAR-T细胞。(A)根据所用方案得到的CAR-T细胞的免疫表型。(B)表达CAR的初始样CD3+细胞的百分比。(C)表达CAR的初始样CD4+细胞的百分比。(D)表达CAR的初始样CD8+细胞的百分比。(E)表达CAR的CD4+/CD8+细胞的比例。
2) 细胞表型的高效保留
临床研究证实,Tnlp 细胞的比例与 CAR-T 疗法的持久缓解率直接相关。本研究通过微流控芯片生产的 CAR-T 产品中,CD3+ Tnlp 细胞比例达到 18.07±6.03%,是传统 9 天方案(3.97±2.37%)的 6 倍;CD4 + 和 CD8+ Tnlp 细胞比例分别为 11.07±6.08% 和 29.2±7.11%,同样远高于传统方案。这种表型优势源于微流控芯片缩短了体外培养时间,避免了 T 细胞向终末分化表型(Tem、Temra)的转化。
同时,PDMS 微流控芯片的生物相容性为细胞存活提供了保障,在 24 小时培养周期内,T 细胞活力维持在 90% 以上,与传统方案无显著差异。此外,微流控生产的 CAR-T 产品中 CD4+/CD8 + 比值保持在 1.63±0.65,更接近理想治疗窗口,有助于平衡抗肿瘤活性与治疗安全性。
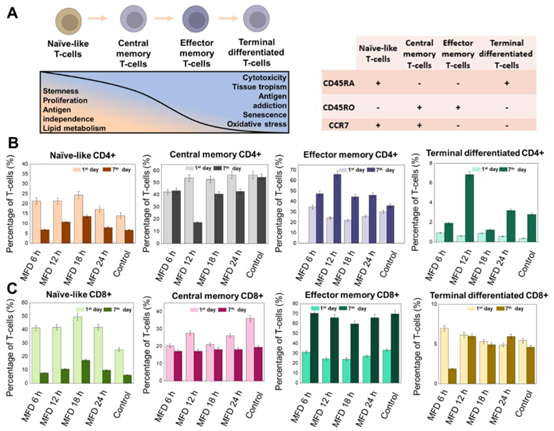
图3 转导后T细胞的免疫表型分析。(A)T淋巴细胞及其特性演变的示意图。(B)在微型生物反应器(MFD)中进行转导后的第1天和第7天(6、12、18、24小时时间点),根据其亚群组成的CD4+ T淋巴细胞百分比。(C)在微型生物反应器(MFD)中进行转导后的第1天和第7天(6、12、18、24小时时间点),根据其亚群组成的CD8+ T淋巴细胞百分比。
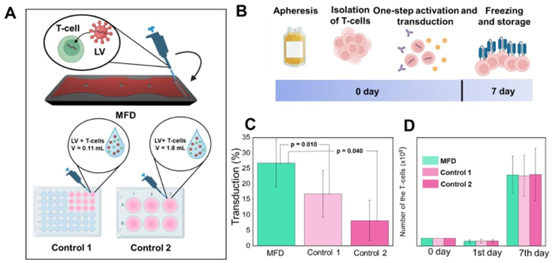
图4 MFD中的T细胞同时激活和转导。(A)MFD中的实验流程以及所使用的对照的示意图。(B)方案持续时间的示意图,包括单采、T细胞分离、一步激活与转导以及增殖。(C)第7天在MFD和孔板(对照1和对照2)中培养的T细胞的转导效率。(D)第0、1和7天在MFD和孔板(对照1和对照2)中培养的T细胞的增殖效率。
4. 技术优势与临床转化价值
1) 核心性能突破
与传统 CAR-T 生产工艺相比,PDMS 微流控平台展现出三大核心优势:一是生产效率的飞跃,24 小时超快周期大幅缩短患者等待时间,尤其适用于病情进展迅速的晚期患者;二是转导效率的提升,在低 MOI 条件下实现高转导率,降低了慢病毒载体的使用成本,解决了 CAR-T 生产中病毒载体昂贵的行业痛点;三是关键细胞表型的保留,Tnlp 细胞比例的提升直接关联临床疗效,为实现长期无病生存提供了可能。
此外,微流控芯片的规模化潜力显著,通过并行化设计可实现多通道同步培养,满足临床批量生产需求。其加工工艺兼容 MEMS 产业的成熟技术,PDMS 模具的标准化生产可降低芯片制造成本,为技术的广泛推广奠定基础。
2) 临床应用前景
该微流控技术不仅适用于抗 CD19 CAR-T 的生产,还可拓展至抗 BCMA、抗 CD22 等多种靶点的 CAR-T 产品,以及 TCR-T、NK 细胞疗法等其他细胞治疗领域。结合 3D 细胞培养芯片技术,未来可进一步构建模拟体内微环境的 “器官芯片级” 细胞培养系统,提升细胞疗法的临床转化效率。
在个性化医疗领域,PDMS 微流控芯片的定制化服务可满足不同患者的治疗需求,例如根据患者 T 细胞质量调整芯片通道结构、培养时间等参数,实现精准化生产。同时,该技术可与基因编辑技术(如 CRISPR-Cas9)结合,构建一体化的细胞治疗生产平台,推动细胞疗法向更高效、更安全、更可及的方向发展。
5. 行业发展与技术展望
微流控芯片技术在 CAR-T 生产中的突破,为细胞治疗行业带来了革命性变革。随着 PDMS 微流控芯片、MEMS 加工、3D 细胞培养芯片等技术的不断融合,细胞治疗生产正从传统的 “实验室级” 向 “工业级” 转型。未来,通过进一步优化微流控芯片的集成化设计,可实现细胞分选、激活、转导、扩增等全流程的自动化,降低人为操作误差,提升产品质量一致性。
在材料创新方面,除 PDMS 外,COC(环烯烃共聚物)、PMMA(聚甲基丙烯酸甲酯)等新型材料的应用将进一步拓展微流控芯片的适用场景,例如 COC 材料的耐温性可支持高温灭菌,适用于临床无菌生产需求。同时,表面修饰技术的创新的将进一步提升细胞与芯片的相互作用,例如通过抗原修饰实现特异性细胞捕获与定向培养。
作为细胞治疗领域的核心创新技术,微流控芯片赋能的 CAR-T 生产工艺不仅解决了传统工艺的效率与疗效瓶颈,更推动了细胞疗法的普惠化。随着技术的临床转化与规模化应用,未来将有更多癌症患者受益于这一创新方案,为肿瘤治疗带来新的希望。
参考文献:DOI: 10.1039/d5lc00139k
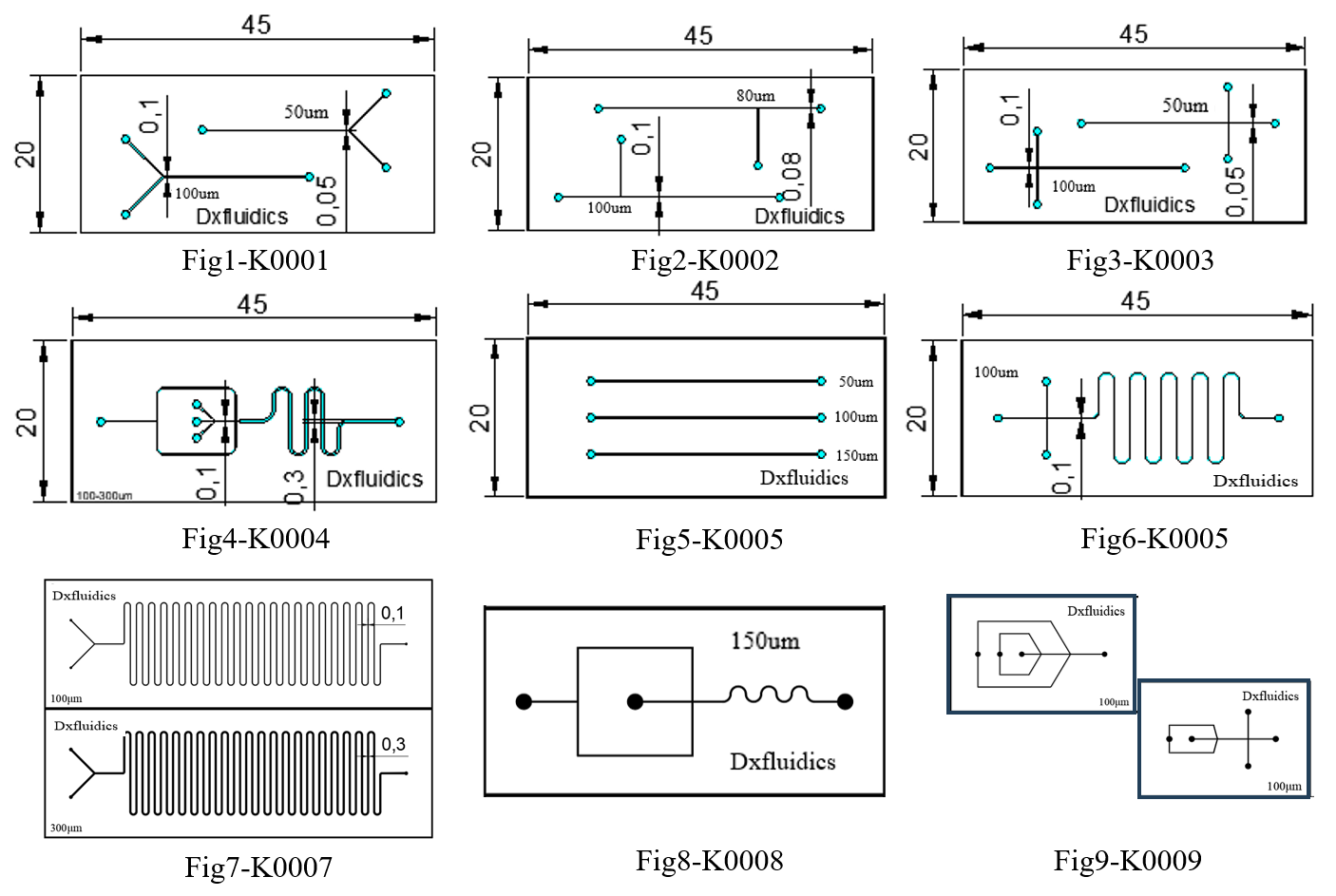
顶旭微控产品(标准PDMS芯片)
本公司也可提供特性化的微流控PDMS芯片加工服务,具体详情,欢迎来电咨询+86-17751163890(同微信),邮箱:sale@dxfluidics.com
| 产品编号 | 外形 (mm) | 高度 (um) | 宽度 (um) | 厚度 (mm) | 芯片材质 | 价格 (CNY) |
| K0001 | 45*20 | 50 | 50&100 | 3+1 | PDMS+Glass | 300 |
| K0002 | 45*20 | 50 | 80&100 | 3+1 | PDMS+Glass | 300 |
| K0003 | 45*20 | 50 | 50&100 | 3+1 | PDMS+Glass | 300 |
| K0004 | 45*20 | 50 | 100&300 | 3+1 | PDMS+Glass | 300 |
| K0005 | 45*20 | 50 | 50&100&150 | 3+1 | PDMS+Glass | 300 |
| K0006 | 45*20 | 50 | 100 | 3+1 | PDMS+Glass | 300 |
| K0007 | 75*25 | 100 | 100&300 | 3+1 | PDMS+Glass | 300 |
| K0008 | 52*25 | 100 | 100&150&200 | 3+1 | PDMS+Glass | 300 |
| K0009 | 35*24 | 100 | 100&200 | 3+1 | PDMS+Glass | 300 |
订购方式



© 2026. All Rights Reserved. 苏ICP备2022036544号-1












