全球流行病的爆发与人口老龄化进程的加快,对创新药物研发提出了前所未有的迫切需求,而传统药物研发模式面临着研发周期超十年、研发成本每十年翻倍、动物模型临床转化效率低、伦理争议突出等核心痛点。在此背景下,基于微流控技术的纳米器件凭借微型化、低样本消耗、高集成度、高通量筛选的核心优势,成为药物传感与筛选领域的革命性技术,为创新药研发、治疗药物监测、违禁药物筛查提供了全新的解决方案。以 PDMS 芯片为核心载体的微流控系统,不仅能在单细胞水平实现精准的药物分析,还可通过构建器官芯片模型,模拟人体器官的微观结构与生理功能,让药物筛选结果更贴近人体内的真实药效反应,彻底改变了传统药物研发的底层逻辑。
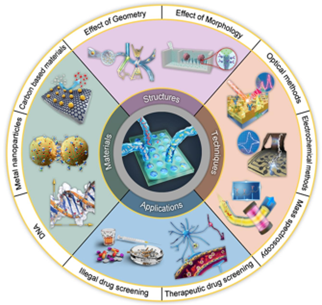
经(Wu等人,2019)许可转载,版权所有2019 Wiley-VCH,以及非法药物筛查。电化学,经(Xu等人,2021)许可转载,版权所有2021 Wiley-VCH,还有质谱法。在治疗学中的应用,经筛查和检测技术许可转载;光学,分别经(Liang等人,2019;Yu等人,2020)许可转载,版权分别为2019年、2020年Wiley-VCH;(He等人,2019),版权所有2019 Wiley-VCH,以及几何设计,经(Zhong等人,2021)许可转载,版权所有2021 Wiley-VCH。药物DNA,经(Nummelin等人,2018)许可转载,版权所有2018 Wiley-VCH。表面形态的影响,经(Kim等人,2014)许可转载,版权所有2014 Wiley-VCH;石墨烯,经(Song等人,2022)许可转载,版权所有2022 Wiley-VCH,以及图1。微流控辅助药物传感和筛查技术的示意图。传感材料的影响;金纳米颗粒,经许可转载
1. 微流控药物传感与筛选的三大核心检测技术体系
检测技术是微流控药物传感芯片的核心,目前主流的技术体系分为光学、电化学与质谱三大类,不同技术凭借各自的特性,适配了药物研发全流程的不同检测场景。
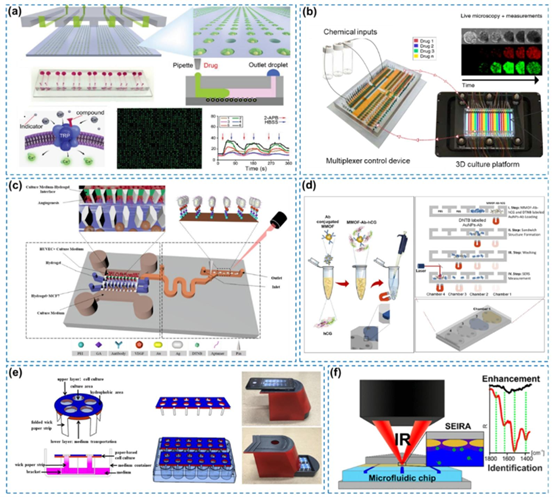
图2. 微流控设备中药物筛选的光学技术。(a)基于荧光的TRPs筛选微流控设备,经许可转载自(Ai等人,2020年),版权所有2020年Wiley-VCH。(b)基于芯片上荧光检测的抗癌药物对肿瘤类器官的组合药物筛选,经许可转载自(Schuster等人,2020年),版权所有2020年自然出版集团。(c)带有表面增强拉曼散射(SERS)检测单元的多功能微流控平台,用于监测不同细胞因子,经许可转载自(Qian等人,2020b),版权所有2020年美国化学会。(d)采用表面增强拉曼散射(SERS)检测器的毛细管驱动微流控芯片,用于检测尿液样本中的人绒毛膜促性腺激素(hCG)分子,经许可转载自(Ahi等人,2022年),版权所有2022年爱思唯尔。(e)具有灯芯状结构的纸基微流控设备,用于抗癌药物的比色筛选,经许可转载自(Fu等人,2021年),版权所有2021年Wiley-VCH。(f)集成原位红外光谱的微流控芯片,用于高灵敏度的单分子筛选,经许可转载自(Kratz等人,2018年),版权所有2018年美国化学会。
光学检测技术是目前微流控药物筛选中应用最广泛的技术体系,核心分为荧光、表面增强拉曼光谱(SERS)、比色与红外检测四大分支。其中,荧光检测凭借超高的灵敏度与特异性,成为小分子药物与细胞水平药物筛选的主流方案,可精准测定抗癌药物的半抑制浓度(IC50),结合微流控类器官芯片,能实时监测药物对肿瘤细胞的杀伤效果;SERS 技术借助等离子体纳米结构的信号增强效应,可实现单分子级的药物检测,能直接对唾液、尿液、汗液等真实生物样本中的药物分子进行定量,适配现场快速检测场景;比色检测凭借裸眼可视的显色反应,与纸基微流控芯片完美适配,实现了无需仪器的床旁快速检测;红外检测则通过无标记的分子指纹识别,无需复杂的探针修饰,即可完成药物分子的快速定量。
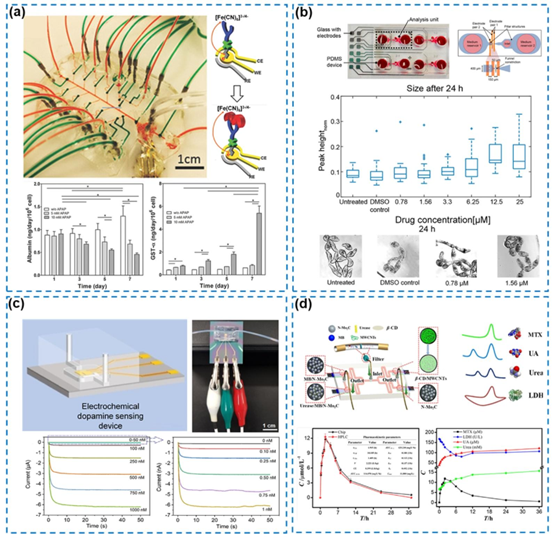
图3. 与微流控集成的不同电化学机制传感器。(a) 用于持续监测细胞分泌物的无标记和可再生电化学微流控生物传感器,经许可转载自(Shin等人,2017年),版权所有2017年Wiley-VCH。(b) 用于自动化抗血吸虫药物筛选的基于阻抗的微流控测定法,经许可转载自(Chawla等人,2018年),版权所有2018年美国化学会。(c) 用于帕金森病小鼠模型中脑脊液和血液多巴胺检测的微流控电化学传感器,经许可转载自(Senel等人,2020年),版权所有2018年美国化学会。(d) 多重微流控电化学传感器在血液肿瘤生物标志物监测中的应用,经许可转载自(Zhu等人,2020年),版权所有2018年美国化学会。
电化学检测技术凭借仪器结构简单、易微型化、成本低、易与微流控芯片集成的优势,成为小型化药物传感设备的核心方案。该体系涵盖电化学阻抗谱、安培法、循环伏安法、差分脉冲伏安法等技术,可实现无标记、非侵入式的药物检测,不仅能对生物标志物进行超灵敏定量,还能对细胞分泌物进行长期动态监测,完美适配器官芯片的药物毒性长期评价实验,最低检测限可达到飞摩尔级别。
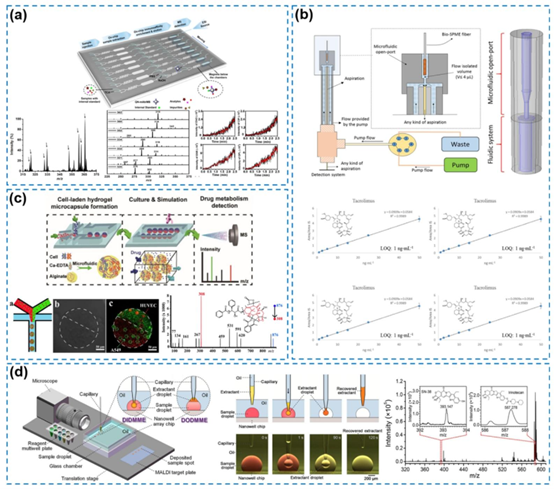
图4. 微流控装置中药物筛选的质谱技术。(a) 用于分析牛奶中残留喹诺酮类药物的集成微流控装置与质谱联用,经许可转载自(Zhao等人,2019年),版权所有2019年美国化学会。(b) Bio-SPME装置与质谱联用用于免疫抑制药物分析,经许可转载自(Tascon等人,2018年),版权所有2018年美国化学会。(c) 用于探测肿瘤-内皮细胞共培养模型中耐药性的集成微流控芯片与质谱联用,经许可转载自(Zheng等人,2020年),版权所有2019年爱思唯尔B.V.,代表中国化学会和中国医学科学院药物研究所。(d) 用于细胞液滴代谢物分析的快速灵活的液滴-液滴微流控微萃取系统,经许可转载自(Sun等人,2020年),版权所有2020年美国化学会。
质谱联用技术则是药物代谢与精准定量的金标准,微流控芯片与质谱的集成,实现了样本前处理、分离、检测的全流程自动化,大幅缩短了分析时间,降低了样本消耗,同时提升了检测通量。该技术可广泛应用于抗生素残留检测、免疫抑制剂血药浓度监测、抗癌药物代谢物分析等场景,纳升级的样本消耗即可实现超高精度的药物定量,是药物代谢研究与治疗药物监测的核心工具。
2. 决定微流控药筛器件性能的核心要素:材料、结构与加工工艺
微流控药物传感芯片的性能,由传感材料、芯片制备材料、微纳结构设计与加工工艺共同决定,这也是微流控芯片设计与制备的核心环节。
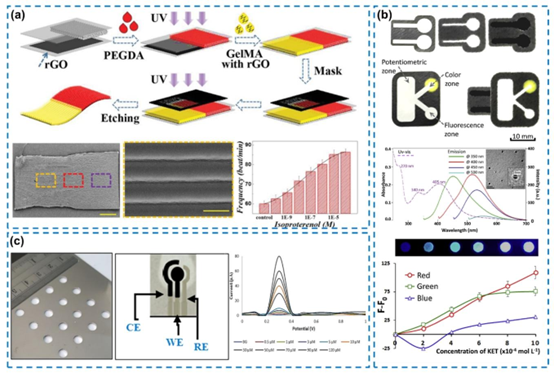
图5. 碳衍生物作为微流控装置中的传感材料。(a)用于心脏传感和分析的具有多种颜色的还原氧化石墨烯杂化各向异性结构膜,经许可转载自(Li等人,2019年),版权所有2019年Wiley-VCH。(b)一种新型三模态系统,其中碳量子点用于荧光传感,经许可转载自(Yehia等人,2020年),版权所有2020年Elsevier。(c)基于石墨烯的电化学方法对多巴胺的微流控检测,经许可转载自(Manbohi和Ahmadi,2019年),版权所有2019年Elsevier。
在材料体系上,分为传感材料与芯片制备材料两大维度。传感材料直接决定了检测的灵敏度与特异性,主流材料包括碳基材料(还原氧化石墨烯、碳纳米管、碳量子点)、金属纳米颗粒(金纳米颗粒、银纳米颗粒)、DNA 与适配体材料,通过不同材料的复合修饰,可实现对目标药物分子的高特异性捕获与信号放大。芯片制备材料则决定了微流控芯片的加工性能与生物相容性,其中 PDMS 是目前应用最广泛的基材,凭借易浇筑、低固化温度、纳米级成型精度、优异的气体渗透性与生物相容性,成为 PDMS 芯片加工的首选材料,适配实验室级芯片定制与小批量制备;玻璃与硅基材料凭借优异的光学性能与化学稳定性,多用于高精度微流控玻璃芯片的加工,适配 MEMS 加工工艺;COC、PMMA 等高分子材料则适配注塑工艺的规模化芯片量产,水凝胶材料则成为 3D 细胞培养芯片的核心基材,能高度模拟人体细胞外基质的生理环境。
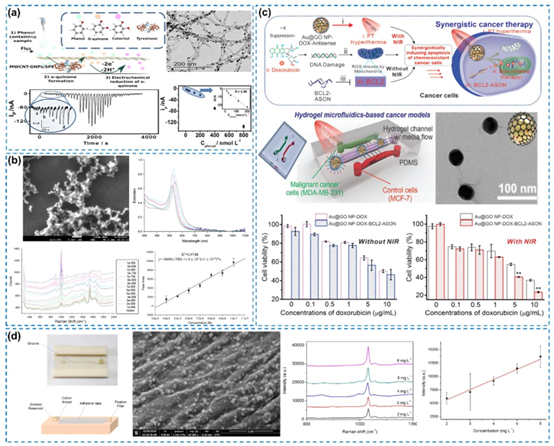
图6. 基于金属纳米颗粒的微流控药物传感。(a)基于商用纺织线基微流控装置与多壁碳纳米管/金纳米颗粒修饰电极组合的苯酚检测,经许可转载自(Caetano等人,2018年),版权所有2018年Elsevier。(b)在微流控通道中基于硼酸根包覆的金纳米颗粒,利用表面增强拉曼散射技术检测甲基苯丙胺、可卡因和吗啡,经许可转载自(Kline等人,2016年),版权所有2016年美国化学会。(c)基于石墨烯-金纳米颗粒杂化物的核酸和阿霉素对癌症凋亡的成像,经许可转载自(Yang等人,2021年),版权所有2021年Wiley-VCH。(d)在纺织线上合成金纳米颗粒用于微流控装置中的尼古丁检测,经许可转载自(Adamo等人,2020年),版权所有2020年Elsevier。
加工工艺是微流控芯片从设计到落地的核心,微纳加工技术的成熟度直接决定了芯片的制备精度与成本。光刻技术是目前主流的微流控芯片制备工艺,通过光刻机完成 SU8 模具、光刻胶模具的制备,再通过 PDMS 浇筑完成芯片微结构的复制,配套 PDMS 键合机、PDMS 对准平台完成芯片的封装与键合;深硅刻蚀、阳极键合等 MEMS 加工工艺,多用于硅基与玻璃芯片的高精度制备;电子束光刻技术则可实现纳米级的微纳结构加工,满足超高灵敏度传感芯片的制备需求。
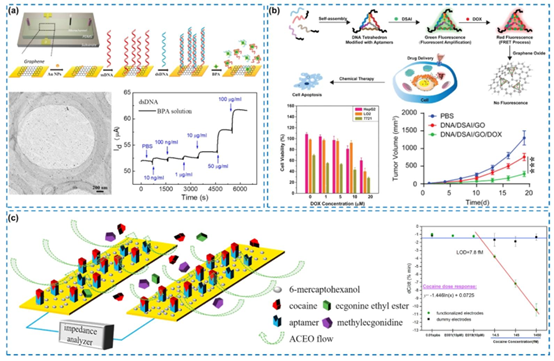
图7. 基于微流控装置的DNA药物传感。(a) 基于DNA功能化石墨烯和微流控装置的双酚A筛选,经许可转载自(Liu等人,2018年),版权所有2018年美国化学会。(b) 用于肝癌细胞诊断和治疗的DNA修饰氧化石墨烯基微流控,经许可转载自(Ma等人,2021年),版权所有2021年Wiley-VCH。(c) 基于适配体修饰微流控系统的血清可卡因检测,经许可转载自(Oueslati等人,2018年),版权所有2018年爱思唯尔。
微流控通道的几何设计与表面形貌,是影响药物筛选效率与检测灵敏度的关键。在几何结构上,经典的 “圣诞树” 型浓度梯度发生器,可实现多浓度药物的同步生成与筛选;分叉、螺旋、三维互连的通道结构,可模拟人体血管的生理环境,构建血管器官芯片;橄榄型、胶囊型的微腔设计,可解决检测过程中的气泡干扰问题,提升检测稳定性。在表面形貌上,纳米间隙、树枝状、微柱阵列等微纳结构,可大幅增强检测信号,提升传感灵敏度,是高性能微流控传感芯片的设计核心。
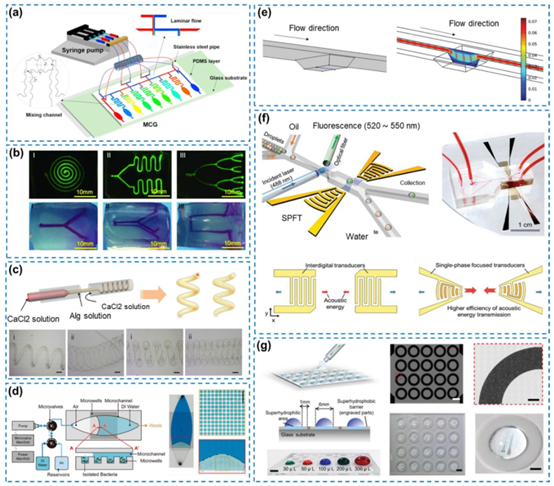
图8. 不同微流控平台的多种几何结构的代表性示例。(a) 基于浓度梯度发生器的微流控装置及大范围流速,经许可转载自(Shi等人,2019年),版权所有2019年Elsevier。(b) 用于开发血管化组织或器官模型的分支状、螺旋状、蛇形和3D互连形式的微流控通道示意图,经许可转载自(Nie等人,2018年),版权所有2018年Wiley-VCH。(c) 基于水凝胶的螺旋中空微纤维的示意图,其用于模拟血管的结构特征和血液涡流,经许可转载自(Li等人,2019年),版权所有2019年Wiley-VCH。(d) 一种橄榄形微流控微孔装置,该装置与基于气泡产生换能器的液滴分选器配合使用,用于生物相容性药物筛选,经许可转载自(Zhong等人,2021年),版权所有2021年Wiley-VCH。(g) 一条使用计算流体动力学(CFD)的鱼,经许可转载自(Kohl等人,2021年),版权所有2021年Wiley-VCH。(f) SERS-AST协议中单相聚焦的示意图,经许可转载自(Liao等人,2021年),版权所有2021年Elsevier。(e) 基于微流控腔囊的高通量药物筛选系统的3D平流-扩散模型,经许可转载自(Tang等人,2022年),版权所有2022年Wiley-VCH。
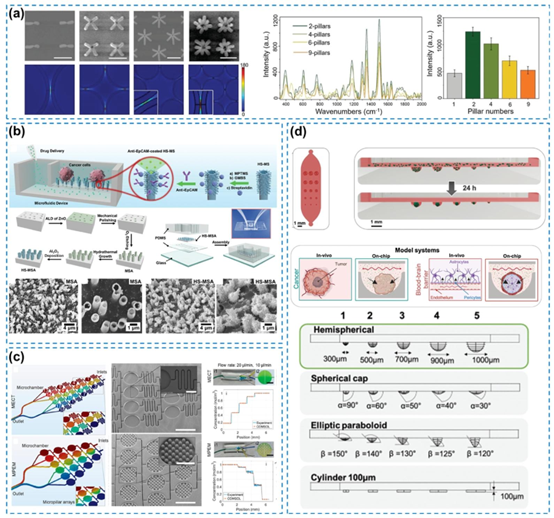
图9. 微流控平台表面不同形貌的代表性示例。(a) 一种嵌入3D纳米间隙等离子体结构的微流控装置,用于增强SERS信号,经许可转载自(Lao等人,2020年),版权所有2020年Wiley-VCH。(b) 具有分级尖刺微吸管结构的微流控装置捕获循环肿瘤细胞(CTCs)的示意图,经许可转载自(He等人,2019年),版权所有2019年Wiley-VCH。(c) 用于在微腔室内生成梯度的嵌入微柱的微流控装置设计,经许可转载自(Jaberi等人,2020年),版权所有2020年美国化学会。(d) 用于控制球体大小和生长动态的多尺寸、不同形状的微腔阵列,经许可转载自(Eilenberger等人,2021年),版权所有2021年Wiley-VCH。
3. 微流控技术在药物筛选领域的落地应用与行业发展趋势
目前微流控纳米器件已在治疗药物筛选与违禁药物筛查两大场景实现了规模化应用。在治疗药物筛选领域,微流控技术实现了从单靶点检测到多器官联合药筛的跨越,通过肝器官芯片、肺器官芯片、肾器官芯片、血脑屏障芯片等单器官模型,可精准评估药物的器官毒性与代谢特性;多器官芯片则能模拟药物在人体内的完整代谢路径,大幅提升药物临床转化的成功率;同时,基于肿瘤类器官的微流控药筛芯片,可实现抗癌药物的高通量个性化筛选,为肿瘤精准医疗提供了核心支撑。在违禁药物筛查领域,微流控芯片凭借小型化、快速检测的优势,可实现唾液、血液、尿液等样本中吗啡、可卡因、甲基苯丙胺等违禁药物的现场快速检测,纸基微流控芯片更是实现了无仪器的现场筛查,适配禁毒执法的现场检测需求。
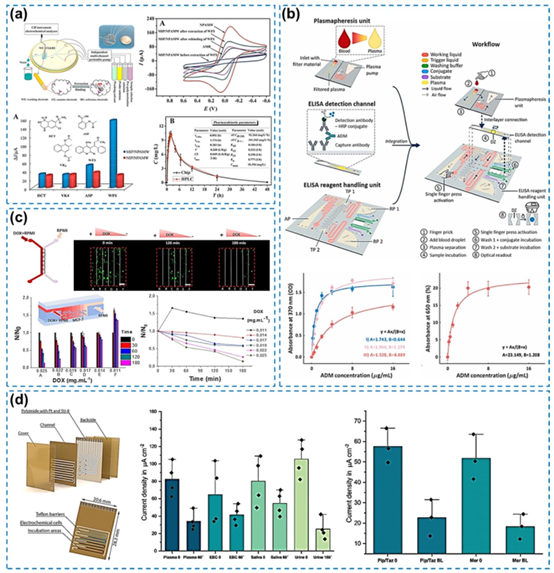
图10. 用于治疗药物传感的微流控装置示意图。(a) 芯片结构示意图以及MIP/NIP修饰的NPAMR对WFS的传感响应,经许可转载自(Liu等人,2017年),版权所有2017年Elsevier。(b) 集成FO探针的卡盒设计3D视图以及用于ADM检测的一步式FO-SPR生物测定法,经许可转载自(Qu等人,2022年),版权所有2022年Elsevier。(c) 自供能ADM检测芯片及其所有组件的示意图,包含ADM ELISA优化,经许可转载自(Ordutowski等人,2022年),版权所有2022年Elsevier。(d) 堆叠式多重生物传感器(Biosensor X)的3D渲染图,以及给予正常剂量哌拉西林/他唑巴坦和美罗培南的动物血浆样本中两种不同β-内酰胺类药物的时间依赖性分析,经许可转载自(Ates等人,2022年),版权所有2022年Wiley-VCH。
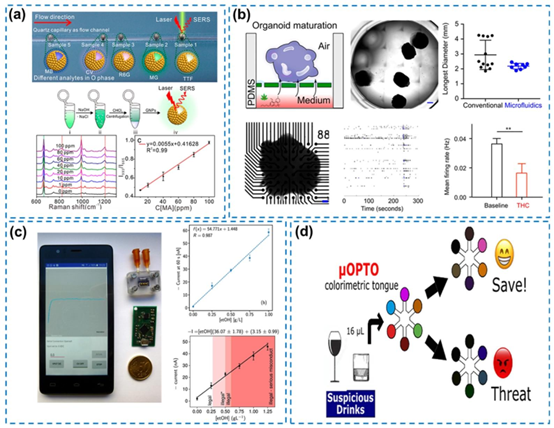
图11. 微流控平台对不同违禁药物的传感和筛选示意图。(a)用于检测甲基苯丙胺的在线类镜面光子晶体膜装置,经许可转载自(Su等人,2019年),版权所有2019年美国化学会。(b)用于筛选大麻暴露影响的一站式微流控脑类器官组装示意图,经许可转载自(Ao等人,2020年),版权所有2020年美国化学会。(c)基于智能手机的全血样本酒精检测系统示意图,经许可转载自(Aymerich等人,2018年),版权所有2018年爱思唯尔。(d)用于生物碱药物传感和筛选的纸基微流控舌,经许可转载自(Dias等人,2021年),版权所有2021年爱思唯尔。
当前微流控药物传感与筛选技术仍面临着芯片加工与操作流程标准化不足、非特异性分子吸附干扰、检测系统全集成化程度低等行业挑战。未来,微流控技术将朝着全集成化、自动化、智能化的方向发展,结合 AI 算法实现药筛数据的自动化分析与解读;微流控芯片定制与代工服务的产业化成熟,将大幅降低技术的应用门槛;而类器官芯片与微流控技术的深度融合,将进一步替代传统动物模型,成为创新药研发的核心工具,推动全球药物研发行业的降本增效与技术革新。
参考文献:doi.org/10.1016/j.bios.2022.114783
© 2026. All Rights Reserved. 苏ICP备2022036544号-1












