1. 微流控技术与 POC 体外诊断的发展背景
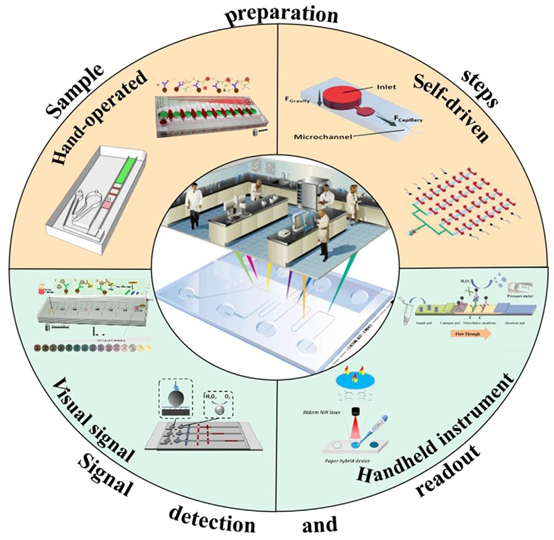
图1 用于即时诊断(POC)的集成微流控装置
床旁即时诊断(POC)作为体外诊断(IVD)领域的核心发展方向,其核心需求是实现检测流程的便携化、快速化与操作简化,摆脱传统实验室检测对大型设备、专业操作人员与复杂操作流程的依赖。传统 IVD 技术如酶联免疫吸附试验(ELISA)、聚合酶链式反应(PCR)虽具备高灵敏度与高特异性,但受限于仪器体积、操作复杂度与检测周期,无法满足去中心化的现场检测需求。
发表于《Aggregate》的这篇权威综述,系统梳理了近三年集成微流控器件在 POC 诊断领域的技术突破,核心围绕 “样本进 – 结果出” 的芯片设计理念,从材料选型、微纳加工工艺、全流程功能集成到临床场景落地,全面剖析了微流控技术的发展现状。微流控技术可将样本处理、生化反应、分离检测等多个实验室流程集成至平方厘米级的芯片上,凭借微量试剂消耗、快速分析、高集成度与便携性的核心优势,已成为 POC 诊断技术升级的核心解决方案。
2. 微流控芯片制备的核心材料与加工工艺
材料选型与加工工艺是微流控芯片性能与产业化落地的核心基础,综述中明确指出,芯片材料的表面特性、光学性能、生物相容性与量产适配性,直接决定了器件的应用场景与功能实现,目前行业主流的制备材料可分为三大类,配套的加工技术也形成了成熟的技术体系。
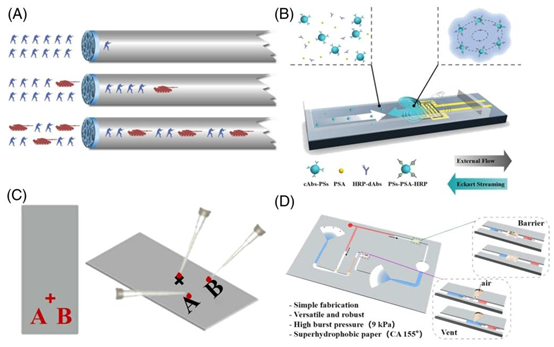
图2 材料科学创新在微流控装置中的应用。(A)一种通过水凝胶基质变化检测可卡因的玻璃毛细管装置。经许可转载。[18] 版权所有2019,施普林格·自然。(B)一种基于聚二甲基硅氧烷(PDMS)的微流控装置,该装置将轮廓模式声流镊子与基于微珠的免疫测定相结合。经许可转载。[28] 版权所有2021,美国化学会。(C)一种用于检测红细胞中ABO和Rh(D)抗原的聚甲基丙烯酸甲酯(PMMA)条带测试。经许可转载。[32] 版权所有2018,爱思唯尔。(D)一种用于纸基微流控装置中集成液体处理的疏水阀。经许可转载。[37] 版权所有2019,美国化学会。
无机材料中,玻璃是高精度微流控芯片的经典基材,具备优异的光学透明性、稳定的表面化学特性与低非特异性吸附优势,通过湿法化学刻蚀、等离子干法刻蚀可实现微米级微流道的精准制备,常通过阳极键合、等离子键合工艺与 PDMS 层复合,形成适配高稳定性生化检测的玻璃微流控芯片。同时玻璃基材易实现环氧基、醛基、羧基等功能化修饰,可稳定固定生物识别分子,是免疫诊断、核酸检测芯片的核心基材之一。
高分子聚合物是目前生物医学微流控领域应用最广泛的材料,其中 PDMS(聚二甲基硅氧烷)占据核心地位。PDMS 具备优异的生物相容性、高气体渗透性与光学透明性,通过软光刻工艺配合 PDMS 热板、PDMS 烘箱、PDMS 浇筑器,可快速完成芯片浇筑成型,配套 PDMS 等离子键合机、PDMS 键合对准平台可实现芯片的高精度封装,是器官芯片、3D 细胞培养芯片、类器官芯片研发的核心基材。针对 PDMS 量产一致性难题,综述也提及了 PMMA(聚甲基丙烯酸甲酯)、COC/COP 等热塑性材料的应用,这类材料可通过热压印、注塑成型实现规模化量产,适配微流控芯片的工业化生产需求,通过紫外梯度照射工艺还可实现表面润湿性的精准调控,构建自驱动毛细管微流控系统。
纸基材料则凭借低成本、便携性与天然毛细管特性,成为资源受限地区 POC 检测的核心方案,通过蜡印、喷墨打印即可完成微流道图案化,配套疏水阀、可溶性延迟结构可实现多步检测流程的自动化控制。而微纳加工技术的持续进步,包括光刻、电子束光刻、深硅刻蚀、镀膜等 MEMS 核心工艺,以及桌面式光刻机、紫外光刻机等设备的普及,大幅降低了微流控芯片研发与加工的门槛,推动了微流控芯片定制、代工产业的快速发展。
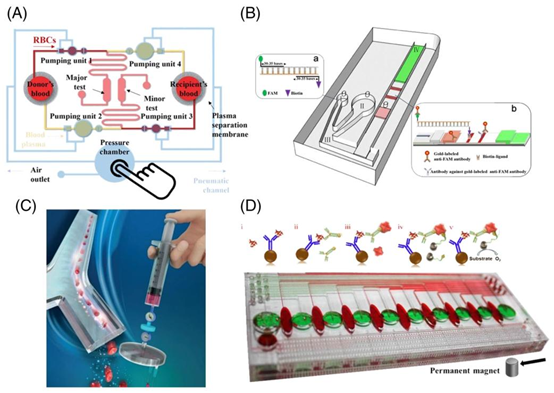
图3 手动样品处理。(A)为血液交叉配型开发的手指驱动微流控装置。经许可转载。[48] 版权所有2018,英国皇家化学会。(B)将侧向流设计与重组酶聚合酶扩增(RPA)相结合的微流控装置,通过翻转和摇动芯片来检测SARS-CoV-2。经许可转载。[50] 版权所有2021,英国皇家化学会。(C)用于手动驱动、连续流微流控样品注入的注射器流量稳定器。经许可转载。[51] 版权所有2019,英国皇家化学会。(D)微流控酶联免疫吸附测定(ELISA)通过简单操作内置磁体,实现疾病生物标志物的“样品进-答案出”检测。经许可转载。[52] 版权所有2017,爱思唯尔。
3. 集成微流控器件的核心功能创新
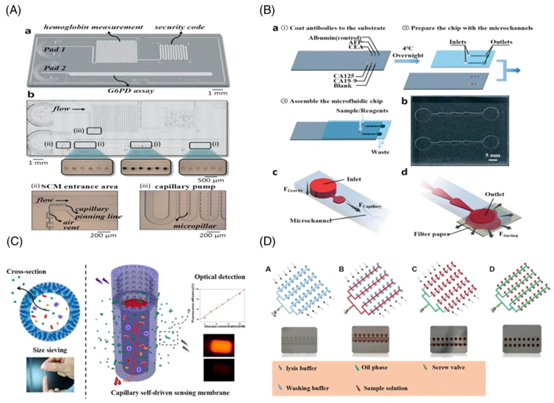
经许可转载。[57] 版权所有 2021,英国皇家化学会。(B) 用于检测多种生物标志物的毛细管自启动微流控芯片。经许可转载。[58] 版权所有 2021,英国皇家化学会。(C) 基于中空纤维膜(HFM)的微流控装置的机理。经许可转载。[59] 版权所有 2020,美国化学会。(D) 基于真空的液体泵送和采样过程。经许可转载。[60] 版权所有 2020,英国皇家化学会。图4 自驱动样品制备。(A) 用于G6PD检测和血红蛋白浓度测定的毛细管驱动微流控芯片。
综述中重点强调,集成微流控芯片的核心突破,在于实现了样本前处理与信号检测两大核心环节的全集成,彻底解决了传统 POC 检测操作复杂、依赖外接设备的痛点。
样本前处理是 POC 诊断的核心瓶颈,传统实验室检测需要离心、移液、孵育等多步人工操作,而集成微流控芯片通过结构设计与表面修饰技术,实现了无外接设备的流体精准控制。手动操作体系中,SlipChip 技术、手指驱动、手摇振荡、磁珠操控、注射器稳流等方案,仅通过人工操作即可完成试剂混匀、样本分离、核酸提取等全流程处理;自驱动体系则通过毛细管力、PDMS 脱气真空驱动等原理,配合芯片表面亲水修饰、疏水修饰、PEG 修饰等功能化工艺,精准调控微通道的流体行为,无需任何外接泵阀系统,即可实现检测流程的全自动化,真正实现了 “样本进 – 结果出” 的检测体验。
信号检测环节的创新,则让微流控芯片彻底摆脱了对大型实验室检测设备的依赖。综述中总结了两大类主流检测方案:一是可视化裸眼检测,包括比色强度分析、多色显色、距离式读数等方案,通过金纳米棒、铂纳米颗粒等信号标签,将靶标物浓度转化为肉眼可识别的颜色变化或条带长度,无需任何仪器即可完成半定量 / 定量检测;二是手持仪器辅助检测,将智能手机、手持压力计、数字温度计等民用设备与微流控芯片结合,实现了检测信号的高灵敏度定量读取,大幅提升了 POC 检测的准确性与场景适配性。
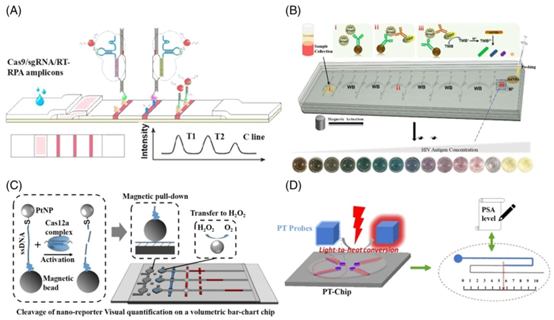
图5 信号输出可视化的不同模式。(A) 在纸质芯片中通过CRISPR/Cas9介导的sgRNA探针三线检测。经许可转载。[61] 版权所有2020,Wiley-VCH。(B) 表面蚀刻金纳米棒(AuNR)用于基于抗体的HIV-1(人类免疫缺陷病毒1型)p24蛋白半定量比色检测。经许可转载。[66] 版权所有2020,美国化学会。(C) 在靶标存在时,通过CRISPR-Cas12a切割的单链DNA(ssDNA)将铂纳米颗粒(PtNPs) tethered到磁珠上。释放的磁珠通过体积 chamber 中的\(H_{2} O_{2}\)淬灭产生\(O_{2}\)气体,以驱动读数。经许可转载。版权所有2019,美国化学会。(D) 通过铂纳米颗粒的光热活化在刻度 chamber(即芯片尺子)中产生用于基于压力的读数的气体。经许可转载。[70] 版权所有2021,美国化学会。
4. 临床应用场景与行业发展挑战
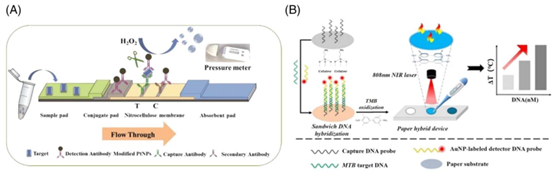
图6 手持仪器的信号检测。(A)使用带纸基装置的外部压力计检测疾病相关蛋白。经许可转载。[81] 版权所有2019,英国皇家化学会。(B)用于细菌DNA定量光热检测的手持数字温度计。经许可转载。[86] 版权所有2020,美国化学会。
基于材料与功能的技术创新,集成微流控芯片已在 POC 诊断的三大核心领域实现了规模化应用:蛋白靶向的免疫诊断、核酸分子检测与小分子代谢物分析。在免疫诊断领域,微流控芯片可实现痕量肿瘤标志物、病原微生物抗原的高灵敏度检测,新冠疫情期间也推动了相关抗原检测芯片的快速落地;核酸检测领域,全集成微流控芯片可完成核酸提取、等温扩增、信号检测全流程,大幅降低了气溶胶污染风险,适配基层与现场的病原微生物快速检测;小分子代谢物检测领域,微流控芯片可实现血清、汗液、唾液等样本中维生素、血糖、乳酸等标志物的快速无创检测,拓展了 POC 诊断的家用与慢病管理场景。同时,微流控技术也在器官芯片、细胞共培养芯片、细胞分选芯片领域实现了跨界应用,为体外生理模型构建、药物筛选提供了全新的技术平台。
综述也客观指出了行业当前面临的核心挑战:一是芯片操作的用户友好性仍需提升,试剂预载、单步上样的方案仍需进一步优化;二是检测结果的标准化与一致性,不同操作人员、不同使用环境下的结果稳定性仍需加强;三是微流控芯片的量产工艺与成本控制,如何实现高性能芯片的规模化、低成本生产,是临床转化与商业化的核心门槛。未来,随着微纳加工工艺的持续升级、芯片功能的全集成化与检测设备的便携化,集成微流控芯片将进一步推动 POC 诊断的去中心化发展,为基层医疗、居家检测、应急现场检测等场景提供更可靠的技术支撑。
参考文献:DOI: 10.1002/agt2.184
© 2026. All Rights Reserved. 苏ICP备2022036544号-1












