参考文献:https://doi.org/10.1002/smmd.70010
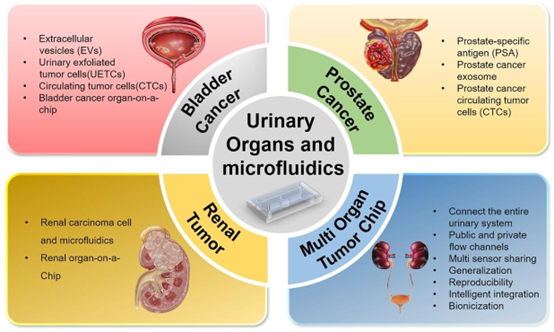
微微流体芯片作为一种在微米尺度操控流体的微型装置,凭借其精准模拟生理微环境、高效处理生物样本等优势,已成为膀胱癌(BCa)、前列腺癌(PCa)和肾癌(RCa)等原发性泌尿系统肿瘤研究的关键工具。与传统动物模型的异质性及人体研究的伦理限制相比,微流体技术(尤其是器官芯片,OOC)能通过仿生设计再现尿动力学状态,探索机械力相关信号通路(如 Hippo-YAP/TAZ)在肿瘤发生中的作用,为疾病诊断、药物筛选和个性化治疗提供了全新平台。
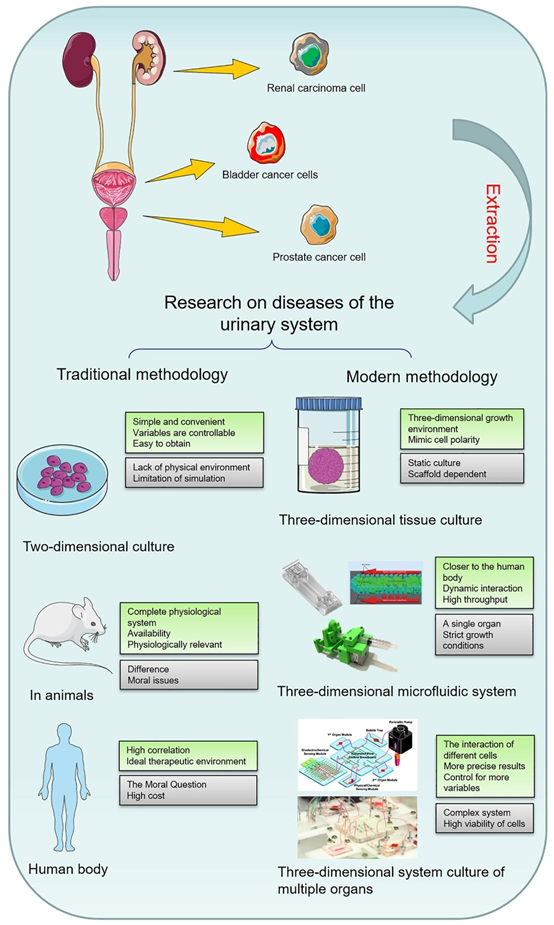
泌尿系统疾病模型
1. 微流体芯片在泌尿系统肿瘤中的应用
1) 膀胱癌(BCa)研究
无创诊断:基于尺寸筛选的微流体装置(如 5μm 孔径滤膜)可高效捕获尿液中的脱落肿瘤细胞(UETCs),结合抗 EGFR 抗体免疫分析,灵敏度达 95%,显著优于传统细胞学方法(35%);双滤膜结构(30-200nm)可分离尿液外泌体(EVs),通过 ELISA 定量分析实现 81.3% 的检测灵敏度。
肿瘤微环境模拟:BCa 器官芯片(如基于 BCG 疫苗的 3D 打印模型)可通过动态流场调控,评估免疫治疗药物的剂量效应,为个性化治疗提供依据。
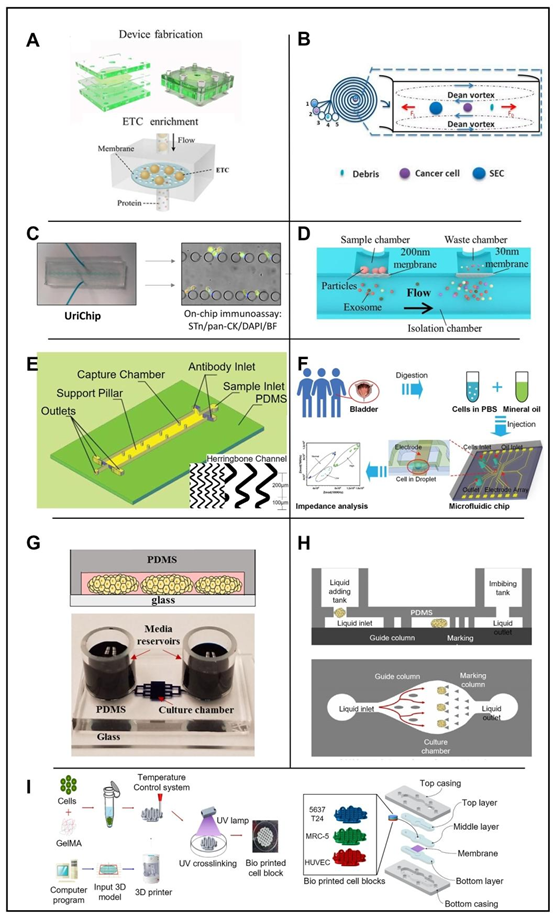
微流控技术在膀胱器官中的应用
在膀胱癌(BCa)研究中,微流体技术通过尿液检测实现无创诊断。针对 urinary exfoliated tumor cells(UETCs),基于尺寸筛选的微装置(如 5μm 孔径滤膜)可高效捕获细胞,结合免疫分析(如抗 EGFR 抗体)实现高灵敏度检测(95%),优于传统细胞学方法(35%)。 extracellular vesicles(EVs)的分离则采用双滤膜结构(30-200nm),通过 ELISA 定量分析,灵敏度达 81.3%。循环肿瘤细胞(CTCs)的捕获借助人字形通道设计,利用抗体修饰实现 90% 的捕获效率,为肿瘤分期提供依据。此外,BCa 器官芯片可模拟肿瘤微环境,如基于 BCG 疫苗的 3D 打印模型,能评估免疫治疗药物的剂量效应,为个性化治疗提供参考。
2) 前列腺癌(PCa)研究
标志物检测:微流体系统革新了前列腺特异性抗原(PSA)检测,如 Claros 系统通过指尖血实现即时检测(POC),与传统 Roche、Abbott 检测结果高度相关;基于微流控电泳的芯片可分析 PSA 糖基化特征(如 α2,3 – 唾液酸化),精准区分高分级 PCa。
循环肿瘤细胞(CTCs)捕获:涡流微流控芯片利用细胞尺寸差异分离 CTCs,捕获效率达 83.82%,优于商用 AdnaTest 系统,为转移监测提供新工具。
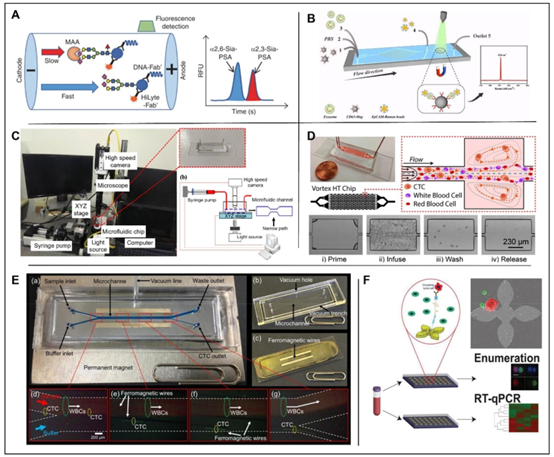
微流控技术在前列腺器官中的应用
前列腺癌(PCa)的诊断中,微流体芯片革新了前列腺特异性抗原(PSA)检测方式。Claros 系统通过指尖血实现 POC 检测,结合银放大免疫分析,与传统 Roche、Abbott 检测结果高度相关。针对 PSA 糖基化特征(如 α2,3 – 唾液酸化),微流控电泳系统可区分高分级 PCa,提升诊断特异性。外泌体检测采用 Raman 生物芯片,通过 CD63 抗体捕获和 EpCAM 标记,实现 PCa 患者与健康人的精准区分(p<0.0001)。CTC 分离则利用涡流微流控芯片和侧向磁泳技术,捕获效率(83.82%)优于商用 AdnaTest,为转移监测提供新工具。
3) 肾癌(RCa)研究
药物筛选:基于患者特异性肿瘤内皮细胞(TEnCs)的器官芯片可模拟血管微环境,评估抗血管生成药物的响应异质性,指导临床用药;类器官微球(如 Caki 细胞与间充质干细胞共培养)在微流控系统中可控生长,结合 5 – 氟尿嘧啶(5-FU)纳米递送系统,为转移性 RCa 治疗提供策略。
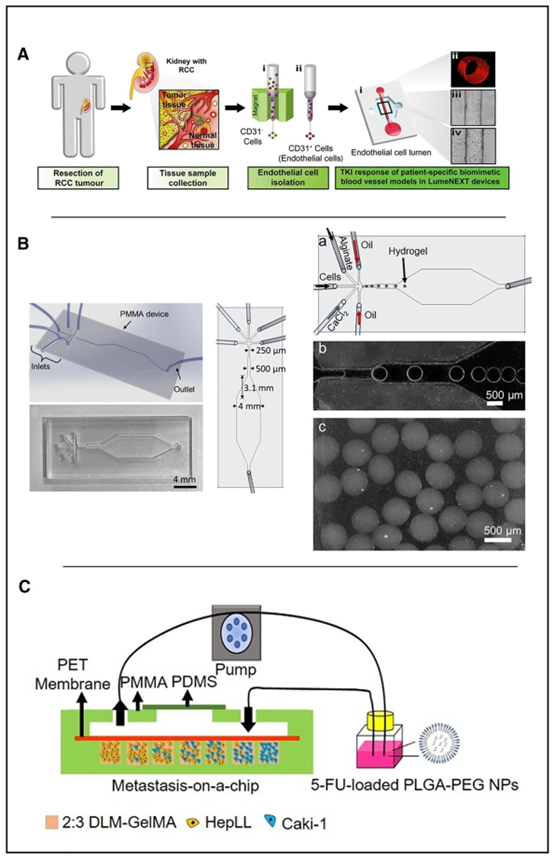
微流控技术在肾脏器官中的应用
肾癌(RCa)研究聚焦于无创诊断和药物筛选。细胞游离 DNA(cfDNA)的片段分析显示,RCa 患者血浆中 cfDNA 水平更高且片段更短,为早期诊断提供标志物。抗血管生成药物测试中,基于患者特异性肿瘤内皮细胞(TEnCs)的器官芯片可模拟血管微环境,评估药物响应异质性,指导临床用药。类器官微球(如 Caki 细胞与间充质干细胞共培养)在微流控系统中实现可控生长,结合 5 – 氟尿嘧啶(5-FU)负载纳米颗粒的递送研究,为 metastatic RCa 治疗提供新策略。
2. 挑战与未来展望
当前技术仍面临挑战:芯片标准化不足导致设备兼容性差,需建立通用接口(如标准 Ruhr 接头);制造误差影响数据重复性,需优化光刻、键合等工艺;仿生度有限,尤其 PCa 器官芯片的细胞类型与真实器官存在差异。未来发展将聚焦于多器官芯片的协同培养(如肠 – 肾轴模型)、智能整合 AI 图像分析与传感器技术,以及降低成本实现规模化应用。
当前技术仍面临瓶颈:芯片标准化不足导致设备兼容性差,需建立通用接口(如标准 Ruhr 接头);制造误差影响数据重复性,需优化光刻、键合等工艺;仿生度有限,尤其 PCa 器官芯片的细胞类型与真实器官存在差异。未来需推动多器官芯片协同培养(如肠 – 肾轴模型),整合 AI 图像分析与传感器技术,降低成本以实现规模化应用,最终为泌尿系统肿瘤的精准诊疗提供更强大的技术支撑。
微流体芯片通过融合 MEMS 加工、表面修饰(如 PEG 修饰载玻片)、3D 细胞培养等技术,在泌尿系统肿瘤的精准诊断、药物研发中展现巨大潜力。随着材料科学与工程技术的进步,其将进一步推动个性化医疗的实现,为替代动物实验、提升临床效率提供关键支撑。 器官芯片(OOC)作为微流体芯片的特殊类型,集成了细胞培养室、微流控系统、刺激 / 给药组件及生物传感器,可模拟人体生理微环境。其细胞培养方式涵盖 2.5D 和 3D 培养,前者依赖基底膜生长,后者通过三维基质实现细胞团簇化生长,更接近天然组织特性。驱动流体的 micropump 分为机械型(如蠕动泵模拟尿液间歇性流动)和非机械型(如重力驱动泵),配合 biosensors(如阻抗传感器、光学传感器)可实时监测细胞状态,为肿瘤微环境研究提供动态数据。
© 2025. All Rights Reserved. 苏ICP备2022036544号-1















