1. 微流控芯片:即时诊断技术的核心载体
在 COVID-19 疫情推动下,即时检测(POCT)技术成为体外诊断领域的研究热点。其中,微流控芯片凭借微型化、集成化、自动化的优势,成为实现 “样本到结果” 全流程诊断的核心载体。韩国庆熙大学团队研发的自容式微流控芯片系统,正是这一技术的典型代表 —— 该系统将核酸提取、反转录环介导等温扩增(RT-LAMP)、荧光检测等步骤集成于方寸之间,仅需 70 分钟即可完成呼吸道病毒(如 SARS-CoV-2、甲型流感、乙型流感)的精准检测。
从材料与加工来看,该芯片采用 3mm 厚 PMMA 板材通过 CNC 加工制成,结合PDMS 芯片常用的微通道设计理念,在 6.8cm×3.5cm×3mm 的空间内集成了 7 个功能腔室,包括裂解液、洗涤液、洗脱液等试剂存储区,以及冻干 RT-LAMP 试剂的反应区。这种设计不仅体现了微流控芯片加工的高精度要求,更通过MEMS 加工技术的微通道与阀门控制,实现了液体的精准分配与防交叉污染 —— 芯片内的石蜡阀门(熔点 58-62℃)与疏水被动阀门配合,既保证了试剂的长期存储稳定性,又能在加热时实现通道的精准开关。
2. 集成化设计:从试剂存储到多病毒检测的全流程创新
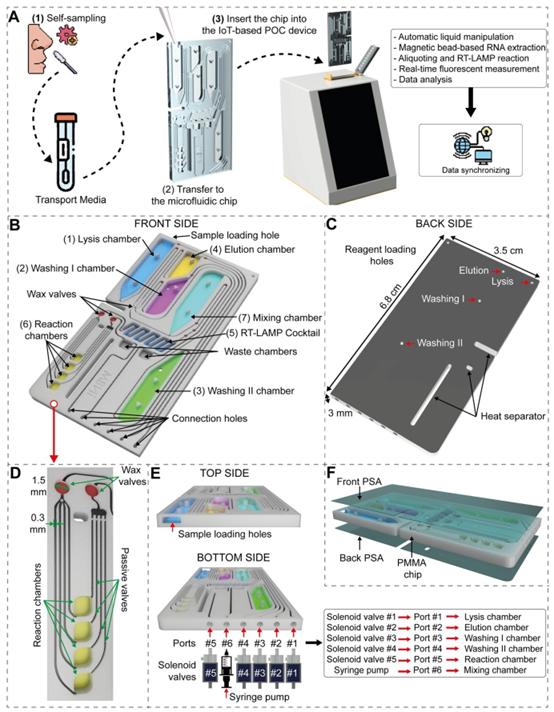
完全独立的微流控芯片设计。(A) 从样本收集到结果的拟议工作流程示意图。(B) 正面、(C) 背面、(D) 分液结构、(E) 顶部和底部的设计细节。(F) 微流控芯片的两侧均用PSA膜密封。
该微流控芯片的核心优势在于 “自容式” 设计,即预封装所有诊断所需试剂,无需外部添加,极大简化了操作流程。芯片内不仅包含液体状态的裂解缓冲液、洗涤缓冲液,还通过真空冷冻干燥技术将 RT-LAMP 反应 cocktail(含酶、引物、Mg²⁺等)与荧光染料(SYBR Green)预存于反应腔室,这种冻干试剂微流控芯片的设计思路,显著提升了系统的便携性与稳定性。
在检测功能上,芯片通过多重检测微流控芯片的设计理念,设置 4 个独立反应腔室,分别靶向人类 18S rRNA 基因(内参)、SARS-CoV-2 的 As1e 基因、甲型流感的神经氨酸酶基因、乙型流感的非结构蛋白 I 基因。通过微流控分液技术,RT-LAMP 反应液被均匀分配至各腔室,结合石蜡阀门的密封作用,实现了多病毒的同步检测且无交叉污染 —— 临床测试中,11 份样本(5 份 SARS-CoV-2、2 份甲型流感、4 份乙型流感)均被精准识别,印证了该设计的可靠性。
3. 物联网 POC 设备:微流控芯片的 “智能搭档”
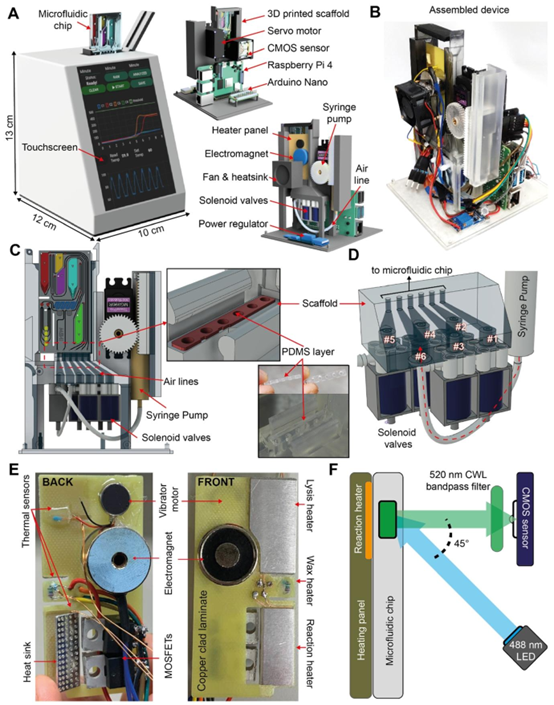
基于物联网的POC设备的开发。(A)设备的设计及其主要组件。(B)所制作的POC诊断设备的数字图像。(C)设备与(D)微流控芯片之间的接口细节以及用于液体操控的电磁阀系统。(E)用于区域温度控制、振动和磁力控制的加热面板细节。(F)用于实时荧光测量的光学设置细节。
为实现芯片的自动化运行,团队开发了基于物联网(IoT)的便携式设备,与微流控芯片形成 “芯片 – 设备” 协同系统。该设备以 Raspberry Pi 4 为控制核心,集成CMOS 传感器用于荧光信号采集、电阻加热板实现区域温控(65℃裂解、65℃RT-LAMP 扩增)、电磁阀与 syringe 泵控制液体流动,配合 5 英寸触控屏实现人机交互。
从技术集成来看,设备的硬件设计充分体现了智能微流控设备的特点:通过 Arduino Nano 实现加热的 PID 精准控制(温差 ±0.5℃),488nm LED 与 525nm bandpass 滤光片组成的光学模块保证荧光检测灵敏度,而 Node-RED 软件框架则实现了数据的实时传输与远程监控 —— 这一物联网微流控系统的设计,让诊断结果不仅能本地显示,还可同步至云端,为公共卫生监测提供数据支持。

基于物联网的POC设备的芯片上流控控制。(A)独立式微流控芯片的数字图像。(B)组装好的物联网-POC诊断设备的数字图像。(C)从裂解到RT-LAMP反应分液的整个过程细节。
4. 性能与优势:重新定义呼吸道病毒检测标准
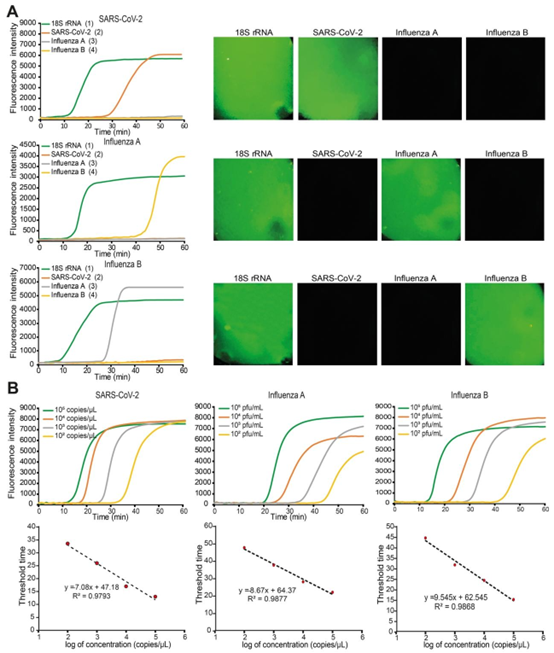
人类的rRNA基因、SARS-CoV-2的As1e基因、甲型流感的神经氨酸酶基因、乙型流感的非结构蛋白I基因,\((10^{3} PFU ml^{-1})\))和乙型流感(\((10^{3} PFU ml^{-1})\))。四个反应腔室预先包被了针对18S的特异性环介导等温扩增(LAMP)引物组。图4(A)使用SARS-CoV-2(\((10\)拷贝/μl)、甲型流感等样本在基于物联网的即时检测设备上进行分子诊断性能评估。左图显示荧光信号的实时检测结果,右图显示每个样本测试结束时反应腔室的荧光图像。(B)三种呼吸道病毒的检测限测试。
该微流控芯片系统在性能上实现了多重突破。灵敏度方面,对 SARS-CoV-2 的检测限达 1×10² copies/μL,对甲型、乙型流感的检测限达 1×10² pfu/mL,优于传统 lateral flow assays(LFAs),接近 RT-PCR 水平;速度上,从样本加载到结果输出仅需 70 分钟,远快于传统 RT-PCR 的数小时;成本上,整套设备硬件成本低于 500 美元,且微流控芯片可通过规模化生产进一步降低单次检测成本。
与现有技术相比,该系统的核心竞争力体现在三方面:一是自动化微流控平台的全流程整合,无需人工干预;二是便携式微流控设备的设计,支持电池供电,适用于野外、基层医疗等资源有限场景;三是多重检测能力,可同时识别多种呼吸道病毒,为合并感染诊断提供解决方案。
5. 应用前景:从实验室到临床的技术落地
该微流控芯片系统的研发,为呼吸道病毒检测提供了全新范式。在临床场景中,其可用于发热门诊的快速分诊,通过现场检测微流控系统实现 “即采即测”;在公共卫生领域,便携式设计使其能部署于机场、学校等场所,助力疫情早期筛查;而在资源匮乏地区,低成本与易操作性的特点可解决传统检测设备短缺的问题。
未来,随着微流控芯片加工技术的升级(如采用PDMS 模具实现更复杂微结构设计),以及器官芯片与微流控技术的融合,该系统有望拓展至更多领域,如病毒变异监测、其他病原体(如细菌、真菌)检测等。可以说,微流控芯片正从实验室技术逐步成为普惠医疗的关键工具,重新定义即时诊断的效率与可及性。
通过将微流控芯片的微型化优势与物联网技术结合,该研究不仅实现了呼吸道病毒检测的技术突破,更构建了 “芯片 – 设备 – 数据” 一体化的诊断生态。这种创新思路为微流控检测技术的产业化提供了重要参考,也为未来精准医疗与公共卫生防控奠定了硬件基础。
参考文献:DOI: 10.1039/d3lc00933e
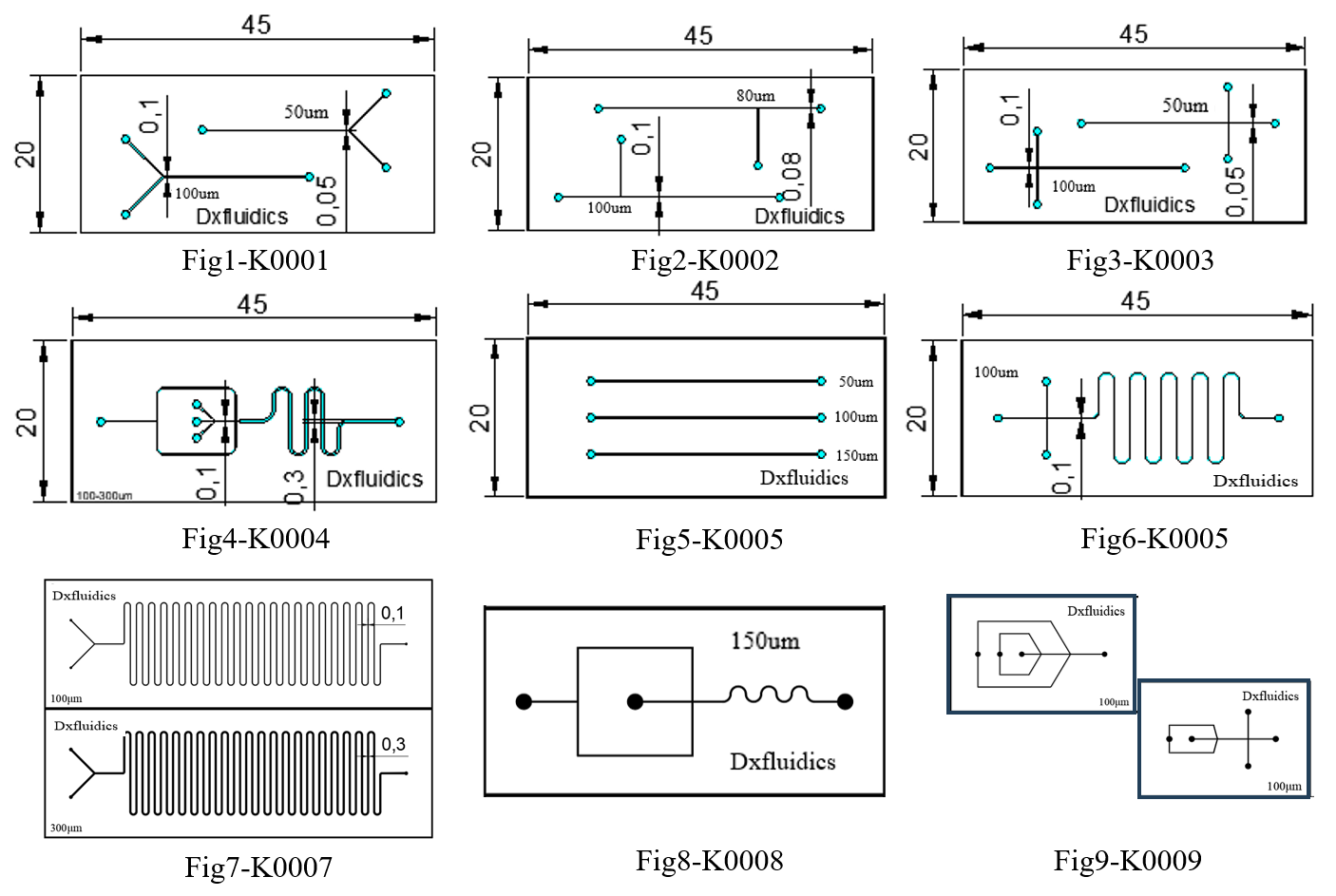
顶旭微控产品(标准PDMS芯片)
本公司也可提供特性化的微流控PDMS芯片加工服务,具体详情,欢迎来电咨询+86-18112558497(同微信),邮箱:sale@dxfluidics.com
| 产品编号 | 外形 (mm) | 高度 (um) | 宽度 (um) | 厚度 (mm) | 芯片材质 | 价格 (CNY) |
| K0001 | 45*20 | 50 | 50&100 | 3+1 | PDMS+Glass | 300 |
| K0002 | 45*20 | 50 | 80&100 | 3+1 | PDMS+Glass | 300 |
| K0003 | 45*20 | 50 | 50&100 | 3+1 | PDMS+Glass | 300 |
| K0004 | 45*20 | 50 | 100&300 | 3+1 | PDMS+Glass | 300 |
| K0005 | 45*20 | 50 | 50&100&150 | 3+1 | PDMS+Glass | 300 |
| K0006 | 45*20 | 50 | 100 | 3+1 | PDMS+Glass | 300 |
| K0007 | 75*25 | 100 | 100&300 | 3+1 | PDMS+Glass | 300 |
| K0008 | 52*25 | 100 | 100&150&200 | 3+1 | PDMS+Glass | 300 |
| K0009 | 35*24 | 100 | 100&200 | 3+1 | PDMS+Glass | 300 |
订购方式



© 2026. All Rights Reserved. 苏ICP备2022036544号-1













