参考文献:DOI 10.3389/fnagi.2025.1599509
1. 微流体芯片技术原理与时空梯度模拟
微流体芯片技术以微米级通道为核心,通过精准操控流体运动构建仿生微环境,其核心优势在于对体内 “时空梯度” 的动态模拟。 这类芯片多采用 PDMS(聚二甲基硅氧烷)、玻璃等透明且生物相容性优异的材料,经 MEMS 加工技术(如光刻、深硅刻蚀)制备而成,可集成微流道、梯度生成区、细胞培养室等功能单元,实现对化学浓度、流体剪切力等多参数的精确调控。
“时空梯度” 指微环境中化学因子(如炎症介质、氧浓度)的空间分布差异与时间动态变化的协同作用。 在生理状态下,血管内皮细胞受血流剪切力梯度调控,维持血脑屏障(BBB)的紧密连接; 而在病理过程中,炎症因子的浓度梯度会驱动神经炎症级联反应。 传统 Transwell 模型因静态培养无法复现这些动态信号,而微流体芯片通过分叉通道设计、流体力学调控,可生成稳定的化学梯度(如 TNF-α、IL-6 浓度梯度)和物理梯度(如 0-10 dyn/cm² 的剪切力梯度),为研究细胞对动态微环境的响应提供了理想平台。
2. 血脑屏障功能的动态调控机制
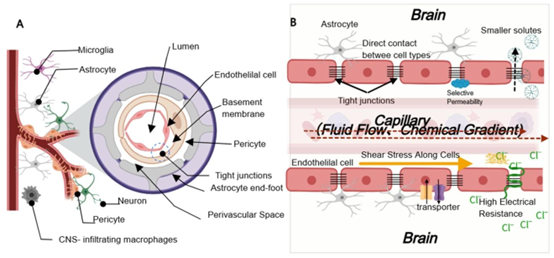
血脑屏障的组成及关键特征 (A) 横截面图展示了神经血管单元,其由内皮细胞、周细胞、星形胶质细胞、基底膜、神经元和免疫细胞组成。(B) 一个有效的体外血脑屏障模型应成功具备以下基本特征:(1) 表达功能性紧密连接的内皮细胞;(2) 与星形胶质细胞共培养以模拟生理条件;(3) 暴露于剪切应力以模拟血管动力学;(4) 对化合物具有选择性通透性;(5) 紧密连接处具有高跨内皮电阻(TEER)。
血脑屏障作为中枢神经系统的保护性屏障,由内皮细胞、周细胞、星形胶质细胞等构成,其完整性依赖于紧密连接蛋白(如 claudin-5、occludin)的表达与细胞间信号传导。微流体芯片通过构建多细胞共培养系统,揭示了微环境梯度对血脑屏障功能的复杂调控机制。
在化学梯度方面,低氧环境可激活内皮细胞的 HIF-1α 通路,上调 VEGF 表达,导致紧密连接蛋白降解;而炎症因子梯度(如 TNF-α)则通过激活 NF-κB 信号通路,增加血脑屏障通透性。物理梯度中,流体剪切力通过 PI3K/Akt 通路调控内皮细胞极性,高剪切力可促进 ZO-1 蛋白聚集,增强屏障功能。例如,在模拟血管脉动的微流控模型中,内皮细胞沿血流方向排列,PECAM-1 表达上调,显著提升血脑屏障的完整性。
3. 帕金森病病理演化的微环境机制
帕金森病(PD)的病理进程与血脑屏障功能异常密切相关。临床研究表明,PD 患者脑微血管中 claudin-5 和 occludin 表达下调,P – 糖蛋白功能受损,导致血脑屏障通透性增加,外周炎症因子(如 IL-6)和神经毒素(如 6 – 羟基多巴胺)渗入脑实质,形成局部浓度梯度。
微流体芯片通过构建 “黑质芯片” 模型,模拟了 PD 病理微环境的关键特征:将人诱导多能干细胞分化的多巴胺能神经元与血脑屏障内皮细胞共培养,引入 α- 突触核蛋白(α-syn)预制纤维后,可观察到 pSer129-αSyn 聚集、线粒体功能异常及神经炎症反应,同时伴随 TEER(跨内皮电阻)值下降,直观再现血脑屏障破坏与神经元退变的相互作用。此外,芯片模型还揭示了代谢梯度的作用 —— 线粒体功能障碍导致的能量分布失衡,会加剧多巴胺能神经元的氧化损伤,形成病理循环。
4. 微流体芯片的实验设计与模型构建
构建 PD 病理模拟模型需整合多参数调控策略。芯片设计常采用多层结构(如 PDMS 基片与玻璃层结合),通过交叉通道引入动态流体,利用多孔膜分隔不同细胞类型(如内皮细胞与星形胶质细胞),并集成 TEER 传感器实时监测屏障完整性。
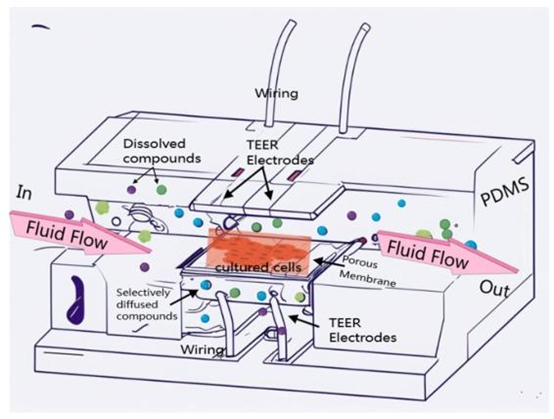
血脑屏障微流控芯片:在此,我们展示了一种先进的多层微流控装置,其设计灵感来源于罗斯·布斯等人,该装置由四个聚二甲基硅氧烷(PDMS)基板、两个玻璃层以及位于PDMS结构中心位置的多孔聚碳酸酯薄膜组成。该集成装置具有两条垂直相交的通道,用于动态引入流体;在通道交叉处设有多孔膜,以促进细胞培养;还嵌入了电极,用于监测跨上皮电阻(TEER)。
在功能验证方面,荧光 tracer 分析可量化物质跨屏障运输效率,而 Western blot 和免疫荧光则用于检测紧密连接蛋白(如 ZO-1)和炎症因子的表达变化。结合计算流体动力学(CFD)模拟,可预测芯片内梯度分布与剪切力场,优化实验参数。例如,通过调控 6 – 羟基多巴胺的浓度梯度,研究者在芯片中成功诱导 PC12 细胞的凋亡梯度,为 PD 神经毒性机制研究提供了量化模型。
5. 技术挑战与未来展望
当前微流体芯片技术面临标准化与生理相关性两大挑战。芯片制备依赖光刻胶模具与 PDMS 浇筑工艺,但不同实验室的材料选择(如 PDMS 与 COP)和加工流程差异,导致模型重复性不足;长期培养中细胞表型不稳定、多器官协同调控缺失等问题,也限制了其临床转化价值。
未来发展需聚焦多技术融合:利用 3D 打印构建复杂类器官芯片,结合 CRISPR 基因编辑优化细胞模型;通过 AI 算法整合多组学数据(转录组、蛋白组),实现梯度信号与分子机制的关联分析。跨学科协作将推动芯片标准化框架的建立,例如制定统一的 BBB 芯片性能评价指标(如 TEER 阈值、 permeability 标准)。此外,跨器官芯片(如脑 – 肠轴芯片)的开发,有望揭示 PD 系统性病理机制,为个性化药物筛选与靶向治疗提供全新平台。 微流体芯片技术通过复现生物微环境的动态特征,不仅深化了对血脑屏障与帕金森病相互作用的理解,更推动了从基础研究到临床应用的跨越。随着技术的不断迭代,其在神经退行性疾病机制研究与精准医学领域的应用前景将愈发广阔。
顶旭微控产品
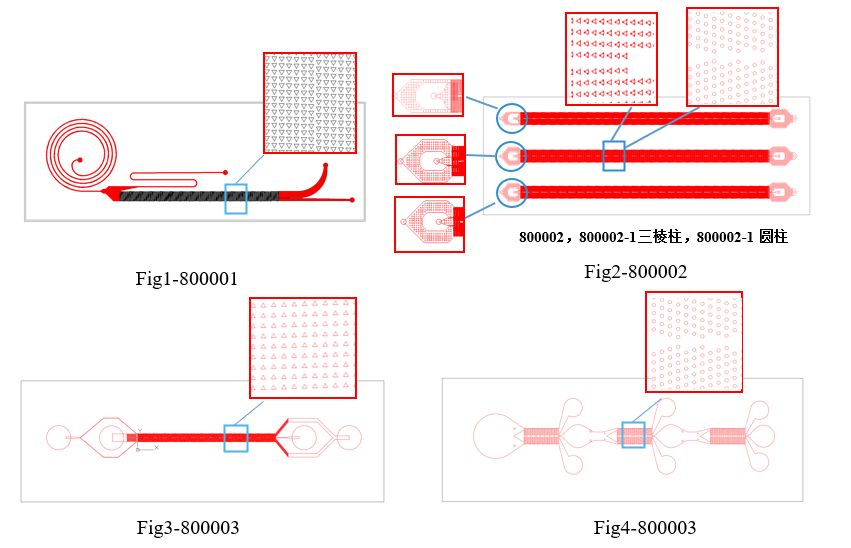
| 产品编号 | 外形 (mm) | 微柱 (um) | 偏移角度θ (um) | 柱间距λ (um) | 分选长度 (mm) | 流道高度 (um) | 材料 | 价格 (CNY) | |
| 形状 | 边长/直径 | ||||||||
| 800001 | 75*25 | 三角 | 60 | 2 | 85 | 35.5 | 50 | PDMS+玻璃 | 500 |
| 800002 | 75*25 | 三角 | 20 | 2 | 40 | 55 | 50 | PDMS+玻璃 | 600 |
| 800002-1 | 75*25 | 圆 | 30 | 2 | 40 | 55 | 50 | ||
| 800002-2 | 75*25 | 三角 | 20 | 2 | 40 | 55 | 50 | ||
| 800003 | 75*25 | 三角 | 30 | 2 | 65 | 28 | 50 | PDMS+玻璃 | 500 |
| 800004 | 75*25 | 圆 | 40 | 9 | 80 | 4mm*3 | 50 | PDMS+玻璃 | 500 |
订购方式



© 2026. All Rights Reserved. 苏ICP备2022036544号-1












