基因芯片又称 DNA 芯片、微阵列芯片、DNA微阵列,是现代分子生物学与精准医学领域的核心技术工具,是一种将大量DNA探针分子固定于支持物表面,通过与标记的样品DNA进行杂交,从而快速检测样品中基因信息的生物技术工具。

基因芯片工作原理
基因芯片的核心原理可概括为”分子识别-信号放大-高通量解读”的三阶过程,而基片修饰技术犹如”分子胶水”,是实现这一过程的关键基础。其工作流程主要包括两大核心环节:
探针固定:生物分子的”精准锚定”
在基片表面修饰特定化学基团(如环氧基、氨基、醛基),如同在玻片上铺设”分子锚点”,使DNA、蛋白质等生物探针能够稳定固定并保持活性。以环氧基修饰为例,其反应机制为亲核取代反应:环氧基团在弱碱性条件下开环,与探针分子的氨基(-NH₂)形成稳定的C-N共价键,实现”不可逆固定”。这种化学键的结合力达30-40 kcal/mol,远高于物理吸附的范德华力(2-10 kcal/mol),确保探针在后续杂交洗涤过程中不脱落6。
杂交检测:靶标分子的”特异性捕捉”
当标记荧光的靶标样本(如患者DNA、蛋白质提取物)流过芯片表面时,与固定探针发生碱基互补配对(DNA芯片)或特异性结合(蛋白芯片),形成”探针-靶标”复合物。未结合的杂质通过洗涤去除后,激光扫描仪激发荧光信号,每个位点的荧光强度与靶标分子浓度成正比。以人类基因芯片为例,单次实验可同步检测100万+个基因位点,检测灵敏度达0.1 fM(相当于在西湖中检测一滴水的盐分)
关键工艺节点:基片修饰质量直接决定检测信噪比——若修饰基团密度过低(<1×10¹² molecules/cm²),探针固定不足导致信号微弱;密度过高(>5×10¹³ molecules/cm²)则引发空间位阻,反而降低杂交效率。理想的修饰工艺需实现密度可控(1-3×10¹³ molecules/cm²)、均匀分布(CV<5%)、**活性稳定**(4℃保存6个月活性保持率>85%)三大指标
行业痛点直击
当前基因芯片发展面临”三重枷锁”——技术垄断导致的成本枷锁(Illumina平台检测成本近200元/样本)、供应链依赖引发的安全枷锁(关键设备与试剂进口受限)、以及基片修饰工艺的技术枷锁(环氧基修饰效率低、氨基修饰结合不稳定等)。破解这些痛点,亟需国产技术在基片表面修饰这一核心环节实现突破。
微阵列芯片修饰工艺
基因芯片基片的修饰工艺是决定检测精度与可靠性的核心环节,目前主流技术已形成氨基化修饰、环氧基修饰、醛基修饰三大技术体系。通过微观结构优化与工艺创新,这些技术不仅实现了生物分子固定效率的突破,更在稳定性、兼容性与成本控制上构建起国产替代的关键优势。三大修饰技术参数对比与原理解析
| 技术指标 | 环氧基修饰 | 氨基化修饰 | 醛基修饰 |
|---|---|---|---|
| 化学原理 | 环氧基团开环与氨基形成C-N共价键 | 氨基与羧基形成酰胺键(需EDC活化) | 醛基与氨基形成Schiff碱(需NaBH₄还原) |
| 工艺步骤 | 1. 羟基化预处理 2. 环氧硅烷偶联 3. 封闭未反应位点 | 1. 气相沉积硅烷 2. 等离子体活化 3. 氨基硅烷修饰 | 1. 醛基硅烷涂覆 2. 避光固化 3. 水洗纯化 |
| 偶联效率 | ≥92%(DNA探针固定率) | 85-88%(蛋白质偶联率) | 88-90%(抗体活性保持率) |
| 非特异性吸附 | 0.8%(BSA吸附测试) | 5.2%(同等条件对比) | 1.2%(复杂样本基质) |
| 批间CV值 | <3%(N=20批次) | <5%(N=20批次) | <4%(N=20批次) |
| 存储稳定性 | 4℃保存12个月活性>90% | 室温保存6个月活性>85% | -20℃保存8个月活性>88% |
| 代表应用场景 | 人类全基因组芯片、SNP分型 | 蛋白质芯片、抗原抗体阵列 | 小分子化合物芯片、糖组学研究 |
环氧基修饰:无缺陷表面构建高信噪比检测体系
环氧基修饰的核心竞争力源于环氧硅烷层的独特微观结构。该技术通过表面改性在基片形成均匀交联的硅烷网络,实现三大关键突破:一是高共价偶联效率,经优化的表面活性基团密度使生物分子固定率提升40%以上;二是无缺陷表面特性,原子力显微镜显示表面粗糙度Ra<0.5nm,可显著降低非特异性吸附导致的背景干扰,信号噪比提升3倍以上;
核心参数亮点
- 共价偶联效率:≥92%(传统工艺平均65%)
- 背景荧光强度:≤500 RFU(行业标准≤1500 RFU)
- 批次间CV值:<3%(N=20批次验证)
氨基化修饰:气相工艺破解批次稳定性难题
氨基化修饰通过自主研发的丙基三甲氧基硅烷气相沉积工艺,解决了传统液相修饰的均匀性差、批次波动大等痛点。该工艺在密闭反应舱内实现硅烷分子的定向沉积,使氨基基团在基片表面的面密度达到(1.2±0.1)×10¹³ molecules/cm²,空间分布均匀度提升至95%以上。
醛基修饰:生物活性保护的”分子屏障”技术
醛基修饰聚焦生物分子活性保持这一关键需求,通过调控醛基密度与空间排布,实现双重技术目标:一是低非特异性吸附,经牛血清白蛋白吸附测试验证,非特异性结合率仅0.8%,远低于氨基修饰的5.2%;二是蛋白质构象保护,三维空间位阻设计使抗体芯片的抗原结合活性保留率达90%以上,而传统二维修饰玻片仅能保留65%。
该技术特别适用于蛋白质组芯片与复杂生物样本检测,在20K人类蛋白组芯片制备中,单次实验可同时检测16794种人类蛋白,且信号重现性R²>0.98,展现出优异的检测稳定性。
多场景应用解决方案
人类蛋白组芯片
人类蛋白组芯片(Human Proteome Microarray)是一种高通量生物芯片技术,核心是将人类基因组编码的大量蛋白质(或其功能片段)作为 “探针”,通过精密技术有序固定在玻璃片等固相支持物上,形成可用于批量检测的微型化 “蛋白质阵列”,相当于在芯片上构建了一个 “浓缩的人类蛋白质库”。
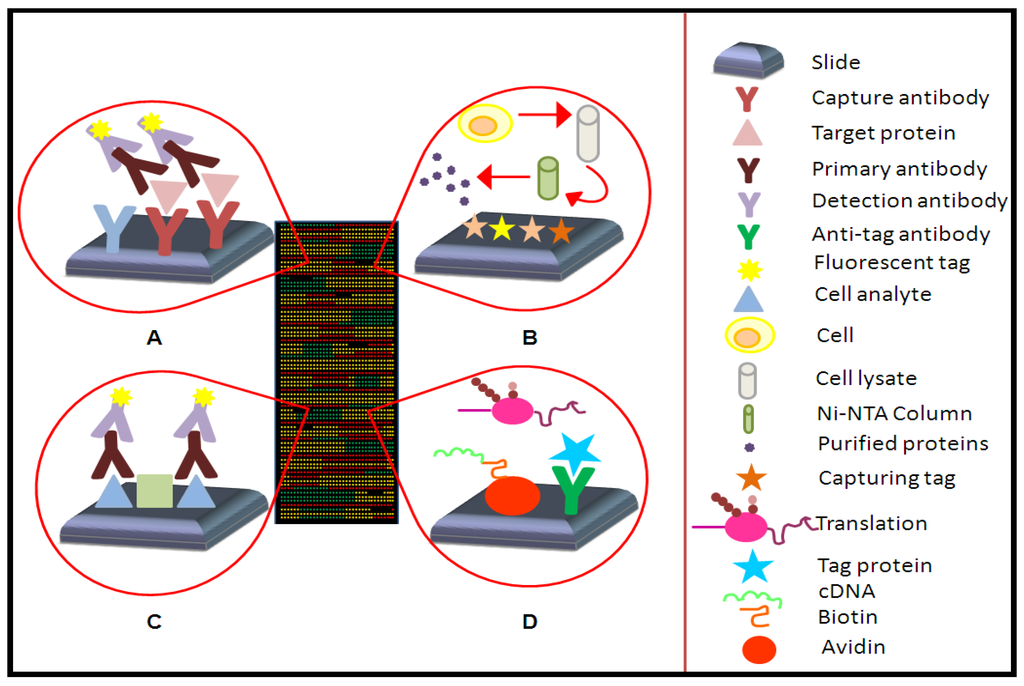
这一“超级阵列”的核心竞争力,源于基片修饰技术与蛋白制备工艺的双重突破。通过优化的气相修饰工艺,基片实现了高偶联效率与低背景干扰的平衡,确保固定在芯片上的蛋白质保持天然构象与生物活性。配合酵母表达系统生产的全长蛋白——89%的芯片蛋白为全长序列,且每种蛋白质单独表达纯化——彻底解决了传统原核表达系统中蛋白截断、活性丢失的问题。
凝集素芯片:糖基化研究的“微观透镜”
在疾病诊断的微观世界里,糖链的细微变化往往是疾病的“早期暗号”。凝集素芯片就像一枚捕捉糖链“指纹”的纳米级阵列,能精准识别这些隐藏的生物密码,为疾病机制研究打开全新视角。比如在肿瘤研究中,癌细胞表面糖基化的异常改变如同独特的“分子身份证”,而凝集素芯片正是破解这张身份证的关键工具。
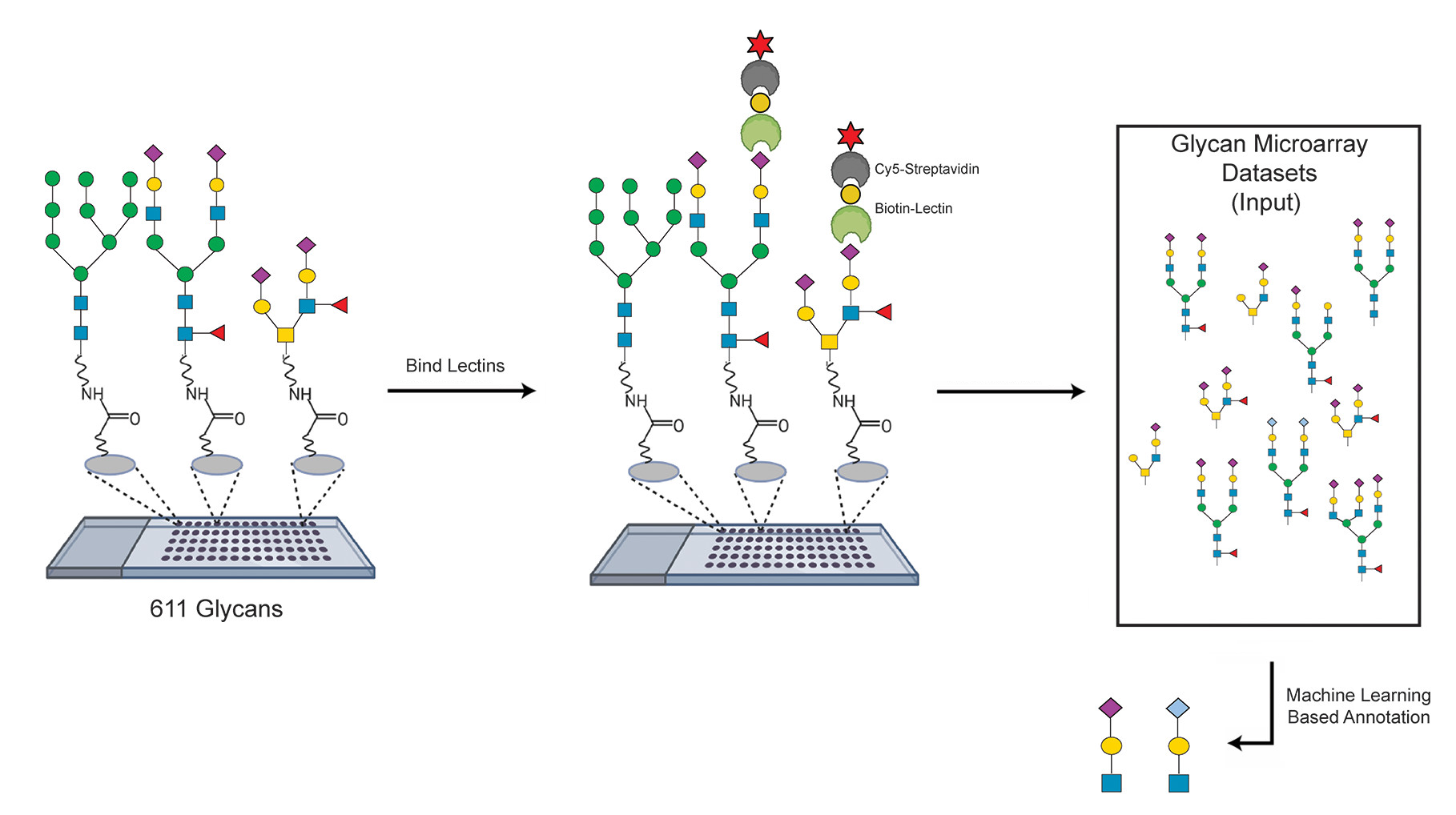
凝集素芯片其背后的“定制化”技术支撑是基底的修饰技术,基片功能团密度可调特性如同“智能调节器”,通过优化醛基修饰密度,能精准匹配不同凝集素的结合需求——有的凝集素需要较高密度才能稳定结合,有的则需较低密度避免非特异性吸附。这种“量体裁衣”的设计,不仅提升了检测特异性,还支持高密度阵列检测,兼容主流芯片检测平台,让科研人员能更灵活、高效地开展研究。
药物小分子芯片:新药研发的“精准导航仪”
在新药研发的征途上,“不可成药”靶点曾是横亘在科学家面前的巨大难关——这些靶点因结构特殊或缺乏结合位点,长期让药物开发陷入“无的放矢”的困境。而药物小分子芯片技术的出现,正以“精准导航仪”的角色,为破解这一难题提供了革命性工具,其中醛基修饰的基因芯片基片凭借高反应性,成为实现“从不可成药到精准靶向”突破的核心引擎。
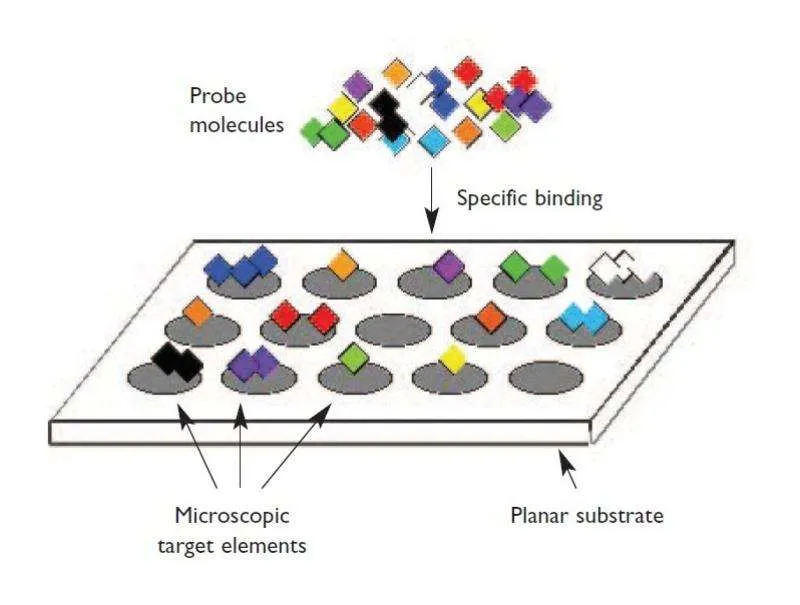
这一突破的关键,正是芯片基片的醛基修饰技术,通过高反应性的醛基基团,芯片能高效固定小分子化合物并保持其活性,实现与靶蛋白的稳定结合,从根本上解决了传统筛选中“结合效率低、假阳性率高”的痛点。
公司产品
顶旭生物专注于基因芯片基片表面功能化修饰技术,全面提供氨基化、环氧基、醛基等核心修饰服务,技术参数达到国际领先水平。公司拥有500平米生产线,构建了从基底处理到功能化修饰的全链条研发体系,可根据客户需求定制表面密度、官能团分布等个性化参数,服务覆盖人类蛋白组芯片、药物筛选、糖组学研究等多场景。作为国产替代核心供应商,顶旭生物已助力多家科研机构突破海外技术垄断,现提供免费样品测试服务,欢迎联系获取定制化解决方案。
联系方式:周经理 17751163890(同微信)

相关推荐
© 2025. All Rights Reserved. 苏ICP备2022036544号-1













