在当前医学疾病研究领域,临床病人仍是最可靠的疾病研究对象,但是出于伦理原因以及其他无法直接从活的人体获取样本的限制,亟需开发其他稳定、可靠、可重复的疾病研究模型,替代以人为研究对象的疾病模型。
以正常或者病人来源的细胞或组织为研究对象,体外构建具有与人体组织器官相似结构和功能特征的模型是疾病研究的重要领域,其中类器官和器官芯片是有望解决上述难题的最具潜力的技术。

传统的体外疾病模型主要包括细胞模型,培养方式主要是二维(2D)静态。这种方式培养的细胞能够维持细胞的部分生物学功能,但缺乏体内多细胞相互作用、细胞-细胞外基质(ECM)以及理化刺激等多种必要微环境因素,使得单一的细胞静态培养无法真实模拟人体组织器官的生理和病理状态。
动物模型虽然可以模拟多细胞、多组织器官等相互作用的生理和病理过程,但是由于种属和遗传背景差异性以及动物伦理学等限制,使得对发生在人类身上的疾病,难以在动物身上完全再现,甚至还会得出与人体疾病相悖的结论。
类器官(organoid)是由多能干细胞和成体干/前体细胞在体外通过细胞自组装等方式形成的包含多种细胞组分、具有源组织器官结构和功能特点的“迷你”器官。
在模拟人体组织器官发育、机体稳态、疾病机制研究和药物开发等领域逐渐展示其巨大的应用前景。
目前,类器官培养方式主要包括基质胶包埋、悬浮动态培养手段,通过在适宜的培养基中添加营养物质和特定的生长因子等,实现促进细胞的分裂增殖、定向分化以及空间结构的形成。
保证类器官在特定的培养系统中既要维持干细胞的自我更新,也要保证分化细胞维持特定的结构和功能。
器官芯片(Organ-on-a-chip)是近10年来迅速发展起来的变革性新技术。它基于微流控芯片技术在体外模拟人体组织器官功能单元的微型细胞/组织培养载体,包括功能单元必须的基本元件和元素,如多细胞组分、细胞外基质、微环境理化因素等。
器官芯片可以弥补现有细胞培养方式的不足,具有传统方法无法比拟的优势:包括三维动态培养、可控的理化刺激、成本低、通量高、可靠性强等。
同时,器官芯片结合成像仪器实时监控细胞生物学变化等,更好地记录细胞在疾病状态下的行为学变化以及对药物反应的全过程。

而 类 器 官 芯 片(organoids-on-a-chip) 是 类 器 官 与 器 官 芯 片两种技术优势的结合,通过集成微流控技术实现更精准、更可控的类器官模型构建,能够控制与模拟组织的微环境、血管化、组织间相互作用,并助力类器官模型的高通量分析。
类器官芯片结合了医学生物学和工程学的优势,能有效解决传统类器官培养技术的局限,不仅能实现细胞的3D培养,重现细胞之间以及细胞与基质之间的相互关系,而且可模拟靶器官在体内的间质流体、机械力刺激等重要的体内微环境。
通过实时成像、传感器等技术,类器官芯片在仿生的微环境中研究个体遗传发育、疾病发生发展机制、药物筛选以及免疫评价中具有无可比拟的优势。
类器官芯片尺寸小,且具有多个培养腔,能提高实验通量,适合多组对照实验同步进行,可用于器官发育模型或疾病模型的构建、药物研发、免疫评价等领域,大大减少个体差异性和实验周期,让单个类器官的研究成为可能,为临床前研究提供有力的论证。
类器官芯片关键应用领域
器官发育模型的构建及发育生物学的研究
类器官芯片可准确模拟靶器官的组织结构,将微通道作为可溶性因子的来源与分布途径,控制ECM中生化浓度梯度的分布,诱导类似体内组织区域化。
例如,将微通道与模式化培养支架相结合,将干细胞和分化的上皮类器官分别局限于类肠道结构中的隐窝和绒毛。
细胞间相互作用在维持内环境稳定和信号转导等方面非常重要,类器官芯片运用集成培养腔可体外模拟多器官之间的相互作用。
类器官芯片共培养体系主要有以微液滴、微接触印刷为代表的接触性共培养和以水凝胶、半透膜、窄通道为代表的非接触性共培养两种方式。
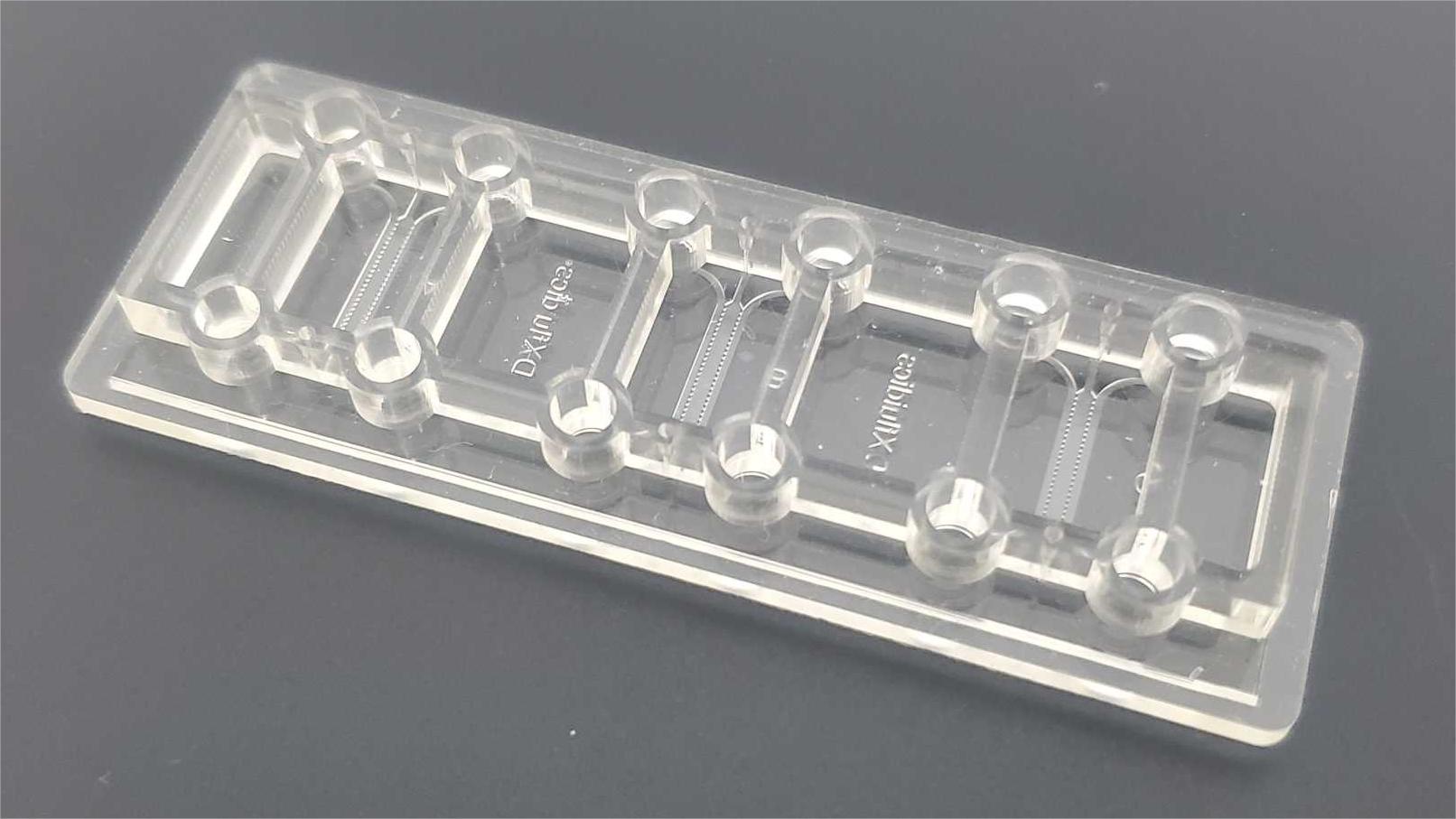
疾病模型的构建及应用研究
疾病模型构建是癌症研究的一大难点,包括肿瘤发生发展、发育障碍、微生物感染等。在类器官芯片上培养患者来源的肿瘤细胞或者诱导性多能干细胞(iPSCs),在构建特异性疾病模型方面具有很大的潜力,能实现患者“个性化”治疗。
缺乏宿主细胞-微生物相互作用的生物模型是人类对微生物的致病机制研究的一个重大阻碍。类器官芯片可集成多功能结构单元,在一定程度上能实现细菌和细胞对氧气浓度的不同要求以及体细胞与微生物共培养实验的长期性。
药物开发和研究
药物研发需要考虑药物的药代动力学、毒副作用、递送系统效率等,但由于缺乏实际可控的临床模型而使药物研发过程变得昂贵而漫长。
类器官芯片基于其高通量、集成度高、重现性等优点可减少药物研发成本,被广泛运用在药物筛选和药物分析等领域。
在仿生微环境中模拟不同器官的结构和生理过程,重现器官间的相互作用和串扰,能够进行更复杂、更有生理学意义的药物研究。
有研究表明,结合微血管的心脏-肝-肠共培养芯片成功模拟了药物的吸收、分配、代谢、排泄和毒性动力学过程(ADMET),可再现药物在体内的代谢过程。
利用多腔室及兼容给药浓度梯度发生器的高通量类器官芯片是近年来药物研发或“个性化”药物治疗的新方法,在短时间内自动化处理多种不同浓度的药物组合,提高药物研发的效率。
类器官芯片可通过对微柱阵列尺寸的优化来控制类器官的大小和均匀度,以减少实验误差。
免疫反应
类器官在培养过程中会丢失一部分免疫细胞、关键基质细胞和细胞因子,这会限制患者来源的类器官在化疗和靶向药物筛选中的功能测试。
研究表明癌症和免疫细胞的相互作用具有个体差异和器官差异性,因此通过类器官芯片共培养肿瘤类细胞和免疫细胞,并通过微流控模拟肿瘤微环境和捕捉细微动态的变化,或许能克服这一困境。

亟需解决的问题
类器官与类器官芯片制造的研究目标,其一是精准模拟人体器官的微环境与各功能组分之间的功能关系,从而建立疾病模型,进行药物筛选和毒性测试,提供个性化医疗方案;其二是在近未来能够使用体外构建的组织或器官来替换人体内患病或老化的组织或器官,发展在组织工程与再生医学领域中的临床应用。
然而,实现类器官与类器官芯片技术的研究突破还面临诸多障碍与挑战。
其一,环境与细胞、细胞与细胞之间的交互关系错综复杂,尚有许多相互作用未被发现或未被研究清楚,这种未知性为精准控制细胞交互关系的目标带来困难,大语言模型等人工智能技术有潜力帮助这类难题的解决。
其二,类器官的自组织是一个极度动态的过程,在其发育发展过程中保持可控制性和可预测性是具有挑战性的,既需要更深入地了解自组织的生物学机制,也需要实时动态监测,还需要实时及时地介入工程化调控和干预的手段。
其三,在类器官的研究应用与平台的构建中都涉及到复杂的伦理问题,包括对干细胞的使用、组织来源的合规性、患者数据的隐私安全性等,需要根据技术进步合理调整伦理标准与法规,确保在技术发展过程中保护个体的权益和确保研究的合法性,同时不阻碍技术的积极进步。
关于我们
顶旭(苏州)微控技术有限公司是一家专注于微流控领域的高科技企业,我们致力于为客户提供微流控芯片定制、表面修饰改性、微流控芯片加工设备、以及微流控仪器等全面的微流控解决方案。公司团队拥有丰富的经验和技术积累,持续将专业知识与创新思维相结合,为客户提供高品质的解决方案。我们将始终坚持以客户为中心,不断挑战自我,不断追求卓越,通过专业、创新和合作,为客户创造更大的价值,共同开创微流控领域的美好未来。
© 2025. All Rights Reserved. 苏ICP备2022036544号-1
















