全细胞生物催化是精细化工合成、生物制药与绿色生物制造领域的核心技术,酿酒酵母等微生物细胞凭借广泛的底物适配性、多样的催化反应类型,成为实验室研发到工业化生产中应用最广泛的全细胞生物催化剂。长期以来,行业内对全细胞生物催化剂性能的认知,均基于数百万个细胞的群体平均数据,却忽略了同基因细胞群中显著的细胞间异质性。单细胞层面的生物催化转化分析,始终是行业亟待突破的技术瓶颈,而微流控芯片技术与质谱检测的融合发展,为解决这一难题提供了全新路径。
1. 微生物单细胞生物催化分析的行业痛点与技术局限
现有单细胞分析技术中,转录组学、代谢组学与蛋白质组学虽已揭示了细胞内成分的异质性,却无法精准回答单个微生物细胞的核心催化性能 —— 单位时间内底物的消耗量、产物的生成量,以及产物的化学特异性与纯度。质谱技术是唯一能在单细胞水平解答上述问题的分析手段,但此前的单细胞质谱研究多集中于体积较大的哺乳动物细胞,针对微生物细胞的单细胞催化分析始终难以突破。
核心技术难点集中在三个方面:一是微生物细胞体积微小,分泌的产物在胞外环境中极易被稀释,浓度远低于常规检测方法的检出限;二是传统液滴微流控体系依赖表面活性剂维持液滴稳定,而表面活性剂会严重抑制质谱电离效率,导致目标产物信号无法被有效检测;三是现有技术难以实现单细胞封装、产物孵育、细胞计数与质谱检测的无缝衔接,检测通量极低,无法满足生物催化研究的实际需求。即便此前的研究通过微流控芯片与质谱联用实现了十余个细胞的催化产物检测,却始终无法突破单细胞分辨率的技术壁垒。
2. 集成化微流控 – 质谱联用平台的设计与搭建
本研究创新性地构建了一套集液滴微流控单细胞封装、在线成像细胞计数与电喷雾质谱定量检测于一体的分析平台,通过微流控芯片设计、材质选型与系统集成的全方位优化,攻克了微生物单细胞生物催化定量分析的核心难题。
在微流控芯片加工与体系设计上,研究团队采用选择性激光诱导蚀刻技术加工的熔融石英玻璃芯片,相比常规 PDMS 芯片,玻璃芯片具备优异的化学稳定性、低表面吸附性与光学通透性,可实现无死体积的标准毛细管无缝连接,精准生成纳升级别的均一液滴。同时,团队摒弃了传统 PDMS 微流控体系中必需的表面活性剂,采用氟化毛细管实现 3nL 体积液滴的长期稳定储存与孵育,既避免了液滴融合,又从根本上解决了表面活性剂导致的质谱离子抑制问题,大幅提升了检测灵敏度。微流控芯片的微通道精准设计,依托先进的 MEMS 加工与微纳加工技术实现,而光刻机、光刻工艺制备的 SU8 光刻胶模具、硅模具,也为 PDMS 芯片加工与微流控芯片的规模化制备提供了成熟的技术支撑。
在单细胞分析流程的集成上,平台实现了 “单细胞封装 – 产物孵育 – 在线细胞计数 – 质谱定量检测” 的全流程自动化。通过微流控芯片将单个微生物细胞与反应底物共同封装于纳升液滴中,经长时间孵育实现产物的有效富集;在液滴进入质谱检测前,通过在线显微成像系统完成每个液滴内细胞数量的精准计数,结合时间戳标记实现液滴成像数据与质谱信号的一一对应,彻底解决了单细胞分析中数据归属的核心问题;最终通过同轴电喷雾离子源,将孵育后的液滴直接送入质谱系统,采用多反应监测模式实现目标产物的高特异性、高灵敏度定量,方法检出限低至 0.25μM,采样速率可达 0.8 样本 / 秒,实现了单细胞水平的高通量分析。
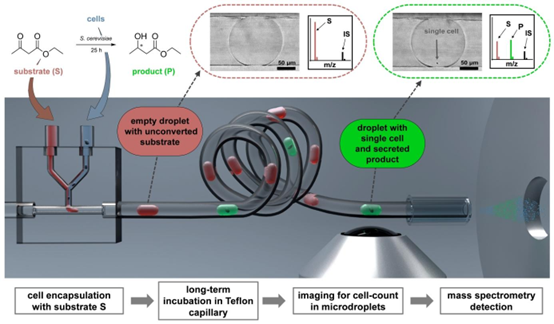
图1. 所提出的基于毛细管的方法通过电喷雾电离质谱检测研究单细胞催化转化的示意图。该平台包括用于细胞封装的玻璃芯片、在特氟龙毛细管中的液滴储存和孵育,以及液滴分析(细胞成像和质谱检测)。将底物(S)和细胞悬液混合并封装到液滴中,这些液滴被无缝转移到特氟龙毛细管中以延长反应时间。在没有细胞的液滴中,底物不会被转化(红色虚线圆圈包含空液滴的照片和示意性质谱图)。在含有单细胞的液滴中,酿酒酵母会将底物还原为相应的羟基产物(P)(绿色虚线圆圈包含含有一个细胞的液滴照片和示意性质谱图)。在检测前确定每个液滴中的细胞数量后,通过质谱法使用内标(IS)对不同液滴中积累的产物进行定量。
3. 核心研究结果与单细胞催化异质性的突破性发现
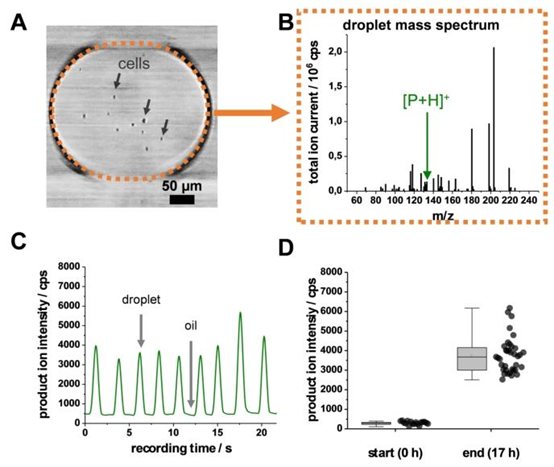
图2. 在15纳升液滴中对所研究的模型反应的评估。A)在300微米内径和1.59毫米外径的管道中,含有细胞(酿酒酵母)的液滴的显微图像。B)单个液滴的典型质谱图,其中信号对应于质子化产物离子\([P+H]^{+}\)。C)每滴含10-15个细胞的反应中产物离子的典型质谱离子计数轨迹(表现为峰),处于连续油相(表现为信号谷)中。D)反应开始时和结束时(17小时)对液滴的评估。每个数据点代表来自单个液滴的产物离子强度,每个液滴含10-15个细胞(\((N=53)\))。
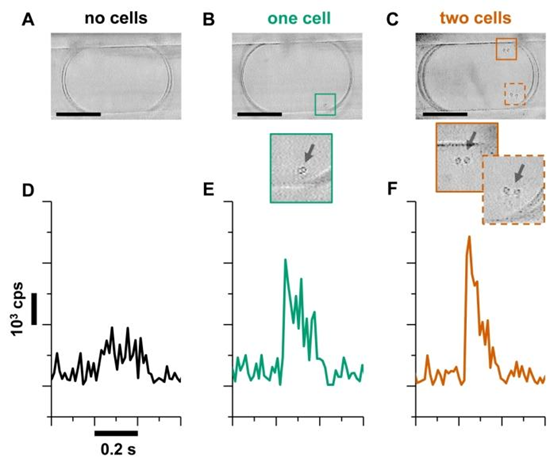
图3. 基于可视化(A)–(C)和ESI-MS(D)–(F)的单细胞分辨率液滴分析。不含细胞的反应混合物空液滴(A)、含一个细胞的液滴(B)和含两个细胞的液滴(C)在反应结束时(25小时)的对比,以及对应的无细胞液滴(D)、含一个细胞的液滴(E)和含两个细胞的液滴(F)的产物离子轨迹。可以在细胞(酿酒酵母)中观察到典型的芽体形成。比例尺:100 μm。
研究以酿酒酵母全细胞催化乙酰乙酸乙酯不对称还原为 3 – 羟基丁酸乙酯为模型反应,完成了平台性能的全面验证,首次实现了微生物单细胞生物催化转化的精准定量。
实验结果显示,该平台可精准区分空液滴、含单细胞液滴与含多细胞液滴的质谱信号差异,通过内标法完成了单液滴内产物浓度的绝对定量。在 25 小时的反应周期后,含单个酿酒酵母细胞的液滴中,产物平均浓度达 0.55μM,远高于方法定量限,最终计算得到单细胞平均产物生成速率为 0.071 fmol/h/ 细胞,高产细胞的产物生成速率可达 0.23 fmol/h/ 细胞,与群体水平的研究数据高度吻合,验证了方法的准确性。
更具行业价值的是,该研究首次在单细胞水平揭示了同基因酿酒酵母细胞的生物催化异质性:研究发现 26% 的被测细胞产物生成速率低于 0.017 fmol/h/ 细胞,而高产细胞的催化活性是低产细胞的数十倍。这一核心发现,是传统群体水平研究完全无法实现的,为生物催化剂的定向进化、高产菌株筛选提供了全新的单细胞分辨率视角。
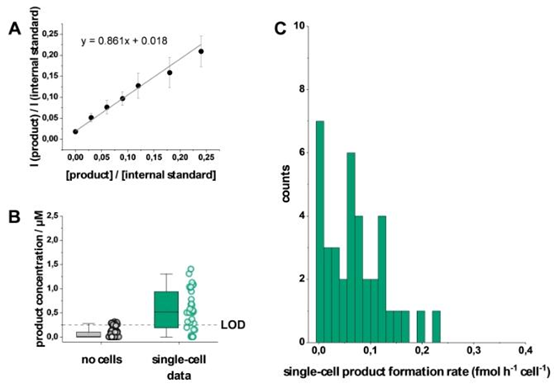
图4. 单细胞特异性产物形成速率的测定。A) 含有产物和内部氯化标准物的液滴校准曲线。B) 反应25小时后,空液滴(无细胞)和含一个细胞的液滴(单细胞数据)中每滴浓度的箱线图;\(N=129\)。虚线表示检测限(0.25μM)。C) 单个细胞的单细胞产物形成速率以直方图形式绘制;\(N=38\)
4. 技术优势与行业应用前景
该集成化微流控 – 质谱联用平台,突破了微生物单细胞生物催化分析的长期技术壁垒,具备三大核心行业优势:一是首次实现了微生物单细胞分泌催化产物的化学特异性、高通量定量分析,填补了全细胞生物催化单细胞研究的技术空白;二是无表面活性剂的液滴体系,解决了传统液滴微流控 – 质谱联用的核心痛点,为微流控芯片与质谱的联用技术提供了全新的设计思路;三是在线成像与质谱检测的无缝衔接,实现了细胞表型与催化性能数据的精准关联,为单细胞生命科学研究提供了通用型技术平台。
在行业应用层面,该技术可直接应用于全细胞生物催化剂的定向进化与高通量筛选,通过单细胞水平的性能评价,大幅缩短高产菌株的筛选周期,提升生物催化工艺的开发效率;同时可拓展至微生物代谢网络的机制研究,揭示细胞异质性的分子基础,为代谢工程改造提供精准的实验依据。此外,该平台可灵活适配不同的微流控芯片定制需求,不仅可用于微生物单细胞分析,还可拓展至 3D 细胞培养芯片、类器官芯片、多器官芯片体系,实现单细胞水平的药物代谢、毒性评价与疾病机制研究,为生物制药、精准医疗、环境微生物检测等领域提供核心技术支撑。随着微纳加工技术的不断进步,定制化微流控芯片加工与微流控系统的集成化发展,将进一步推动该技术的产业化落地,成为单细胞生命科学研究与生物制造产业升级的核心工具。
参考文献:doi.org/10.1002/ange.202204098
© 2026. All Rights Reserved. 苏ICP备2022036544号-1













